Форма и геометрические размеры
Реакционной зоны
Форма и геометрические размеры поверхности контакта металла и газовой струи всегда интересовали металлургов с тех пор, как было освоено применение воздуха, а позднее и кислорода для продувки металлических ванн сталеплавильных агрегатов в интересах форсирования протекающих в них процессов и увеличения их производительности.
Для исследований широко применялись визуальные наблюдения за ходом продувки в промышленных агрегатах, "холодное" и "горячее" моделирование, скоростная фото- и киносъемка, звукозапись и т.п. Благодаря этому накоплен обширный материал о форме и размерах реакционной зоны при подводе кислорода к металлу как сверху, так снизу или сбоку. Рассмотрим подробнее наиболее часто встречающуюся на практике продувку сверху.
При небольших удельных расходах кислорода, как правило, связанных с незначительными (дозвуковыми) скоростями истечения газа из сопла фурмы и с малыми давлениями кислорода перед соплом, форма реакционной зоны напоминает воронку, обращенную вершиной вниз (рис. 19). Естественно, эта форма реакционной зоны лишь приблизительная, обобщающая и усредняющая многочисленные и существенные изменения формы поверхности металла, некоторое каплеобразование, отдельные отрывы и даже выбросы небольших объемов металла и т.п. Размеры такой "открытой" реакционной зоны определяются по уравнениям И.Г. Казанцева [76] или Л.М. Ефимова [77].
Диаметр воронки определяется размерами струи на уровне встречи ее с поверхностью металла и некоторым кольцеобразным зазором вокруг нее, образуемым отходящими из этой зоны газами СО и отраженным не полностью ассимилированным кислородом.
d3³d (x1/d B+1), (79)
где х1 – расстояние от среза сопла до поверхности спокойного металла;
d3 и d – диаметры реакционной зоны и сопла фурмы;
B – эмпирически определяемая постоянная для данной формы сопла и данного динамического напора истекающего газа.
Наибольший интерес, несомненно, представляет глубина проникновения струи газа в толщу металла после неупругого соударения с его поверхностью. Она является функцией критерия Архимеда и определяется уравнением [77]:
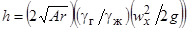 (80)
(80)
и
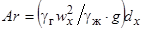 (81)
(81)
Таким образом:
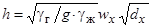 (82)
(82)
где wx – скорость газа на оси потока при его встрече с поверхностью металла;
gг и gж – плотности газа и металла;
dх– диаметр струи при встрече ее с жидкостью.
В последние годы некоторые исследователи для определения геометрических размеров "открытой" реакционной зоны вывели ряд уравнений. Для Ar>10 [72, 73] справедливы формулы:
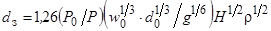 (83)
(83)
и
hз=(P0/P)w0 d0b1/2/g1/2 H1/2, (84)
где P0 и P – давления дутья при выходе из сопла и в нижней точке реакционной зоны (на глубине ее h3);
w0 и d0 – скорость истечения газа из сопла и диаметр сопла;
H – расстояние от среза сопла до спокойной поверхности металлической ванны;
b – параметр, характеризующий изменение осевой скорости струи;
b=(wx/w0)×(H/d0) (85)
Следует отметить, что при продувке ванны открытой струёй, последняя оказывает эжектирующее влияние на окружающий ее газ и с металлом контактирует не технический кислород, а его смесь с окружающими струю азотом и продуктами горения топлива, образующими печную атмосферу.
В современных кислородных конверторах продувка ванны сверхзвуковыми кислородными струями приводит к резкому увеличению скорости окисления углерода, в результате чего почти вся плавка протекает при условиях заглубленной газовой струи в толщу вспененной металло-шлаковой эмульсии.
Размеры реакционной зоны при продувке сверху приближенно определяются с помощью полуэмпирических уравнений [72] для глубины ее:
hmax/d=2,1( 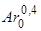 /1+Hф/60d) (86)
/1+Hф/60d) (86)
и максимального диаметра зоны:
D3max=3,3(1/rм g)0,49 (87)
С помощью "горячего" моделирования установлено, что при продувке металла кислородом образуются:
1) "первичная" реакционная зона, представляющая собой область взвеси в окислительной газовой среде мельчайших металлических капель, которые окисляются на лету и своим окислением определяют высокую температуру этой области, порядка 2000-2500°С;
2) "вторичная" реакционная зона, представляющая собой область раздробленного, интенсивно перемешиваемого, "вспененного” газами металла. Через толщу этого металла интенсивно прорываются из объема первичной реакционной зоны пузырьки еще не ассимилированного металлом кислорода, оксида углерода, образующейся при контактировании кислорода с углеродсодержащим металлом. Температура во вторичной реакционной зоне на протяжении всей продувки изменяется по направлению от первичной реакционной зоны от типичных для нее значений (2000-2500 °С) до величин, характерных для всего объема металла в конвертере (1400-1650 °С).
Хотя строгих границ, между обеими рассматриваемыми зонами (см. рис. 20) не существует, их приходится условно разграничивать по причине резкого различия протекающих в обеих зонах физико-химических процессов.
В «первичной зоне» металл, взвешенный в газовой фазе в виде капель и находящийся на разрыхленной поверхности зоны контакта с газами, интенсивно поглощает кислород. При этом окисляются все примеси металла и само железо. Часть капель, в особенности мелких, за период их витания в кислороде успевает полностью окислиться и сгореть. Часть капель, преимущественно крупных, успевает не окислившись еще полностью слиться с образующим реакционную зону и окружающим ее металлом. Однако и эти капли активно участвуют в поглощении и ассимиляции металлом кислорода. Вследствие окисления железа и шлакообразующих компонентов металлического расплава на поверхности этих капель всегда существует слой железистого шлака, кроме того, в этом уже сильно обезуглероженном и перегретом (до 2000¸2500°С) металле растворяется большое количество
 |
кислорода.
Его можно приближенно оценить по уравнению [78]:
lg[O]/a(FeO)=–(6320/T)+2,734 (88)
Оно составляет порядка 2-3 % - в зависимости от активности (FеО) в контактирующем с металлом "первичном" шлаке.
Таким образом, «первичная» реакционная зона снабжает окружающую ее «вторичную зону» кислородом в форме пузырьков еще не полностью ассимилированного кислорода, пузырьков оксида углерода, высокожелезистых "первичных" шлаков и растворенного в металле кислорода. Высокие температуры первичной реакционной зоны весьма благоприятствуют интенсивному растворению извести в образующихся в этой зоне "первичных" шлаках. Хотя в эту зону лишь случайно попадают отдельные кусочки извести, этот процесс, как показывают опыты с применением пульсирующего кислородного дутья, имеет весьма большое значение [77]. В отдельных участках реакционной зоны формируются небольшие объемы шлака, уже ассимилировавшие некоторое количество оксида кальция. В этих объемах процесс шлакообразования продолжается и тогда, когда они выносятся из первичной реакционной зоны образующимися в ней турбулентными потоками в окружающие, более холодные участки конвертерной ванны.
Таким образом, в «первичной» реакционной зоне преимущественное развитие получают реакции непосредственного окисления примесей металла за счет их прямого контакта с кислородом. Во вторичной реакционной зоне преобладают реакции "двухстадийного" окисления за счет образовавшихся оксидов железа и оксидов примесей металла в «первичной» реакционной зоне.
Глава 3.
“Экстракционное“ рафинирование металла
Общие положения
Под экстракционным рафинированием металла, по аналогии с некоторыми процессами химической технологии, следует понимать очищение его от примесей, вредных для его эксплуатационных свойств, путем их перехода в другие, контактирующие с металлом фазы под действием "закона распределения". Такое распределение примеси между контактирующими фазами происходит, строго говоря, без изменения форм существования рассматриваемой примеси при переходе ее из одной фазы в другую, а ее концентрации в обеих фазах связаны между собой условиями равенства ее химического потенциала во всех контактирующих фазах:
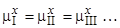 , (89)
, (89)
где верхний индекс обозначает рассматриваемый (экстрагируемый) элемент, а нижний – условный номер контактирующей фазы.
Процесс экстрагирования рассматриваемой примеси полностью прекращается, когда выравниваются химические потенциалы примеси "х" во всех контактирующих фазах и когда, например, не имеет места постепенное увеличение массы той или иной из фаз. Если химический потенциал какого-либо элемента (примеси) "х", находящегося в чистом виде составляет 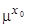 , то в рафинируемой фазе например в металле, он составит:
, то в рафинируемой фазе например в металле, он составит:
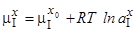 (90)
(90)
где 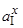 – активность элемента “х” в металлической фазе, вычисленная при условии, что за единицу активности принят этот элемент “х”, находящийся в насыщении в металле (в фазе 1).
– активность элемента “х” в металлической фазе, вычисленная при условии, что за единицу активности принят этот элемент “х”, находящийся в насыщении в металле (в фазе 1).
Равновесие наступает при условии, когда 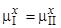 т.e. при:
т.e. при:
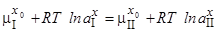 (91)
(91)
и тогда массообмен между фазами I и II прекращается. В чистом виде такой процесс в металлургии стали почти не встречается. Он наблюдается при распределении растворимых газов между двумя полностью несмешивающимися металлами – например, водорода между железом и свинцом.
Почти во всех типичных для металлургии стали случаях имеет место не просто переход той или иной примеси из металла в контактирующую с ним фазу, но и одновременное химическое взаимодействие этой примеси с компонентами контактирующей с металлом среды, извлекающей примесь. В результате даже в таком, казалось бы простейшем случае, как экстрагирование из металла азота или водорода в газовую фазу мы имеет дело с таким энергоемким процессом как молизация этих газов и, следовательно, здесь имеет место не просто их распределение в соответствии с законом выравнивания их химических потенциалов.
С учетом всего сказанного выше и, принимая во внимание определенную неточность применяемых терминов о распределении тех или иных примесей, например, между металлом и шлаком, мы в дальнейшем под "экстракционным рафинированием металла" будем подразумевать вообще удаление из него примесей в другую, извлекающую фазу вне зависимости от того, какие при этом та или иная примесь претерпевает химические или аллотропические превращения, или другие "изменения формы существования". В каждом конкретном случае задача металлурга состоит в детальном изучении природы процесса рафинирования, т.е. его термодинамики и кинетики, а также влияния на них различных побочных факторов.
Безусловно, под такое понимание экстракционного рафинирования подпадает и окислительное рафинирование металла. Однако, технологический период плавки, на продолжении которого происходит окисление примесей металла, создаваемые для этого условия хода плавки и используемые технические средства настолько специфичны, что эти процессы удобней рассматривать отдельно как "окислительное рафинирование" со всеми его особыми проблемами и закономерностями.
Основной задачей экстракционного рафинирования является удаление из металла таких вредных для его свойств примесей как сера, кислород, водород, азот и неметаллических включений, образуемых некоторыми из этих элементов с расплавленным железом и другими компонентами сплава. По самой сути процесса задача экстракционного удаления того или иного элемента состоит в возможно более полном его извлечении из металла. В дальнейшем теория этого вида рафинирования будет рассматриваться именно под этим углом зрения.
Однако на практике далеко не всегда полное удаление даже "вредной" примеси является оптимальным для служебных свойств металла. Металл всегда представляет собой гетерогенную систему фаз и влияние той или иной примеси на сам металл (растворитель) и на взвешенные в нем неметаллические диспергированные фазы может быть различным и часто недостаточно изученным. Кроме того, те технологические мероприятия, которые положительно влияют на процесс извлечения той или иной вредной примеси, могут оказаться далеко не полезными для природы самого металлического расплава, для тех или иных его компонентов и для его макро- и микронеоднородности и служебных качеств готовых изделий.
Для изучения процесса экстракционного рафинирования и нахождения наиболее благоприятных для него условий необходимо знать химический состав и физическую природу как металлической (рафинируемой), так и экстрагирующей, т.е. извлекающей примеси, фазы. Особое значение имеет наличие в последней компонентов, имеющих химическое сродство к извлекаемой из металла примеси, т.е. компонентов, понижающих ее активность и химический потенциал. С другой стороны, поскольку одним из звеньев экстракционного рафинирования всегда является массоперенос экстрагируемой примеси, принявшей ту или иную форму в экстрагирующей фазе, кинетика рафинирования в большой степени зависит от вязкости фазы, извлекающая примесь, интенсивности перемешивания, степени гомогенности и т.д. Во многих случаях процесс извлечения примесей экстрагирующей фазой определяется размерами удельной поверхности контакта металла и фазы, извлекающей примеси, условиями смачивания, т.е. адгезией обоих фаз друг к другу и изменением адсорбционной способности контактирующих фаз при изменении их состава или температуры.
В общем случае процесс экстракционного рафинирования металла складывается из следующих этапов:
1. Массоперенос примеси внутри очищаемого металла.
2. Адсорбционно-кинетическое звено, имевшее место на поверхности контакта металла и извлекающей фазы – чаще всего сопровождающееся формированием практически нерастворимых или малораcтворимых в металле химических соединений удаляемой примеси.
Дата добавления: 2016-11-26; просмотров: 1902;











