Количество вещества. Единица количества вещества.
Под количеством вещества (ν) понимают определенное число структурных единиц этого вещества. За единицу количества вещества принят 1 моль.
1 моль- количество вещества, содержащее столько же структурных единиц (атомов, молекул или других частиц), сколько их содержится в 12 г (0,012 кг) изотопа углерода 12С.
Т.к. масса 12С равна 1,993·10-23 г, то в 12 г углерода 12С содержится N = 12г/1,993·10-23 г = 6,02·1023 атомов.
Поэтому можно дать следующее определение моля:
Моль- это такое количество вещества, в котором, независимо от агрегатного состояния, содержится 6,02·1023 структурных единиц вещества.
Говоря о количестве вещества, всегда надо точно знать, из каких структурных единиц состоит вещество. Например:
· 1 моль железа – это 6,02•1023 атомов Fe, т.к. железо состоит из атомов.
· 1 моль воды – это 6,02•1023 молекул H2O, т.к. вода состоит из молекул.
· 1 моль хлорида натрия - это 6,02•1023 условных молекул NaCl (хлорид натрия состоит из ионов).
· 1 моль CuSO4•5H2O - это 6,02•1023 структурных единиц, каждая из которых состоит из одной условной молекулы CuSO4 и пяти молекул H2O.
Число 6,02•1023 называется постоянной Авогадро и обозначается NA.
Таким образом, NA указывает число структурных единиц в одном моле вещества:
NA = 6,02•1023 моль-1
Отсюда следует, что:
· если известно число структурных единиц (N), то количество вещества определяется по формуле:
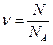
· если известно количество вещества (ν), то число структурных единиц определяется по формуле:
N = ν • NA
Следует различать понятия «моль вещества», «моль химического элемента», «моль ионов».
Моль химического элемента – это 6,02•1023 атомов данного химического элемента.
Понятие «моль вещества» и «моль химического элемента» совпадают лишь для веществ, имеющих атомную или металлическую структуру. Например, моль вещества Fe и моль химического элемента Fe – это одно и то же. В обоих случаях это 6,02•1023 атомов железа.
Моль вещества содержит столько молей каждого химического элемента, сколько атомов этого элемента содержится в одной молекуле вещества.
Например, 1 молекула С2Н6 содержит 2 атома С и 6 атомов Н; 6,02•1023 молекул С2Н6 содержат 2•6,02•1023 атомов С и 6•6,02•1023 атомов Н или 1 моль С2Н6 содержит 2 моль атомов С и 6 моль атомов Н.
Моль ионов– это 6,02•1023 ионов данного вида.
Моль вещества содержит столько молей ионов каждого вида, сколько ионов этого вида образуется при диссоциации одной условной молекулы вещества.
Например, из одной молекулы Na2SO4 при диссоциации образуется 2 иона Na+ и 1 ион SO42-:
Na2SO4→ 2 Na+ + SO42-
При диссоциации 6,02•1023 молекул Na2SO4 образуется 2•6,02•1023 ионов Na+ и 6,02•1023 ионов SO42- , следовательно, 1 моль Na2SO4 содержит 2 моль ионов Na+ и 1 моль ионов SO42-.
Понятие моль относится не только к атомам, молекулам или ионам, но и к любым другим частицам. Например, 1 моль электронов – это 6,02•1023 электронов.
Дата добавления: 2016-11-26; просмотров: 4735;











