Изотерма поверхностного натяжения. Поверхностная активность
Из адсорбционного уравнения Гиббса видно, что влияние природы вещества на адсорбцию заключено в величине и знаке производной 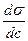 . Предельное значение этой производной при с→0, взятой со знаком минус, называют поверхностной активностью (g):
. Предельное значение этой производной при с→0, взятой со знаком минус, называют поверхностной активностью (g):
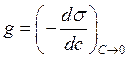 (8)
(8)
Поверхностная активность является важнейшей адсорбционной характеристикой веществ, определяющей многие их свойства и области применения. Уравнение (8) показывает, что чем сильнее уменьшается поверхностное натяжение с ростом концентрации, тем больше поверхностная активность. Величина и знак поверхностной активности зависят как от природы самого вещества, так и от природы растворителя и адсорбента.
Вопрос 5. Понятие о поверхностно-активных и неактивных веществах. Правило Дюкло-Траубе.
Все вещества по способности адсорбироваться на границе раздела фаз делятся на три группы:
Группа 1.
Поверхностно-активные вещества (ПАВ). Для таких веществ g>0, 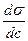 <0, Г>0. Поверхностно-активные вещества способны накапливаться в поверхностном слое, т.е. способны самопроизвольно переходить из объема фазы на границу раздела. Для этого необходимо, что бы данные вещества отвечали следующим требованиям:
<0, Г>0. Поверхностно-активные вещества способны накапливаться в поверхностном слое, т.е. способны самопроизвольно переходить из объема фазы на границу раздела. Для этого необходимо, что бы данные вещества отвечали следующим требованиям:
1) обладали малой растворимостью и не могли уходить в глубь раствора;
2) поверхностное натяжение самого поверхностно-активного веществ меньше, чем поверхностное натяжение чистого растворителя σо, то есть σПАВ< σо. Последнее условие необходимо для того, чтобы замена молекул растворителя в поверхностном слое на молекулы ПАВ была энергетически выгодной.
Таким условием соответствуют вещества дифильного строения, то есть состоящие из двух разных частей. Молекулы ПАВ имеют неполярную (углеводородную часть) и полярную, представленную функциональными группами –СООН, –NH2, –OH, –NO2 и др. Части молекул ПАВ, оказываются родственными обеим контактирующим фазам. Углеводородные гидрофобные радикалы обеспечивают малую растворимость молекул и выталкиваются из воды на поверхность. Поверхностное натяжение органических кислот, аминов, спиртов и т.д. всегда в несколько раз ниже, чем у воды.
Группа 2.
Поверхностно-инактивные вещества (ПИВ). Эти вещества повышают поверхностное натяжение раствора с увеличением концентрации. Для них g<0; 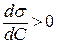 ; Г<0. Для ПИВ характерно стремление уйти с поверхности в объем раствора, а для этого они должны обладать следующим условиями:
; Г<0. Для ПИВ характерно стремление уйти с поверхности в объем раствора, а для этого они должны обладать следующим условиями:
1) иметь хорошую растворимость;
2) поверхность натяжение вещества должно быть больше, чем у чистого растворителя.
Хорошая растворимость обеспечивает переход молекул в глубь раствора, а большее значение поверхностного натяжения способствует замену молекул ПИВ в поверхностном слое на молекулы растворителя. Отрицательная адсорбция для вещества эквивалентна положительной для растворителя. Таким условиям отвечают неорганические основания, кислоты, соли в водных растворах, характеризующиеся сильным взаимодействием с молекулами растворителя.
Группа 3.
Поверхностно-неактивные вещества (ПНВ). Для этой группы веществ g=0, 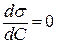 , Г=0. Эти вещества равномерно распределяются между объемом фазы и поверхностным слоем.
, Г=0. Эти вещества равномерно распределяются между объемом фазы и поверхностным слоем.
Представим на рисунке 4 (а, б) зависимости поверхностного натяжения и адсорбции для трех видов веществ.
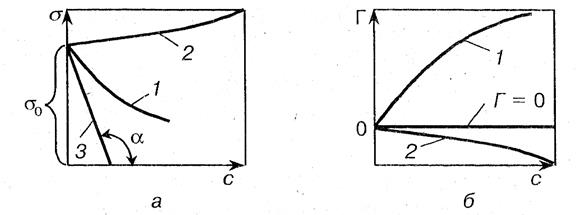
Рис 4 (а, б) Влияние растворенных веществ на поверхностное натяжение воды: 1 – раствор поверхностно-инактивного вещества; 2 – раствор полярного органического вещества; 3 – раствор мицеллообразующего поверхностно-активного вещества
Графически поверхностная активность, согласно уравнению (8) определяется как наклон касательной, проведенной к кривой σ=f(c) в точке пересечения её с осью ординат. Для точки А g=tgα.
Правило Дюкло-Траубе. Строение адсорбционных слоев
При экспериментальном изучении адсорбции на границе жидкость-газ Дюкло-Траубе установили следующую закономерность: Поверхностная активность в гомологическом ряду жирных кислот, аминов, спиртов возрастает в 3-3,5 раза при переходе к каждому следующему гомологу:
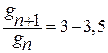 (9)
(9)
Можно дать следующее качественное обоснование правилу Дюкло и Траубе: при удлинении углеводородной цепи в молекуле ПАВ возрастает её гидрофобная часть, то есть снижается её растворимость в полярных растворителях. Это приводит к увеличению стремления молекул переходить из объема раствора на поверхность раздела фаз.
|
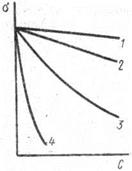
Рис 5 Изотермы σ = f(с) для ряда водных растворов предельных жирных кислот в системе жидкость воздух: 1 – муравьиная; 2 – уксусная;
3 – пропионовая; 4 – масляная.
Вопрос 6. Ориентация молекул в поверхностном слое.
Понятие о липосомах. Структура биологических мембран
Существование минимального значения поверхностного натяжения у растворов ПАВ и предельного значения адсорбции (Г∞) позволили И.Ленгмюру высказать предположение об ориентации адсорбированных молекул в поверхностном слое. Молекулы ПАВ состоят из двух частей: полярной (гидрофильной) и неполярной (гидрофобной). При адсорбции полярная группа, обладающая большим сродством к полярной фазе (например, к воде) втягивается в неё. В то же время неполярная группа выталкивается в неполярную фазу.
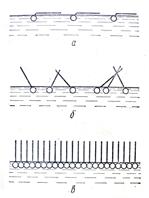
Рис 7 Образование поверхностных слоев
При малых концентрациях ПАВ углеводородные радикалы «лежат» на поверхности полярной жидкости, а полярные группы погружены в нее.
С увеличением концентрации ПАВ в растворе число молекул, находящихся в поверхностном слое, возрастает. Это приводит в пределе к образованию на граничной поверхности насыщенного мономолекулярного адсорбционного слоя, в котором молекулы ПАВ предельно ориентированы. Этот случай образно называют молекулярным частоколом Ленгмюра. Существование мономолекулярного насыщенного слоя хорошо объясняет постоянство предельной адсорбции Г∞ у органических веществ одного и того же гомологического ряда.
Используя представления Ленгмюра о строении поверхностного слоя, можно рассчитать размеры молекул ПАВ в насыщенном адсорбционном слое. Очевидно, что предельная адсорбция (Г∞) численно равна избыточному количеству ПАВ (моль), приходящемуся на единицу поверхности раздела (м2). Произведение предельной адсорбции на постоянную Авогадро (Г∞NA) определяет число молекул, которое занимает единицу площади. Из этого следует, что площадь поперечного сечения молекулы ПАВ в насыщенном слое можно рассчитать по уравнению:
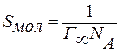 (10)
(10)
Произведение предельной адсорбции Г∞ на молярную массу ПАВ (М) равно массе ПАВ (m), приходящейся на единицу поверхности насыщенного адсорбционного слоя:
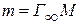 (11)
(11)
Тогда длина молекулы ПАВ в насыщенном адсорбционном слое, равная толщине этого слоя, может быть найдена с помощью уравнения:
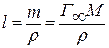 (12)
(12)
где ρ – плотность ПАВ, кг/м3; Г∞ – предельная адсорбция, моль/м2; М – молярная масса, кг/моль.
Представления об ориентации молекул ПАВ в насыщенном адсорбционном слое сыграл большую роль в развитии учения о структуре биологических мембран.
Е.Горшнер и Г.Грендел (1925) в опытах с липидами, экстрагированными из мембран эритроцитов, установили, что площадь образованного ими мономолекулярного слоя практически вдвое больше суммарной поверхности самих эритроцитов.
Этот факт позволил Ф.Даниэли и Г.Давсону (1931-1933) предложить первую общепринятую модель биологической мембраны. Согласно этой модели основным элементом мембранных структур клетки является бимолекулярный слой из молекул липидов, полярные группировки которых направлены наружу, а неполярные углеводородные радикалы – внутрь.
Полярные группы взаимодействуют с белками. Даниэли и Давсон предполагали, что белки образуют симметричные мономолекулярные слои на внешней и внутренней стороне липидного бислоя.
Позднее было установлено ассиметричное распределение белков в клеточных мембранах. Среди мембранных белков имеются такие, которые способны взаимодействовать с гидрофобными радикалами и проникать в глубь мембраны (интегральные белки). Так как часть поверхности мембраны свободна от белков (у эритроцитов около 30%, у микросомальных мембран около 20%), в настоящее время наиболее принятой является мозаичная модель мембраны. Макромолекулы интегральных белков, пронизывающих мембрану, могут образовывать поры – ионные каналы, которые обладают избирательной проницаемостью для различных ионов.
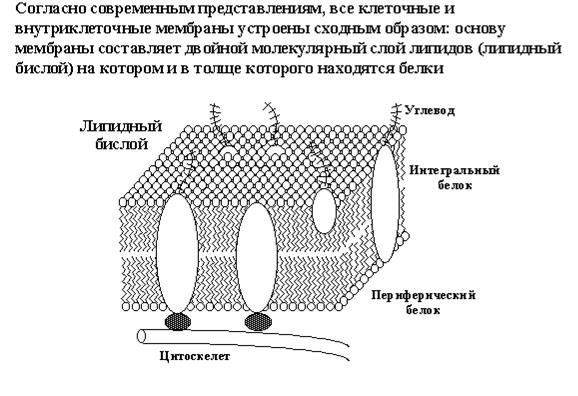
Рис 8 Общая схема строения мембран
Во всех живых клетках биологические мембрану выполняют функцию барьера, отделяющего клетку от окружающей среды, и разделяющего внутренний объем клетки на сравнительно изолированные "отсеки" (compartments). Сами по себе перегородки, разделяющие клетки на отсеки, построены из двойного слоя липидных молекул (называемого часто липидным бислоем) и практически непроницаемы для ионов и полярных молекул, растворимых в воде. Но в этот липидный бислой встроены многочисленные белковые молекулы и молекулярные комплексы, одни из которых обладают свойствами селективных (т. е. избирательных) каналов для ионов и молекул, а другие - насосов, способных активно перекачивать ионы через мембрану.
Дата добавления: 2016-11-04; просмотров: 8680;











