СТЕАРИНОВАЯ КИСЛОТА
При изучении высших кислот учащиеся подробно знакомятся со свойствами бытового химического продукта — мыла и впервые на практике встречаются с веществом, обладающим двойственной функцией, — олеиновой (непредельной) кислотой.
Свойства стеариновой кислоты. Стеариновая кислота в воде нерастворима, поэтому для опытов, иллюстрирующих ее кислотные свойства, нельзя, как обычно, воспользоваться водным раствором.
а) Расплавляют немного стеарина или стеариновой свечи в фарфоровой чашке и помещают в него небольшой кусочек натрия. Наблюдается выделение газа — водорода:
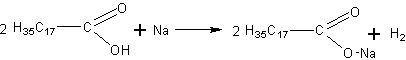
б) В пробирке растворяют кусочек стеарина в органическом растворителе (эфир, хлороформ, бензол) и к полученному раствору добавляют 2 капли спиртового раствора фенолфталеина. Затем вносят 1—2 капли разбавленного раствора гидроксида натрия и встряхивают пробирку. Розовой окраски раствора не наблюдается, так как стеариновая кислота нейтрализовала щелочь:
С17Н35СООН + NaOH à C17H35COONa + Н2О
При дальнейшем прибавлении щелочи к раствору кислоты розовая окраска появляется после того, как кислота будет нейтрализована.
Добавляя щелочь к эфиру с фенолфталеином без стеариновой кислоты, наблюдают моментальное появление окраски.
в) В пробирку со спиртом добавляют 2—3 капли щелочи и 1-2 капли фенолфталеина и к полученной смеси при перемешивании прибавляют эфирный раствор стеариновой кислоты или даже твердый стеарин. При этом происходит обесцвечивание раствора вследствие нейтрализации щелочи.
Стеариновая кислота — кислота слабая. О силе стеариновой кислоты можно судить по гидролизу ее солей, например стеарата натрия C17H35COONa.
а) Растворяют в воде тонкие стружки простого мыла и добавляют спиртовой раствор фенолфталеина. Появление розовой окраски говорит о том, что стеариновая кислота — кислота слабая. Параллельно может быть испытан фенолфталеином водный раствор ацетата натрия. В этом случае розовая окраска если и появляется, то очень слабая, так как уксусная кислота сильнее стеариновой.
б) В цилиндр до половины наливают воду, а затем по стенке осторожно прибавляют небольшое количество спиртового раствора мыла с фенолфталеином. В спиртовом растворе гидролиз соли не происходит и розовая окраска не наблюдается. На границе же соприкосновения спиртового раствора соли с водой появляется розовое кольцо.
Получение мыла (стеарата натрия) из стеарина. Один из современных способов получения мыла состоит в нейтрализации кислот, получаемых окислением синтетических углеводородов или же непосредственным синтезом из водяного газа.
Кусочек стеарина (стеариновой кислоты) нагревают в химическом стаканчике с водой, пока стеарин не расплавится (темп. пл. 69°С), и приливают к нему понемногу раствор гидроксида натрия до полного растворения (стеарат натрия растворяется в воде). К полученному раствору прибавляют поваренную соль до насыщения.
В насыщенном растворе поваренной соли стеарат натрия не растворяется и всплывает наверх в виде хлопьев.
Получение стеариновой кислоты из мыла. Стеариновая кислота, как кислота слабая, может быть получена действием минеральной кислоты на мыло:
2C17H35COONa + H2SO4 à 2C17H35COOH + Na2SO4
Как вещество не растворимое в воде, стеариновая кислота при этом выделяется из раствора.
В химическом стаканчике при нагревании готовят крепкий раствор мыла в воде. Для более быстрого растворения мыло должно быть предварительно нарезано в виде тонких стружек. Продолжая нагревать раствор мыла, прибавляют к нему раствор серной кислоты до выделения стеариновой кислоты. При охлаждении раствора 1 сверху образуется твердый слой стеариновой кислоты.
Таким способом в случае необходимости можно получить некоторое количество кислоты для классных занятий.
Моющее действие мыла. Мыло обладает свойством эмульгировать жиры и суспензировать твердые частички грязи.
а) Готовят, как было указано выше, раствор мыла в воде и прибавляют к нему 1 мл растительного масла. Смесь сильно взбалтывают до образования эмульсии, похожей на молоко. В другой пробирке подобным способом получают эмульсию из таких же количеств чистой воды и масла. Хотя во второй пробирке эмульсия была получена позднее, она быстро расслаивается на воду и масло. В первой же пробирке эмульсия оказывается устойчивой и не разделяется в течение всего урока.
б) В двух разных пробирках готовят суспензию сажи в воде и в мыльном растворе. Фильтруют растворы одновременно через бумажные фильтры. В первом случае фильтруется чистая вода, во втором случае мыльный раствор настолько сильно удерживает сажу, что суспензия, не разделяясь, проходит через фильтр.
Моющее действие мыла проявится еще более ярко, если фильтр с осадком сажи перевернуть на другую сторону, снова вложить в воронку и сперва пропустить через него воду, а затем мыльный раствор. Вода проходит прозрачной и не смывает сажу, мыльный же раствор совершенно очищает фильтр от сажи, становясь черным.
Действие жесткой воды на мыло. В жесткой воде мыло не дает пены и плохо мылит, так как превращается в нерастворимые в воде соли:
2C17H35COONa + СаСI2 à (C17H35COO)2Ca + 2NaCl
Хлопья нерастворимого мыла можно часто наблюдать при получении мыльного раствора в домашних условиях.
а) Раствор мыла в воде разливают в две пробирки. В одну из пробирок добавляют небольшое количество раствора хлорида кальция СаСI2. При встряхивании пробирок в одной из них наблюдают образование пены, в другой — отсутствие пены и образование осадка соли кальция.
б) В один цилиндр наливают около 50 мл дистиллированной воды, в другой такой же цилиндр — 50 мл водопроводной воды (если водопроводная вода очень «мягкая», в нее добавляют немного
раствора хлорида кальция). В оба цилиндра приливают по 1 мл спиртового раствора мыла и встряхивают. В первом случае образуется устойчивая пена. Во втором пены нет, но образуется осадок нерастворимой соли. Во второй цилиндр продолжают добавлять раствор мыла до тех пор, пока при встряхивании не будет получаться неисчезающая пена. По количеству затраченного раствора мыла можно приблизительно судить о степени жесткости воды.
Опыт показывает, что при пользовании жесткой водой большое количество мыла расходуется на осаждение кальциевых (и магниевых) солей и что только после их осаждения мыло, как поверхностно-активное вещество (ПАВ) начинает выполнять свою основную функцию — давать пену. Чтобы сделать воду «мягкой» и не расходовать мыло нерационально, соли кальция, как известно, осаждают предварительно кипячением или с помощью специальных добавок, например соды.
Дата добавления: 2018-11-26; просмотров: 1703;











