Модель атома Резерфорда
Важнейшим шагом вперед явилась попытка непосредственного опытного зондирования внутренних областей атома с целью установления пространственного распределения зарядов в атоме. Такое зондирование осуществил Резерфорд с помощью α – частиц, наблюдая изменение направления их полета (рассеяние) при прохождении через тонкие слои вещества.
Опыты Резерфорда показали, что наряду со случаями отклонения α – частиц в основном на малые углы происходят столкновения, вызывающие отклонения на углы вплоть до 180˚. Проанализировав результаты опыта, Резерфорд пришел к выводу, что столь сильное отклонение α – частиц возможно только в случае, если внутри атома имеется чрезвычайно сильное электрическое поле. Это поле создается зарядом, связанным с большой массой и сконцентрированным в очень маленьком объеме.
Основываясь на этом выводе, Резерфорд предложил в 1911 г. ядерную модель атома: атом представляет собой систему зарядов, в центре которой расположено тяжелое положительное ядро с зарядом Ze, имеющее размеры, не превышающие 10-14м. Вокруг ядра в области с линейными размерами порядка 10-10м расположены Z электронов, распределенных по всему объему, занимаемому атомом. Почти вся масса атома сосредоточены в ядре. Созданная Резерфордом модель напоминала строение солнечной системы, где вокруг массивного Солнца движутся сравнительно легкие планеты, поэтому такую модель строения атома назвали планетарной.
Итак, результаты опытов по рассеянию α – частиц свидетельствуют в пользу ядерной модели Резерфорда. Однако ядерная модель оказалась в противоречии с законами классической механики и электродинамики. Поскольку система неподвижных зарядов не может находиться в устойчивом состоянии – под действием кулоновских сил электроны сразу упали бы на ядро, Резерфорду пришлось отказаться от статической модели атома и предположить, что электроны движутся вокруг ядра, описывая искривленные траектории. Но в этом случае электрон будет двигаться с ускорением, непрерывно излучая электромагнитные волны, согласно классической электродинамике. Процесс излучения сопровождается потерей энергии, так что, в конечном счете, электрон должен упасть на ядро. Такая модель также не объясняла спектральных закономерностей. Электрон, приближаясь к ядру должен двигаться все быстрее, порождая все более короткие электромагнитные волны, в этом случае спектр излучения должен быть сплошным.
Недостатки модели: непрерывная потеря электроном энергии в виде излучения электромагнитных волн; неустойчивость атома; сплошной спектр излучения. В действительности: атом – устойчивая система; излучение имеет линейчатый спектр.
Для объяснения этих противоречий можно было выдвинуть два предположения: либо считать, что предложенная Резерфордом ядерная модель атома не соответствует действительности, либо считать, что законы классической физики имеют ограниченное значение и не могут применяться к движению таких маленьких частиц материи, как электрон.
Заменить ядерную модель атома другой моделью, которая соответствовала бы опытам Резерфорда и не противоречила бы классической физике, не удалось.
Постулаты Бора
Выход из затруднения был предложен Бором. Опираясь на идеи квантовой теории Планка, Бор предположил, что и в случае атома Резерфорда непрерывное излучение, требуемое классической электродинамикой, невозможно. Для истолкования линейчатых спектров Бор предположил, что излучение обладает частотой, определяемой из следующего условия
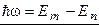 ,
,
где Em и En – энергии системы до и после излучения.
Исходя из этого закона, можно заключить, что спектры не дают нам картины движения частиц в атоме, как принимается в классической теории излучения, а позволяют судить лишь об изменениях энергии при различных возможных процессах в атоме. Дискретный характер спектральных линий свидетельствует о существовании определенных, дискретных значениях энергии, соответствующих особым состояниям атома. Эти состояния Бор назвал стационарными, ибо предположил, что атом может пребывать в каждом из них определенное время и, покидая его, снова попадает в другое стационарное состояние, изменяя свою энергию на конечную величину.
В 1913 г. Бор сформулировал два постулата:
1. Первый постулат (постулат стационарных состояний) - существуют стационарные состояния атома, находясь в которых он не излучает энергию. Этим стационарным состояниям соответствуют определенные (стационарные) орбиты, по которым движутся электроны.
Правило квантования орбит – из всех орбит электрона, возможных с точки зрения классической механики, осуществляются только те, для которых момент импульса равен величине, кратной постоянной Планка 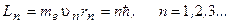 - целое число, m – масса электрона, υ– скорость электрона, r – радиус орбиты.
- целое число, m – масса электрона, υ– скорость электрона, r – радиус орбиты.
2. Второй постулат (правило частот) – при переходе атома из одного стационарного состояния в другое испускается или поглощается один фотон
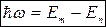 .
.
5. Атом водорода. Рассмотрим электрон, движущийся в поле атомного ядра с зарядом Ze. При Z = 1 такая система соответствует атому водорода, при иных Z – водородоподобному атому, т.е. иону, имеющему порядковый номер Z в таблице Менделеева и один электрон. Согласно закону Кулона между двумя точечными зарядами будет действовать сила
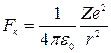
По закону динамики
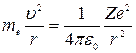 (*)
(*)
Используя правило квантования орбит( первый постулат) и исключая скорость, получим для радиусов допустимых орбит
 (**)
(**)
Радиус первой боровской орбиты атома водорода
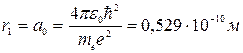
Внутренняя энергия атома складывается из кинетической энергии электрона (ядро неподвижно) и энергии взаимодействия электрона с ядром – потенциальной энергии а также используя (*) получим
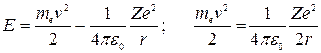
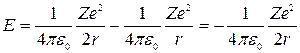
Подставив сюда выражение для радиуса орбиты (**), получим
 , (***)
, (***)
где n =1,2,3,… - номер орбиты.
Из формулы следует, что энергетические состояния атома водорода образуют последовательность энергетических уровней, изменяющихся в зависимости от числа n. Энергетическое состояние, соответствующее n = 1, называется основнымили невозбужденнымсостоянием. Все состояния с n >1 называются возбужденными.
При возрастании n энергетические уровни сближаются к границе, соответствующей n = ∞. При этом энергия электрона в атоме равна нулю. Знак минус в формуле показывает, что электрон связан в атоме силой притяжения к ядру. Абсолютное значение энергии является энергией связи электрона в атоме, находящимся в состоянии n. Значение энергии связи En = 0 соответствует ионизации атома, т.е. отрыву от него электрона. Для основного состояния энергия ионизации атома водорода, рассчитанная по формуле (***), равна 13,6 эВ.
При переходе атома водорода из состояния m в состояние n , m > n, излучается фотон, так как энергия Em > En по модулю
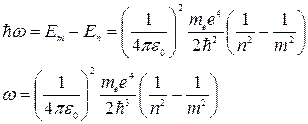
Переписав это соотношение для 1/λ, получим обобщенную формулу Бальмера
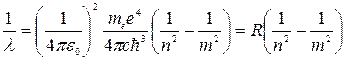 ,
,
Здесь постоянная Ридберга определяется подстановкой численных значений универсальных физических констант и поразительно совпадает с известным из опытов значением этой постоянной.
На рисунке приведена схема энергетических уровней атома водорода. Стрелками указаны переходы, соответствующие излучению различных спектральных серий.
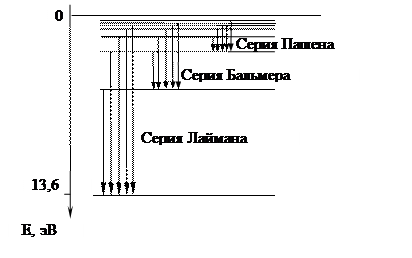
Постулаты Бора о существовании стационарных состояний атомов и правило частот нашли свое экспериментальное подтверждение в опытах Франка и Герца в 1913 г. В опытах изучались столкновения электронов с атомами. Первые опыты были поставлены на парах ртути. Электроны, встречающие на своем пути атомы ртути испытывали с ними соударения двух видов. При упругих столкновениях энергия электронов не изменялась, а изменялось лишь направление их движения. Это, хотя и затрудняло попадание электронов на анод, однако не могло служить причиной полного отсутствия анодного тока, который возрастал с увеличением разности потенциалов. При неупругих столкновениях электрон терял свою энергию, передавая ее атому ртути. В соответствии с постулатами Бора атом не может принять энергию в любом количестве, а лишь определенную порцию, переходя при этом в возбужденное состояние. Ближайшим к основному состоянию атома ртути является возбужденное состояние, отстоящее от основного по шкале энергий на 4,86 эВ. Таким образом, при напряжении 4,86 В должно происходить резкое падение анодного тока, что и наблюдалось в эксперименте. Аналогичная ситуация должна повторяться при напряжениях, кратных 4,86 эВ. Правило частот также подтвердилось на эксперименте. Ртутные пары переходя из возбужденного состояния в основное излучали ультрафиолетовые волны с длиной волны, соответствующей первой резонансной линии в спектре ртути.
Теория Бора сыграла важную роль в создании атомной физики. Особенно велика ее роль в развитии атомной спектроскопии, где огромный экспериментальный материал с помощью теории Бора был систематизирован и сведен к определенным полуэмпирическим закономерностям.
Однако наряду с определенными успехами в теории Бора с самого начала обнаружились существенные недостатки. Теория была внутренне противоречива. Основываясь на механическом соединении классической физики с квантовыми постулатами, теория Бора в ряде проблем привела к существенным трудностям. Наиболее серьезной неудачей в теории Бора явилась абсолютная невозможность с ее помощью создать теорию атома гелия, содержащего помимо ядра два электрона. Постепенно становилось очевидным, что теория Бора представляла собой лишь переходный этап на пути создания последовательной теории атомных и ядерных явлений. Такой последовательной теорией явилась квантовая (волновая) механика. Она объяснила не только многообразие явлений атомной и ядерной физики, но и физическое содержание самих постулатов Бора.
Вопросы для самоконтроля:
1. Каковы недостатки модели атома Резерфорда?
2. Какая серия спектральных линий относится к видимой области спектра? Лаймана? Бальмера? Пашена?
3. Каков смысл постулатов Бора?
4. Как с помощью постулатов Бора объясняется линейчатый спектр атома?
5. Какова суть опытов Франка и Герца?
6. В чем состоят недостатки теории Бора?
Лекция 4.
Дата добавления: 2020-12-11; просмотров: 546;











