Расход воздуха на горение
Зная химический состав газа, реакции полного горения и атомные массы горючих газов можно определить количество кислорода О2 для полного сгорания газа.
Например, для полного сгорания 1 кг водорода Н2 требуется 8 кг кислорода О2, при этом образуется 9 кг водяных паров H2O. Зная содержание в воздухе кислорода (21% по объему), можно определить теоретический объем воздуха, необходимый для полного сгорания 1 м3 газа.
На практике теоретический объем воздуха определяется по упрощенным формулам. Считают, что для полного сгорания 1 м3 газа на каждую 1000 Ккал его низшей теплоты сгорания Q 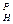 требуется 1,1 м3 воздуха:
требуется 1,1 м3 воздуха:
 Vо =1,1
Vо =1,1 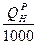 м3 в-ха/м3газа.
м3 в-ха/м3газа.
Например:
для сгорания 1 м3 метана требуется: Vо =1,1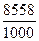
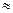 9,35 м3 в-ха/м3газа;
9,35 м3 в-ха/м3газа;
для сгорания 1 м3 пропана требуется:Vо =1,1 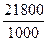
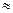 24 м3 в-ха/м3газа.
24 м3 в-ха/м3газа.
В действительности для полного сгорания топлива требуется несколько больше воздуха, чем теоретически необходимо. Это объясняется несовершенством перемешивания топлива с воздухом.
Отношение действительного объема воздуха к теоретически необходимому для полного сжигания топлива называется коэффициентом избытка воздуха.
a = 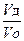
Действительный объем воздуха
Vд = aVo м3 в-ха/м3газа
Газ и воздух достаточно хорошо перемешиваются, поэтому при сжигании горючих газов коэффициент избытка воздуха сравнительно мал
a = 1,02…1,3.
Дата добавления: 2019-05-21; просмотров: 1145;











