Схема фазовых превращений однокомпонентных систем
Углеводородные газы, подобно всем индивидуальным веществам, изменяют свой объём при изменении давления и температуры.
На рис. 4.1 представлена диаграмма фазового состояния для чистого этана. Каждая из кривых соответствует фазовым изменениям при постоянной температуре и имеет три участка.
Справа от пунктирной линии отрезок соответствует газовой фазе, горизонтальный участок – двухфазной газожидкостной области, левый участок – жидкой фазе. Отрезок пунктирной линии вправо от максимума в точке С называется кривой точек конденсации (или точек росы), а влево от максимума – кривой точек парообразования (кипения).
В точке С пунктирной линии кривые парообразования и конденсации сливаются. Эта точка называется критической. Эта точка максимальной температуры (критической температуры,Ткр) и критического давления(Ркр), при которых газ и жидкость могут ещё сосуществовать в равновесии. Выше температуры, равной критической, газ ни каким повышением давления нельзя перевести в жидкое состояние.
С приближением температуры и давления к критическим значениям свойства газовой и жидкой фаз становятся одинаковыми, поверхности раздела между ними исчезают. Исчезают различия между физико-химическими свойствами жидкой и газообразной фазами. Свойства уравниваются, например плотности.
Следовательно, с приближением к критической точке по кривой начала кипения плотность жидкой фазы будет непрерывно убывать.
Если же к ней приближаться по линии точек конденсации, то плотность пара будет непрерывно возрастать.
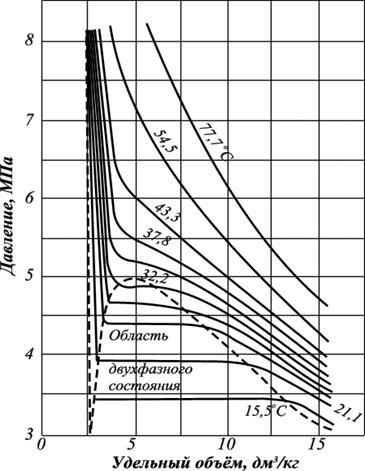
Рис. 4.1. Диаграмма фазового состояния чистого этана
Для индивидуальных углеводородов граничным давлением (при данной температуре) между жидкой и газовой фазой является давление упругости паров, при котором происходит конденсация или испарение.
Обе фазы (жидкость и пар) при данной температуре присутствуют в системе только в том случае, если давление равно упругости насыщенного пара над жидкостью. Давление, при котором газ начинает конденсироваться, называется давлением насыщениядля газа.
Фазовые превращения углеводородов можно также представить в координатах "давление–температура" (рис. 4.2).
Для однокомпонентной системы кривая давления насыщенного пара на графике давление–температура является одновременно кривой точек начала кипения и линией точек росы. При всех других давлениях и температурах вещество находится в однофазном состоянии.
Фазовая диаграмма индивидуальных углеводородов ограничивается критической точкой С (рис. 4.2). Для однокомпонентных систем эта точка определяется наивысшими значениями давления и температуры, при которых ещё могут существовать две фазы одновременно.

Рис. 4.2. Диаграмма фазового состояния этана в координатах Р–Т
Из анализа представленной зависимости (рис. 4.2) следует, что путём соответствующих изменений давления и температуры углеводороды можно перевести из парообразного состояния в жид-кость, минуя двухфазную область.
Газ, характеризующийся па-раметрами точки А (рис. 4.2), можно изобарически нагреть до температуры точки В, а затем, повысив давление в системе при постоянной температуре, перевести вещество в область точки D, расположенную выше критической точки С, и далее в область точки Е.
При этом свойства системы изменяются непрерывно и фазового разделения углеводорода на жидкую и паровую фазы не произойдёт. При дальнейшем охлаждении системы (от точки D до точки Е), а затем при снижении давления до точки F, вещество приобретёт свойства жидкости, минуя область двухфазного состояния.
Дата добавления: 2019-02-08; просмотров: 964;











