Энергетические характеристики адсорбции
Теплота адсорбции Q=-ΔH ΔH<0
Различают две энергетические характеристики процесса адсорбции –
интегральная теплота адсорбции – общее количество тепла, выделяющееся при адсорбции, отнесенное к единице массы адсорбента, равна убыли энтальпии при изменении адсорбции А от А1 до А2;
дифференциальная теплота адсорбции равна количеству теплоты, выделяющееся при адсорбции 1 моль адсорбата на бесконечно большой поверхности адсорбента (настолько большой, что адсорбция 1 моль не изменяет степени заполнения поверхности q).
Постоянство А – условие изостеричности процесса.
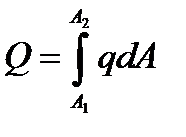

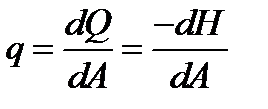 (2.37)
(2.37)
Обычно q уменьшается при адсорбции т.к. сначала насыщаются наиболее активные центры адсорбции.
 Величину Qad обычно измеряют в результате прямых экспериментов в калориметрах, значение же qst получают расчетным путем из изотерм адсорбции при различных температурах (в прямых экспериментах нельзя обеспечить условие q = const при адсорбции 1 моль – реальная поверхность не может быть бесконечно большой). Для этого на графике А= f(P) или Г = f(C) проводят ряд линий - изостер при А = const (линии параллельные оси абсцисс). Это видно из рис.2.13.
Величину Qad обычно измеряют в результате прямых экспериментов в калориметрах, значение же qst получают расчетным путем из изотерм адсорбции при различных температурах (в прямых экспериментах нельзя обеспечить условие q = const при адсорбции 1 моль – реальная поверхность не может быть бесконечно большой). Для этого на графике А= f(P) или Г = f(C) проводят ряд линий - изостер при А = const (линии параллельные оси абсцисс). Это видно из рис.2.13.
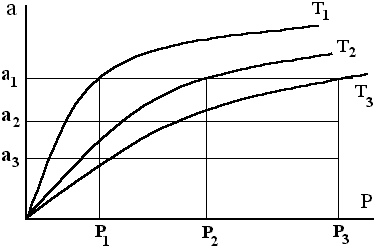
Рис. 2.13. Определение дифференциально – молярной изостерической теплоты адсорбции из изотерм адсорбции (Т3>T2.>T1).
Из точек пресечения изостер с изотермами для всех изотерм адсорбции определяют Р1, Р2, Р3 и т.д. (каждому значению Т соответствует своё значение Р).
На рис. 2.13 даны построения для изостеры А1. Полученные данные располагают в координатах lnP = f(1/Т) (рис.2.14). Дифферециально-молярную изостерическую теплоту адсорбции qst (на рисунке - для адсорбции А1) определяют из тангенса угла наклона полученной прямой qst = R×tga. Аналогично вычисляют дифференциальные теплоты и для других значений А.
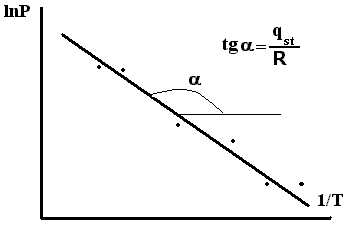
Рис.2.14. Графическое определение qst
Дата добавления: 2016-07-27; просмотров: 2938;











