Лиофильные коллоидные системы
К лиофильным системам относятся растворы коллоидных ПАВ. Для лиофильных систем характерно сильное межмолекуляр-ное взаимодействие дисперсной фазы и дисперсионной среды. Это приводит к образованию сольватных оболочек вокруг частиц дис-персной фазы и снижению их свободной поверхностной энергии. Поэтому они термодинамически устойчивы к слипанию частиц и характеризуются самопроизвольным диспергированием. В случаях когда дисперсионной средой служит вода, используют обычно термин «гидрофильные системы».
Растворы ПАВ обладают способностью к самоорганизации. При определенных условиях происходит самопроизвольная ассо-циация молекул с образованием мицелл − частиц характерного строения, состоящих из десятков дифильных молекул, имеющих достаточно длинные гидрофобные радикалы и полярные гидро-фильные группы (см. п. 2.1.1).
В случае полярного растворителя, в частности воды, ядро мицелл образуют гидрофобные радикалы, а гидрофильные группы ориентируются наружу в сторону дисперсионной среды (рис. 3.8). При этом гидрофильные концы молекул связаны с молекулами воды, образующими гидратную оболочку вокруг частиц. Такое строение мицелл определяет малую величину поверхностной энергии дисперсной системы (малое межфазное поверхностное натяжение), что и обеспечивает их агрегативную устойчивость. Частица обычно состоит из 50…100 молекул ПАВ. Образующаяся система полидисперсная, с определенным распределением по размерам частиц.
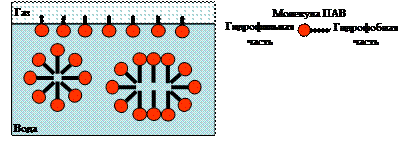 |
Рис. 3.8. Образование мицелл в водном растворе ПАВ
Мицеллы могут образовывать не все ПАВ, а только те, кото-рые имеют оптимальное соотношение гидрофильных и гидро-фобных свойств, определяемое эмпирической характеристикой – ГЛБ (гидрофильно-липофильный баланс). В частности, длина углеводородной цепи гидрофобного радикала должна быть достаточно велика – 10...18 атомов углерода. В неполярных дисперсионных средах образуются обратные мицеллы, в которых полярные группы объединяются в гидрофильное ядро, а углеводородные радикалы образуют олеофильную оболочку.
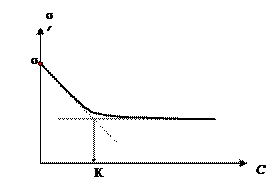 При малых концентрациях ПАВ присутствуют в растворе в молекулярной форме, образуя истинный раствор. Дифильные мо-лекулы сорбируются поверхностью растворителя, например воды (см. п. 2.1.1), величина поверхностного натяжения уменьшается с ростом их концентрации. При определенной величине концент-рации − критической концентрации мицеллообразования (ККМ) − вся поверхность растворителя будет занята молекулами ПАВ. Дальнейшее увеличение их количества в растворителе приводит к образованию мицелл. При этом концентрация ПАВ в мо-лекулярной форме остается неизменной. Соответственно величина поверхностного натяжения при концентрациях ПАВ, превышаю-щих ККМ, остается постоянной (рис. 3.9). На величину ККМ силь-но влияет длина углеводородной цепи молекулы ПАВ: ККМ умень-шается в 2…3 раза при увеличе-нии длины углеводородной цепи гидрофобного радикала на одну СН2- группу.
При малых концентрациях ПАВ присутствуют в растворе в молекулярной форме, образуя истинный раствор. Дифильные мо-лекулы сорбируются поверхностью растворителя, например воды (см. п. 2.1.1), величина поверхностного натяжения уменьшается с ростом их концентрации. При определенной величине концент-рации − критической концентрации мицеллообразования (ККМ) − вся поверхность растворителя будет занята молекулами ПАВ. Дальнейшее увеличение их количества в растворителе приводит к образованию мицелл. При этом концентрация ПАВ в мо-лекулярной форме остается неизменной. Соответственно величина поверхностного натяжения при концентрациях ПАВ, превышаю-щих ККМ, остается постоянной (рис. 3.9). На величину ККМ силь-но влияет длина углеводородной цепи молекулы ПАВ: ККМ умень-шается в 2…3 раза при увеличе-нии длины углеводородной цепи гидрофобного радикала на одну СН2- группу.
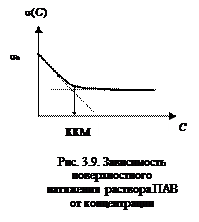
 В концентрационных зависимостях физико-химических свой-ств растворов ПАВ в точке ККМ наблюдаются резкие изменения. Например, при концентрациях боль-ших ККМ, возрастает светорассеяние, электропроводность ионогенных ПАВ остается неизменной.
В концентрационных зависимостях физико-химических свой-ств растворов ПАВ в точке ККМ наблюдаются резкие изменения. Например, при концентрациях боль-ших ККМ, возрастает светорассеяние, электропроводность ионогенных ПАВ остается неизменной.
Выше ККМ весь избыток ПАВ находится в виде мицелл.
В случае достаточно большой концентрации ПАВ происходит взаимодействие мицелл с образованием геля (структурированные жидкокристаллические системы).
Процесс изменения состояния ПАВ в зависимости от концен-трации обратим:
молекулярный раствор ↔ мицеллярный раствор ↔ связнодисперсная система
(золь) (гель)
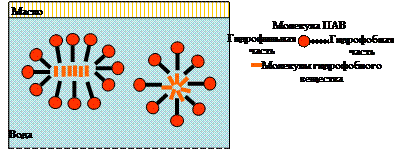
Для водных мицеллярных растворов ПАВ характерно раство-рение неполярных органических веществ, не растворимых (слабо-растворимых) в воде – солюбилизация (от латинского solubilis – растворимый). Она происходит в результате самопроизвольного проникновения молекул этих гидрофобных веществ в неполярное ядро мицеллы (рис. 3.10).
Необходимо отметить, что мицелярные растворы ПАВ (кон-центрация ПАВ больше ККМ) используют в качестве моющих средств, способных удалять гидрофобные загрязнения с различных поверхностей. ПАВ улучшают смачивание поверхностей, способствуют отрыву частиц загрязнений и стабилизации их в растворе. Образующаяся пена обеспечивает унос загрязнений.
Две несмешивающиеся жидкости (в простейшем случае вода и неполярная органическая жидкость) в присутствии мицелло-образующих ПАВ могут самопроизвольно образовывать микро-эмульсии – термодинамически устойчивые дисперсные системы в результате процесса, подобного солюбилизации. Дисперсная фаза состоит из капель, размер которых не превышает 100 нм. В зависимости от того, какая фаза непрерывная, а какая дисперсная, различают прямые и обратные микроэмульсии. Прямые − капли не
 |
полярной органической жидкости в воде, обратные − капли воды в неполярной органической жидкости.
Рис. 3.10. Солюбилизация
Обратные микроэмульсиии можно использовать для получе-ния твёрдых наночастиц (микрореакторы). Добавление в систему соответствующего реагента приводит к протеканию в каплях полярной фазы химических реакций с образованием нерастворимого вещества, размеры частиц которого будут ограничены размером капель.
Контрольные вопросы
1. Лиофобные золи. Структурная формула мицеллы.
2. Седиментационная и агрегативная устойчивость дисперсной системы.
3. Электрофорез.
4. Эффект Тиндаля.
5. Растворы ПАВ. Мицеллярные растворы ПАВ, солюбилизация.
Дата добавления: 2020-10-25; просмотров: 752;











