ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДЫ
КАЧЕСТВЕННЫЕ РЕАКЦИИ АЛИФАТИЧЕСКИХ УГЛЕВОДОРОДОВ
АЛКАНЫ
Алканы не окисляются перманганатом калия на холоде, вследствие этого раствор не будет изменять окраску. Предельные углеводороды в обычных условиях химически инертны: они не взаимодействуют с концентрированными серной и азотной кислотами, не окисляются сильными окислителями, такими как, перманганат калия, дихромат калия и др. Этим свойством алканов пользуются в фармации, когда необходимо открыть примеси, например, в вазелиновом масле:
1) при прибавлении к испытуемому маслу раствора перманганата калия в сернокислой среде при комнатной температуре розовая окраска не исчезает; или
2) при добавлении к испытуемому маслу бромной воды при комнатной температуре желто-бурая окраска не исчезает, то это служит признаком отсутствия в вазелиновом масле примесей.
Применение алканов в медицине.
-бутан (С4Н10) используют для заполнения аэрозольных упаковок лекарств;
- вазелин(С5Н12 – С25Н52) и парафин(С19 –С35) являются основой для мазей; - вазелиновое масло(С5Н12 – С15Н32)применяется в составе комбинированных лекарственных средств, как смягчающее средство; как мазевая основа.
- парафин применяются для лечения теплом при невралгиях, невритах, артритах, артрозах и т.д.
АЛКЕНЫ И АЛКИНЫ
Для непредельных связей характерны реакции электрофильного присоединения, такие реакции являются качественными для обнаружения двойных и тройных связей.
СН2 = СН2 + Вг2 ---> СН2 – СН2
| |
Вг Вг
этилен 1,2 -дибромэтан
Вг Вг
+ Вг2 | |
СН ≡ СН + Вг2 à СН=СН à СН - СН
| | | |
Вг Вг Вг Вг
ацетилен 1,2 -дибромэтилен 1,1,2,2- тетрабромэтан
Бурая окраска брома быстро исчезает, присоединение брома идет легко, при комнатной температуре.
При окислении алкенов раствором перманганата калия в нейтральной или слабощелочной среде происходит разрыв π - связи и присоединение гидроксильной группы к каждому атому углерода, т.е. реакция гидроксилирования. В результате получаются двухатомные спирты (гликоли). Эта реакция носит имя открывшего ее русского химика Е.Е.Вагнера (1888), она используется как качественная реакция для обнаружения двойной связи. В результате этой реакции окрашенный раствор перманганата калия быстро обесцвечивается и выпадает бурый осадок оксида марганца (IV).
3СН2=СН2 + 2КмпО4 +4Н2О -----> 3СН2 – СН2 +2КОН +2МпО2↓
| |
ОН ОН
этилен этандиол-1,2 (этиленгликоль)
Мп+7 +3е ----> Мп+4 2 окислитель
2С-2 - 2е ----> 2С- 3 восстановитель
Алкины легко окисляются различными окислителями, в частности перманганатом калия. При этом раствор перманганата калия обесцвечивается, что служит указанием на наличие тройной связи. Ацетилен окисляется раствором калия перманганата в нейтральной среде до щавелевой кислоты.
3С2Н2 + 8КмпО4 +4Н2О ---- > 3Н2С2О4 + 8МпО2 ↓+ 8КОН
ацетилен щавелевая
кислота
Мп+7 + 3е ---- Мп+4 8 окислитель
2С- - 8е ---- 2С+3 3 восстановитель
Реакция отличия алкинов, имеющих концевую тройную связь НС ≡, от алкенов и алканов – образование соли, называемые ацетиленидами. Ацетилениды серебра и меди (+1) легко образуются и выпадают в осадок при пропускании ацетилена через аммиачный раствор оксида серебра или хлорида меди (+1).
NH3
НС ≡ СН + Аg2О ----- > Аg - С º С - Аg ↓ + Н2О
ацетилен ацетиленид серебра
NH3
СН3- С º СН + СиС1 -----> СН3- С º С - Си + НС1
пропин метилацетиленид меди (+1)
Ацетилениды серебра и меди как соли очень слабых кислот легко разлагаются при действии сильной минеральной кислоты с выделением исходного алкина.
Из алкенов получают полимерные массы, из которых в производстве изготавливают медицинскую технику, вспомогательный материал (шприцы, системы для переливания крови, шовный материал и т.д.), полимерные пломбы для стоматологии и др. Введение в формулу лекарственного препарата двойной связи усиливает биологическое действие препарата на организм. Например, гексенал активнее действует на организм, чем фенобарбитал:
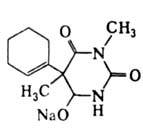
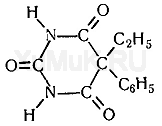
гексенал фенобарбитал
Ацетилен используется при получении таких химических веществ, как уксусная кислота, ароматические углеводороды, этиловый спирт; обладает наркотическими свойствами.
ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДЫ
Для качественного обнаружения моногалогенопроизводных (производные хлора и брома) углеводородов пользуются пробой Ф.Ф. Бельштейна. Для этого их вносят на медной проволочке в пламя горелки. При этом пламя окрашивается в зеленый цвет. Этот метод обнаружения галогенов в органических соединениях используется в органической химии и фармацевтическом анализе. Трех - и четырехпроизводные метана, как например, трихлорметан (СНС13) и тетрахлорметан (СС14) не горят зеленым пламенем.
Йодпроизводные углеводороды взаимодействуют с нитратом серебра. Причем такие реакции проходят лучше и до конца в спиртовых растворах. В результате чего образуется желтый осадок иодида серебра.
С2Н5ОН
С2Н5 I + АgNО3 -----> С2Н5ОNО2 + АgI↓
иодэтан этиловый эфир
азотной кислоты
Хлор - и бромпроизводные углеводороды с нитратом серебра при обычных условиях не дают осадка галогенида серебра.
Галогенпроизводные углеводороды являются лекарственными средствами, и широко используются в медицинской практике.
Хлорэтан (этилхлорид, С2Н5С1) – применяют как местноанестезирующее (обезболивающее) средство.
Хлороформ(1,1,1 – трихлрметан, СНС13)– как средство для ингаляционного наркоза, ввел в хирургическую практику Н.И. Пирогов во времена Крымской войны (1853 – 1856 г.г.); в наше время используется для анализа катионов и анионов для экстракции.
Йодоформ(1,1,1 –трийодметан, СНI3)-антисептическое (обеззараживающее) средство в хирургических перевязках, в виде присыпок и мазей.
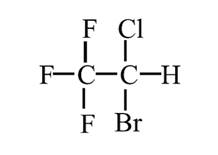 Фторотан (галотан)
Фторотан (галотан)
(2 – бром - 1,1,1 – трифтор - 2 –хлорэтан) эффективное средство для общего наркоза.
Трихлорэтилен (НС1С = СС12) – мощное наркотическое средство при необходимости кратковременного наркоза.
Дата добавления: 2021-01-11; просмотров: 948;











