От концентрации субстрата.
Пропорциональная зависимость скорости реакции от концентрации субстрата наблюдается лишь при его низких концентрациях, затем постепенно прирост скорости реакции начинает отставать от роста концентрации субстрата, и в конце концов увеличение концентрации субстрата перестает вызывать возрастание скорости реакции. Скорость ферментативных реакций при высоких концентрациях субстрата приближается к определенному пределу, который называется максимальной скоростью -Vmax (рис. 3).
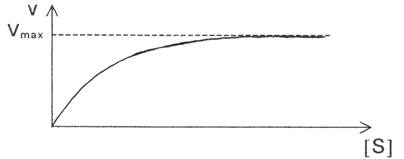 |
Рис. 3. Зависимость скорости ферментативной реакции
От концентрации субстрата
Физический смысл этого явления заключается в следующем: при очень низких концентрациях субстрата скорость реакции зависит от скорости поступления молекул субстрата на активный центр фермента. По мере роста концентрации субстрата количество свободных активных центров уменьшается, так как фермент переходит в фермент-субстратный комплекс и лимитирующей стадией катализа теперь будет не присоединение субстрата к активному центру фермента, а дальнейшие превращения фермент-субстратного комплекса. При очень высоких концентрациях субстрата свободного фермента больше не будет, он весь находится в составе фермент-субстратного комплекса. В этом случае скорость ферментативной реакции станет максимальной и будет обусловлена концентрацией фермент-субстратного комплекса, т.е. концентрацией фермента.
Зависимость скорости ферментативной реакции
От температуры.
График зависимости скорости ферментативной реакции от температуры имеет колоколообразный характер (рис. 4). Вначале повышение температуры вызывает возрастание скорости ферментативной реакции, затем скорость реакции достигает максимума, и при дальнейшем увеличении температуры скорость реакции снижается вплоть до её прекраще
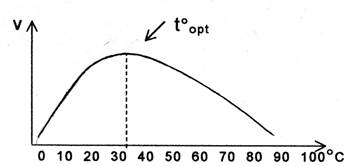 |
ния. Температура, при которой отмечается наибольшая скорость реакции, называется температурным оптимумом реакции - t°opt.
Рис. 4. Зависимость скорости ферментативной реакции
От температуры
Возрастание ферментативной активности при повышении температуры от низких величин до температурного оптимума (левая ветвь кривой на рис. 4) объясняется увеличением среднего энергетического уровня и числа столкновений реагирующих молекул с ростом температуры. Согласно правилу Вант-Гоффа повышение температуры на 10° вызывает увеличение скорости химической реакции в 2-4 раза. Это правило относится ко всем химическим реакциям и, в том числе, к ферментативным.
Снижение активности ферментов при повышении температуры выше температурного оптимума (правая ветвь кривой на рис. 4) объясняется тепловой денатурацией ферментного белка, которая при высоких температурах (80-100°С) вызывает полную потерю каталитической активности фермента.
Для большинства ферментов температурный оптимум равен 37-40°С, т.е. соответствует температуре тела. В очень коротких опытах температурный оптимум может быть более высоким, так как за очень малое время денатурация фермента произойти не успевает.
Как видно из рис. 4, при очень низких (ниже 0°С) и высоких (80-100°С) температурах активность ферментов равна нулю. Однако при низких температурах ферменты сохраняют свою нативность и при повышении температуры у них вновь появляется каталитическая активность. В настоящее время ферменты выделяют из растворов путем лиофильной сушки, т.е. сушки в замороженном состоянии при очень низком давлении. Полученные таким образом лиофилизированные ферментные препараты хорошо сохраняются в течение длительного времени даже при комнатной температуре.
Действие же высоких температур приводит к необратимой потере ферментами способности ускорять химические реакции, так как в этом случае происходит их необратимая денатурация. Поэтому на практике для подавления ферментативной активности (например, ферментов микробов, вызывающих порчу пищевых продуктов) обычно используется термическая обработка.
Дата добавления: 2020-07-18; просмотров: 563;











