ХАРАКТЕРИСТИКА ТОПЛИВА
СОСТАВ ТОПЛИВА
Твердые и жидкие топлива состоят из горючих (углерода - 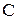 , водорода -
, водорода - 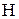 , летучей серы -
, летучей серы - 
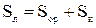 ) и негорючих (азота -
) и негорючих (азота - 
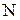 , кислорода -
, кислорода - 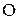 ) элементов и балласта (золы -
) элементов и балласта (золы - 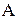 , влаги -
, влаги - 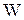 ).
).
Газообразные топлива состоят из горючих ( 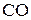 ,
, 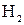 ,
, 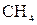 ,
, 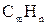 ) и негорючих (
) и негорючих ( 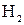 ,
, 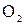 ,
, 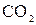 ) газов и небольшого количества водяных паров (
) газов и небольшого количества водяных паров ( 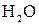 ).
).
При изучении характеристик твердых и жидких топлив и их состава различают рабочую, горючую и сухую массу. Состав рабочей, горючей и сухой массы обозначается соответственно индексами «р», «г», «с» и выражается следующими равенствами:
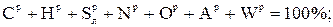 (1.1)
(1.1)
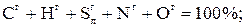 (1.2)
(1.2)
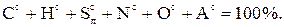 (1.3)
(1.3)
В формулах (1.1), (1.2), (1.3) содержание элементов дано в процентах на 1 кг топлива. Коэффициенты пересчета состава топлива из одной массы в другую приведены в табл.1.1.
Таблица 1.1
| Заданная масса топлива | Коэффициенты пересчета на массу | ||
| рабочую | горючую | сухую | |
| Рабочая | 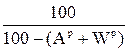
| 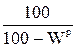
| |
| Горючая | 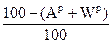
| 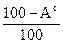
| |
| Сухая | 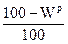
| 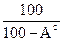
|
Для сланцев состава ( 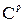 ,
, 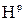 ,
, 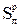 ,
, 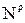 ,
, 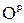 ,
, 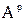 ,
, 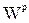 ) пересчет с рабочей массы на горючую осуществляется с помощью коэффициента
) пересчет с рабочей массы на горючую осуществляется с помощью коэффициента
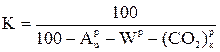 (1.4)
(1.4)
где 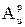 - истинная зольность рабочей массы, %;
- истинная зольность рабочей массы, %; 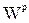 - влажность рабочей массы, %;
- влажность рабочей массы, %; 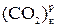 - содержание углекислоты карбонатов, %.
- содержание углекислоты карбонатов, %.
Истинная зольность рабочей массы определяется по формуле:
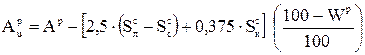 , (1.5)
, (1.5)
где 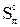 - содержание серы в лабораторной золе в процентах к массе топлива;
- содержание серы в лабораторной золе в процентах к массе топлива; 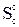 - содержание сульфатной серы в топливе, %.
- содержание сульфатной серы в топливе, %.
Величина 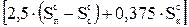 для ленинградских и эстонских сланцев может быть принята равной 2,0, для кашпирских - 4,1.
для ленинградских и эстонских сланцев может быть принята равной 2,0, для кашпирских - 4,1.
Пересчет состава (%) рабочей массы топлива при изменении влажности проводится по формулам:
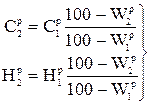 , (1.6)
, (1.6)
где 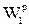 - начальная влажность топлива, %;
- начальная влажность топлива, %; 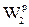 - конечная влажность топлива, %.
- конечная влажность топлива, %.
Средний состав (%) смеси двух твердых или жидких топлив, заданных массовыми долями, - первого ( 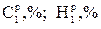 ) и второго
) и второго 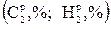 - определяется уравнениями:
- определяется уравнениями:
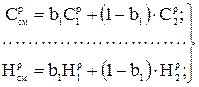 , (1.7)
, (1.7)
где массовая доля 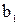 одного из топлив в смеси находится по формуле:
одного из топлив в смеси находится по формуле:
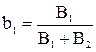 , (1.8)
, (1.8)
где 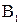 и
и 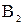 - массы топлив, входящих в смесь, кг.
- массы топлив, входящих в смесь, кг.
ХАРАКТЕРИСТИКА ТОПЛИВА
Теплота сгорания топлива. Теплотой сгорания топлива называют количество теплоты в кДж, выделяемой при полном сгорании 1 кг твердого (жидкого) или 1 м3 газообразного топлива.
Для твердого и жидкого топлива различают теплоту сгорания высшую 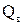 (кДж/кг) и низшую
(кДж/кг) и низшую 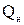 (кДж/кг).
(кДж/кг).
Величины высшей и низшей теплоты сгорания рабочей, горючей и сухой массы твердого (жидкого) топлива связаны выражениями:
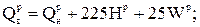 (2.1)
(2.1)
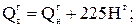 (2.2)
(2.2)
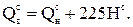
Тепловые расчеты печей, котлов выполняют, пользуясь низшей теплотой сгорания рабочей массы твердого и жидкого топлива.
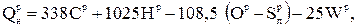 (2.3)
(2.3)
где 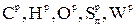 - содержание элементов в рабочей массе топлива, %.
- содержание элементов в рабочей массе топлива, %.
Низшая теплота сгорания (кДж/м3) газообразного топлива:
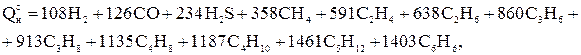 (2.4)
(2.4)
где 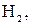
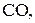
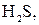
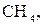
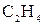 и т.д. - объемное содержание газов, входящих в состав газообразного топлива, %.
и т.д. - объемное содержание газов, входящих в состав газообразного топлива, %.
При пересчете низшей теплоты сгорания пользуются следующими формулами:
с горючей массы на рабочую и обратно
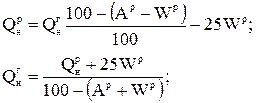
 (2.5)
(2.5)
с сухой массы на рабочую и обратно
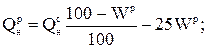
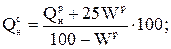
для горючих сланцев - с горючей массы на рабочую и обратно
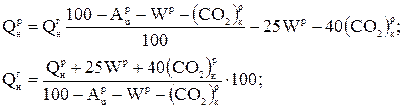
при изменении влажности
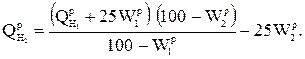
Для смеси двух твердых, жидких или газообразных топлив низшая теплота сгорания определяется по формуле
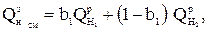
где 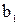 - массовая доля одного из топлив в смеси;
- массовая доля одного из топлив в смеси; 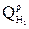 - низшая теплота сгорания первого вида топлива в смеси, кДж/кг (кДж/м3);
- низшая теплота сгорания первого вида топлива в смеси, кДж/кг (кДж/м3); 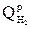 - низшая теплота сгорания второго вида топлива, кДж/кг (кДж/м3).
- низшая теплота сгорания второго вида топлива, кДж/кг (кДж/м3).
Для сравнения тепловой ценности различных видов топлива пользуются понятием условного топлива. Условным топливом называют такое топливо, теплота сгорания которого равна 29300 кДж/кг.
Пересчет расхода натурального топлива на условное осуществляется по формуле
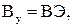 (2.6)
(2.6)
где 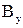 и B - соответственно расход условного и натурального топлива, кг, кг/с; Э - тепловой эквивалент топлива, определяемый по формуле
и B - соответственно расход условного и натурального топлива, кг, кг/с; Э - тепловой эквивалент топлива, определяемый по формуле
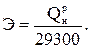 (2.7)
(2.7)
Зольность, влажность и сернистость топлива.При рассмотрении условий работы котлов, печей на различных видах топлива пользуются приведенными величинами зольности 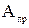 , влажности
, влажности 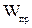 и сернистости
и сернистости 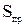 топлива:
топлива:
приведенная зольность топлива, 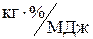 ,
,
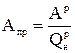 ; (2.8)
; (2.8)
приведенная влажность топлива, 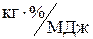 ,
,
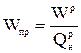 ; (2.9)
; (2.9)
приведенная сернистость топлива, 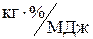 ,
,
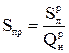 . (2.10)
. (2.10)
Дата добавления: 2020-05-20; просмотров: 412;











