Глава 16 МЕТАЛЛЫ И СПЛАВЫ
ОБЩИЕ СВЕДЕНИЯ
Для изготовления деталей (заготовок) машин, приборов, агрегатов, радиоэлектронных изделий используют конструкционные материалы и материалы специального назначения (электротехнические, полупроводниковые и др.).
Конструкционные материалы подразделяют на металлические, неметаллические и композиционные.
Особо большое значение в народном хозяйстве имеют металлы и их сплавы благодаря наличию комплекса свойств: высокой твердости, прочности, вязкости, пластичности, тепло- и электропроводности и др. Все металлы и сплавы делят на черные (на основе железа) и цветные. Наибольшее применение имеют сплавы, получаемые на основе меди, алюминия, цинка.
Металлы и их сплавы могут находиться в твердом, жидком и газообразном агрегатных состояниях. Переход металлов и их сплавов в то или иное агрегатное состояние связан с изменением температуры, давления.
В твердом состоянии металлы и сплавы имеют кристаллическое строение. В кристаллах атомы располагаются в строго определенном порядке, образуя при этом простые или сложные решетки. Наиболее характерными для металлов являются: объемно-центрированная кубическая (рис. 16.1, а), гранецентрированная кубическая (рис. 16.1,6) и гексагональная плотноупакованная (рис. 16.1, в) решетки.
Большое влияние на развитие науки о металлах и законов построения кристаллической решетки оказали работы М. В. Ломоносова, Д. И. Менделеева, П. П. Аносова, Е. С. Федорова и Д. К. Чернова.
Первичная кристаллизация металла (сплава) — процесс его перехода из жидкого в твердое состояние. В отличие от материалов, которые затвердевают при понижении температуры постепенно (рис. 16.2, а), металлы кристаллизуются при постоянной температуре, называемой критической температурой фазового превращения или теоретической температурой кристаллизации Ts. Практически же переход металла из жидкого состояния в твердое, кристаллическое проходит при температурах ниже Ts (в интервале от Ts до Тф) (рис. 16.2,6).
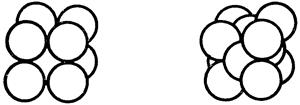
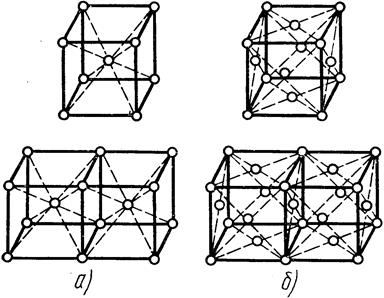
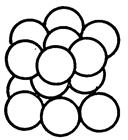
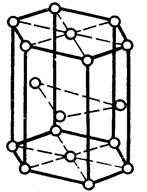
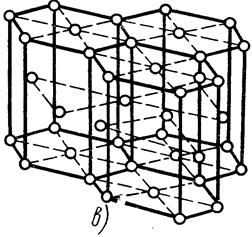
Рис. 16. 1
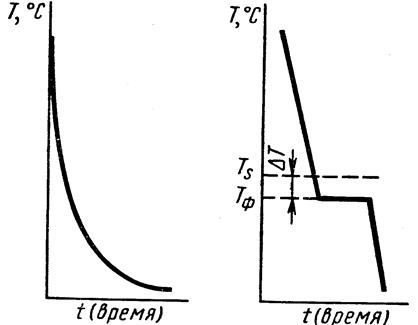
Рис. 16.2
Разность температур Ts- Тф = AT называется степенью переохлаждения. Таким образом, фазовое превращение — это скачкообразный переход металла (сплава) из одной фазы в другую под воздействием внешних факторов (температуры, давления) с изменением его свойств. Фазовые превращения могут проходить и в твердых металлах при изменении температуры.
В производстве различных изделий детали (заготовки) из чистых металлов применяются очень редко. Это объясняется трудностью получения абсолютно чистых металлов и их низкими механическими свойствами. Например, в чистом железе, получаемом современной технологией, содержание примесей не превышает 0,01 %; оно практически не используется.
В электротехническом производстве для изготовления электромагнитов, якорей электрических машин исполь-
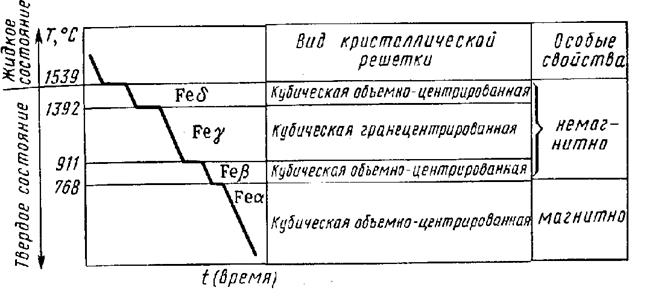
Рис 16.3
зуют технически чистое железо, содержание примесей в котором находится в пределах 0,1—0,2%.
В преобладающем большинстве случаев для изготовления деталей изделий применяют сплавы. Сплав может представлять собой химическое соединение, твердый раствор, механическую смесь или их совокупность.
Химические соединения (интерметаллиды) наиболее характерны для элементов, относящихся к разным периодам и подгруппам периодической системы Д. И. Менделеева (например, золото — цинк, магний — свинец).
Твердые растворы — это твердые фазы, включающие в различных соотношениях атомы разных элементов в одной кристаллической решетке.
Механические смеси образуют вещества, не вступающие в химические соединения и не способные образовать твердые растворы.
Для получения сплава с требуемыми свойствами подбирают необходимые компоненты в различных соотношениях. Свойства сплава могут изменяться от внешних факторов (температуры, давления и др.). Состояния сплавов в зависимости от температуры и соотношения компонентов иллюстрируются диаграммой состояния сплава.
Следует отметить, что при изменении внешних факторов, например температуры, отдельные металлы (железо, кобальт и др.) могут приобретать новые свойства и структуру. Существование вещества с различными кристаллическими структурами и физическими свойствами называется аллотропией. Аллотропические формы обозначают буквами греческого алфавита: α, β, γ, δ.
Простейшая диаграмма состояния для железа — кривая охлаждения показана на рис. 16.3.
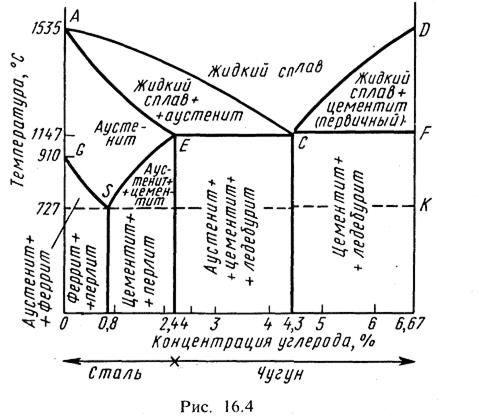
Наиболее сложной является диаграмма состояния сплава железо - углерод, упрощенный вид которой представлен на рис. 16.4. Оба элемента (железо и углерод) обладают способностью к аллотропии. Поэтому они могут образовывать химические соединения и твердые растворы, в которых даже незначительное изменение содержания углерода ведет к изменению структуры и свойств сплава.
Сплавы железо — углерод в зависимости от содержания углерода делятся на стали (содержание углерода до 2,14%) и чугуны (содержание углерода более 2,14%). Предельное содержание углерода в сплаве 6,67%.
Линии диаграммы ACD и AECF соответствуют фазовым превращениям. Сплавы железо — углерод, расположенные выше линии ACD, называемой линией ликвидуса, находятся в жидком состоянии. Линия AECF называется линией солидуса. Ниже линии солидуса сплавы любой концентрации находятся в твердом состоянии. Между линиями ликвидуса и солидуса сплавы имеют жидкотвердое (двухфазное) состояние.
При охлаждении жидкого сплава ниже линии АС в нем образуются кристаллы аустенита — твердого раствора углерода в железе (его аллотропической формы γ-железа). Твердый раствор углерода в α-железе называется ферритом; область чистого феррита незначительна (на диаграмме не показана).
Охлаждение сплава (с высоким содержанием углерода) ниже линии CD связано с образованием цементита (первичного), т. е. устойчивого химического соединения железа с углеродом Fe3C (карбида железа).
При дальнейшем понижении температуры аустенит претерпевает вторичную кристаллизацию, сопровождающуюся изменением формы кристаллической решетки и растворимости углерода. В низкоуглеродистых сплавах из аустенита выделяется феррит (ниже линии GS), в сплавах с более высоким содержанием углерода — цементит вторичный (ниже линии SE).
У низкоуглеродистых сплавов (до 0,8 % С) непрерывно возрастающее количество феррита, вызванное понижением температуры, ведет к выделению углерода и насыщению им оставшегося аустенита. При 727 °С насыщенный аустенит превращается в перлит — эвтектоидную смесь цементита и феррита. Структура таких сплавов после охлаждения будет состоять из феррита и перлита.
При охлаждении сплавов, содержащих углерода более 0,8% (до 2,14%), аустенитные зерна непрерывно растут за счет цементитной сетки и обедняются углеродом. При температуре 727 °С аустенит превращается в перлит, а структура охлажденного сплава будет включать перлит и цементит (вторичный).
Сплав, содержащий 0,8% С, называют эвтектоидной сталью; менее 0,8% — доэвтектоидной, а более 0,8 — заэвтектоидной. Структура эвтектоидной стали — перлит.
Чугуны по содержанию углерода делятся на доэвтектические (2,14-4,3% С), эвтектические (4,3% С), заэвтектические (4,3-6,67% С).
Доэвтектический чугун начинает кристаллизоваться при температурах ниже линии АС. С понижением температуры содержание аустенита увеличивается, а жидкая фаза обогащается углеродом. При 1147°С происходит эвтектическое превращение чугуна с образованием ледебурита (эотектики - механической смеси аустенита и цементита). Наличие ледебурита в структуре характерно для всех видов чугуна.
Часть диаграммы состояния сплава железо — углерод, относящаяся к сталям, имеет огромное значение при выборе режимов термической обработки для получения новой структуры и свойств сталей.
Дата добавления: 2016-06-22; просмотров: 3185;











