ТЕОРИИ РЕГУЛЯЦИИ ПОТРЕБЛЕНИЯ ПИЩИ
Вводные замечания
Одним из фундаментальных свойств организмов является их способность возмещать потерю расходуемых веществ и поддерживать определенный уровень пластических и энергетических материалов (см. гл. 2 и 3). Это достигается с помощью специального механизма, контролирующего потребление пищи, который все еще остается во многих отношениях загадочным. Благодаря этому механизму обеспечивается соответствие поступающих веществ и веществ, расходуемых на процессы жизнедеятельности, включая основной обмен, рост, размножение, внешнюю работу и т. д. Такое равновесие между поступлением и расходом веществ - непременное условие длительного существования организмов. Ясно, однако, что для поддержания такого соответствия необходима весьма сложная система управления, особенно учитывая сложность химического состава организма. Система управления должна получать прямые и косвенные сигналы о недостатке или избытке определенных веществ в организме и трансформировать их в соответствующие формы пищевой активности. При этом происходит стимуляция или торможение пищевой деятельности, а также изменение ее направления. В многоканальную систему управления включены как система рецепторов (обонятельных, вкусовых, зрительных, желудочно-кишечного тракта, внутренней среды, центральной нервной системы), так и система гормональных факторов.
На многих этапах химический состав пищи и концентрация жизненно необходимых молекул рецептируются и соответствующая информация поступает в так называемый пищевой центр, контролирующий пищевую активность, т. е. инициирующий и прекращающий потребление пищи, а также участвующий в ее выборе. В отличие от многих традиционных механизмов управления, где поддержание некоторых параметров достигается в пределах самой системы, аппетит регулируется по типу, характерному для открытых систем. В этом случае имеет место гомеостатирование за счет регулирования входа и выхода данной системы.
Мысль об автоматическом управлении потреблением пищи пищевым центром мозга была, по-видимому, впервые высказана И. П. Павловым в 1911 г. В настоящее время вопрос о механизмах регуляции потребления пищи стал привлекать пристальное внимание физиологов, биохимиков и клиницистов. В особенности детально исследуются структура и функции пищевого центра, который охватывает многие структуры центральной нервной системы и контролирует как поведенческие, так и вегетативные процессы, связанные с потреблением и усвоением пищи.
Весьма совершенная регуляция потребления пищи характерна не только для высших форм жизни, но и для примитивных организмов, например кишечнополостных. Более того, даже применительно к простейшим можно, по-видимому, говорить о регуляции потребления пищи и ее выбора, о насыщении и аппетите, о соответствии потребляемой пищи потребностям в ней и т.д. В первом приближении можно считать, что избыток какого-либо вещества приводит к торможению аппетита к данному веществу, а недостаток его в организме вызывает усиленное потребление.
Все эти вопросы рассмотрены в фундаментальных обзорах, посвященных регуляции выбора и потребления пищи, а также взаимоотношениям этих процессов с обменом веществ (Handbook..., 1967; Weser, 1973; Асатиани, Бакурадзе, 1974; Booth, 19/4; Slanger, 1974; Hall, 1975; Lepkovsky, 1975; Hunger..., 1976; Committee..., 1980; Management..., 1985; Morleyetal., 1985; Fisler, 1987; Замбржицкий, 1989; Thephysiology..., 1989; Кассиль, 1990; Greenetal., 1990, и др.), а также в наших специальных сводках (Уголев, Кассиль, 1961, 1972; Кассиль и др., 1970; Уголев, 1978, и др.).
8.2. Регуляция аппетита
Представляется важным начать этот раздел словами, сказанными нами еще в 1961 г.: "...в процессе эволюции аппетит формируется не как реакция на уже возникшее истощение пищевых ресурсов, но как механизм, задолго предупреждающий такое истощение... Теории, связывающие голод и аппетит с исчерпанием запасов, несмотря на подкупающую простоту, должны быть отвергнуты. Аппетит не следует за исчерпанием депо пищевых веществ, но предваряет и не допускает его... Многочисленные раздражители, формирующие состояние голода и аппетита, имеют до известной степени сигнальный характер. Это обусловливает пластичность и нестандартность управления процессами питания" (Уголев, Кассиль, 1961. С. 364).
Как отмечено выше, регуляция аппетита у высших организмов, включая человека, связывается с деятельностью сложноорганизованного и расположенного на многих уровнях центральной нервной системы пищевого центра. Пищевой центр - это не очень определенное понятие о системе структур, локализованных в головном мозге и обеспечивающих различные стороны регуляции пищевой деятельности. В инициации пищевой активности, ее торможении и регуляции пищевого мотивированного поведения важная роль отводится латеральной области и вентромедиальным ядрам гипоталамуса. Это доказывается тем, что разрушение его определенных участков приводит к тяжелым нарушениям питания у экспериментальных животных.
В настоящее время принято, что при всех обстоятельствах гипоталамус является одним из основных звеньев, участвующих в формировании пищевой мотивации. При этом на состояния голода и сытости оказывают влияние так называемые центральные и периферические пептиды, эндогенные факторы, продукты обмена и т. д. Кроме того, продемонстрировано, что пищевое поведение может определяться структурно-функциональным состоянием всех отделов головного мозга, в том числе бледного шара, красного ядра, покрышки среднего мозга, черной субстанции, височной и лобных долей, таламуса, гиппокампа, неокортекса и ряда других. Обширная литература, касающаяся этой проблемы, а также морфофункциональных характеристик пищевого центра, представлена в капитальных обзорах:Замбржицкий, 1989; Кассиль, 1990.
В соответствии с современными взглядами, пищевой гипоталамический центр состоит из нескольких специализированных частей, так называемых центров голода и сытости, которые в свою очередь находятся под корригирующим влиянием ряда центральных образований. Непосредственно в указанные центры через хемочувствителъные элементы, а также через различные периферические рецепторы поступают сигналы, приводящие к активации, торможению или модификации пищевой деятельности.
Однако гипоталамические центры являются лишьчастью структур, связанных с регуляцией пищевого поведения. Имеется много данных, что и другие подкорковые структуры, в частностибледное ядро,стриопаллидарная система и другие,также принимают участие в регуляции аппетита. Значительную роль в организации пищевых реакций играет лимбическая система. Наконец, огромная роль в формировании пищевого поведения принадлежит коре больших полушарий.
В настоящее время трудно представить полную, а тем более исчерпывающую картину регуляции пищевой активности. Тем не менее установлено, что в регуляции аппетита большое значение имеют периферические и центральные рецепторы, а также специфические и неспецифические гормональные сигналы.
Потребление пищи, ее переработка и всасывание в пищеварительном канале, депонирование и расход все эти процессы трансформируются в разнообразные потоки информации, которые в конечном итоге определяют повышение или понижение (вплоть до прекращения) пищевой активности. Различными исследователями сделаны попытки связать регуляцию аппетита с определенными видами обмена веществ. Так сформировалось несколько теорий регуляции аппетита, которые в сжатом виде охарактеризованы ниже. (Обширная сводка литературы представлена в обзорах: Уголев, 1978; Кассиль, 1990.)
8.2.1. Аминоацидстатическая теория
Теория, получившая большую популярность, связывает регуляцию аппетита с изменением уровня аминокислот в крови. Действительно, ряд аминокислот может вызывать понижение аппетита и, следовательно, служить физиологическим сигналом сытости. В настоящее время эта теория приобретает дополнительные аргументы, так как показано, что некоторые аминокислоты являются медиаторами или модуляторами в нервной передаче. Такое сочетание создает исключительные условия для функционирования глутамина, аланина, глицина и некоторых других аминокислот в качестве точечных и гибких регуляторов. При этом их уровень в крови может отражать как условия питания, так и функциональное состояние организма.
8.2.2. Глюкостатическая теория
Эта теория регуляции аппетита отводит важную роль уровню глюкозы в крови и его гомеостатированию. В сущности, выдвинуто несколько глюкостатических теорий. Первая из них связывает торможение пищевой активности с повышением концентрации глюкозы в крови, обычно имеющим место при всасывании пищи, а пищевое возбуждение с ее снижением. Однако эта относительно простая теория не получила широкого распространения, так как многие факты противоречили ей. Тем не менее показано, что в центральной нервной системе, особенно в области гипоталамуса, есть специализированные клетки, обладающие высокой чувствительностью к глюкозе, разрушение которых с помощью токсических аналогов глюкозы приводит к развитию гиперфагии. Согласно некоторым точкам зрения, для регуляции аппетита чрезвычайно важен не абсолютный уровень глюкозы в крови, а ее артерио-венозная разница, возрастающая при сытости и падающая до отрицательных значений при голодании. Наличие специализированных глюкорецепторов, связанных с регуляцией аппетита, является аргументом в пользу глюкостатической теории, так же как и ряд фактов, свидетельствующих о том, что в центральной нервной системе имеются нейроны, отвечающие на локальную гипергликемию. Влияние на аппетит глюкозы и аминокислот может реализоваться через некоторые общие звенья метаболизма (см. метаболическую теорию регуляции аппетита).
8.2.3. Липостатическая теория
Весьма привлекательна липостатическая теория, связывающая появление аппетита с переходом от питания экзогенными нутриентами к мобилизации жировых депо. Эта теория говорит, что пищевая деятельность активируется автоматически в момент перехода от экзотрофии к эндотрофии. Однако остается не вполне ясной природа сигналов, возбуждающих голод. Возможно, в этом процессе определенную роль играет выделение гормонов, обеспечивающих мобилизацию жировых депо.
8.2.4. Дегидратационная теория
Дегидратационная теория объясняет чувство насыщения физиологическим обезвоживанием крови. Такое обезвоживание происходит при интенсивном пищеварении в связи с переходом части жидкости в виде секретов из крови в желудочно-кишечный тракт. По всей вероятности, такой механизм имеет определенное значение в качестве одного из компонентов сытости.
Однако с позиций этой теории трудно объяснить происхождение голода, который мог бы возникать при питье воды в результате увеличения объема циркулирующей жидкости, чего в действительности никогда не происходит. Физиологическое обезвоживание крови, по-видимому, может иметь большее отношение к регуляции потребления воды, т. е. к возникновению чувства жажды, чем к регуляции голода.
8.2.5. Термостатическая теория
Особое место занимает теория, связывающая прекращение еды с локальным повышением температуры тела, в частности гипоталамической области, где представлены центры голода и сытости. Согласно этой теории, животные едят для того, чтобы не остывать, и прекращают еду, чтобы не перегреваться (Strominger, Brobeck, 1953). Предполагается, что эффект насыщения тем выше, чем больше специфическое динамическое действие (СДД) пищи. Причем чем сильнее повышается температура, тем сильнее тормозится аппетит. Эта точка зрения получила ряд экспериментальных подтверждений. Вместе с тем она подверглась справедливой критике, так как не могла объяснить многих особенностей регуляции аппетита.
8.2.6. Метаболическая теория
Крупным недостатком всех перечисленных теорий является то, что регуляция потребления пищи связывается с обменом одной из групп пищевых веществ - белков, углеводов, жиров, с обменом воды и т. д. В конце концов становится все более очевидным, что все виды обмена веществ имеют отношение к регуляции аппетита. В связи с этим нами была выдвинута так называемая метаболическая теория, согласно которой регуляция аппетита связана с энергетически наиболее значимыми и в то же время общими конечными звеньями метаболизма всех пищевых веществ - циклом Кребса. Эта теория была предложена нами еще в 50-х годах и затем развита совместно с В. Н. Черниговским и В. Г. Кассилем в течение 60-70-х годов (Уголев, 1962; Кассиль и др., 1970; Уголев, Кассиль, 1972; обзор: Уголев, 1978). Впоследствии эта теория получила новые доказательства и подтверждение (Booth, 1974).
В основе метаболической теории лежит предположение, что регуляция потребления пищи должна быть связана прежде всего с освобождением основной части энергии, поступающей в организм с пищей. Как известно, окисление пищевых веществ (жиров, белков, углеводов) завершается циклом Кребса с освобождением до 70% заключенной в пище энергии. В конечном счете деятельность пищевого центра должна быть связана с оценкой заключенной в пище энергии, что согласуется с данными о гипоталамусе как «счетчике калорий». Если так, то можно думать, что метаболиты цикла Кребса имеют первостепенное значение для регуляции потребления пищи. Экспериментальная проверка показала, что такое предположение правильно. Введение голодным крысам натриевой соли лимонной кислоты - метаболита одной из первых стадий цикла Кребса - приводит к более глубокому торможению аппетита, чем введение глюкозы. Особенно важно, что насыщение, вызываемое цитратом, наступает значительно быстрее, чем после введения глюкозы. Очевидно, влияние глюкозы на пищевой центр опосредуется через метаболиты цикла Кребса.
Следует иметь в виду, что метаболическая теория регуляции аппетита не отрицает ни одну из упомянутых выше теорий. Напротив, она позволяет понять глубокую связь различных типов обмена веществ с регуляцией аппетита и варьирование у животных разных видов то одних, то других типов сигналов голода и насыщения.
8.3. Специализированные аппетиты
Взрослые животные поддерживают собственный вес в течение длительного времени как при ограничении, так и при избытке пищи. Следовательно, они обладают способностью каким-то образом учитывать потребность в пищевых веществах. Потребность в калориях определяется периферическими сигналами и пищевым центром, повреждение или патологические изменения которого могут приводить к недостаточному или избыточному поглощению калорий. Можно было бы свести регуляцию потребления пищи к регуляции потребления калорий. Такое предположение, возможно, справедливо для монофагов, т. е. организмов,питающихся определенным типом пищи с одним составом. Однако оно не пригодно для полифагов, у которых экспериментально доказано существование специализированных аппетитов (Уголев, Кассиль, 1972).
Уже в 1911 г. И. П. Павлов подошел к проблеме специализированного отношения к пище, охарактеризовав пищевой центр как один из важнейших регуляторов «химического равновесия тела». Действительно, регуляцию химического состава организма в сфере пищевого поведения нельзя себе представить иначе, чем с точки зрения существования специализации аппетита, благодаря чему человек и животные находят и выбирают именно те виды пищи, которые в данный момент более всего соответствуют их потребностям. По-видимому, дифференцированное отношение к различным видам пищи долгое время не попадало в поле зрения физиологов по той причине, что пищевые реакции рассматривались как врожденные. Имелось, однако, немало наблюдений, свидетельствующих, что даже животные, питание которых узко специализировано, периодически меняют пищевые склонности. Это обстоятельство привело к необходимости выяснить, какие именно сдвиги в организме приводят к изменению выбора пищи и является ли этот выбор адекватным. Очень важно было также определить физиологические механизмы, лежащие в основе регуляции специализированного пищевого поведения. В ряде случаев изменение пищевых склонностей представлялось целесообразной и адаптивной реакцией, в других - создавалось впечатление, что изменение пищевой реакции не адекватно потребностям организма. Ответы на эти вопросы получены лишь частично.
Нельзя не отметить, что переход от описательной стороны проблемы к экспериментальной также связан с именем И. П. Павлова. Еще в 1892 г. он отметил избирательный отказ от мясной пищи собаками с эккпавловским соустьем. Эта реакция рассматривалась как следствие повышения в крови азота, вызванного выключением печени. В более поздних работах сотрудники И. П. Павлова деятельность пищевого центра оценивали как по пищевому поведению, так и по динамике слюноотделения. Было, в частности, показано, что отрицательная реакция на избыточно введенные в организм сахар или поваренную соль проявляется в отказе от этих веществ и выделении на них большого количества жидкой «отмывающей» слюны.
Значительные успехи в области физиологии специализированных аппетитов были сделаны благодаря разработке метода активного выбора пищи. Этот метод наиболее полно был использован и усовершенствован, начиная с работ П. Янга (Young, 1941) и К. Рихтера (Richter, 1956,1957). Было установлено,что крысы, получившие возможность свободного выбора отдельных пищевых компонентов, растут и развиваются лучше, чем животные на стандартной диете, составленной в соответствии с теоретически рассчитанной физиологической нормой. Близкие данные были получены и в педиатрической клинике. Оказалось, что дети, получившие возможность после прекращения молочного вскармливания свободно выбирать пищу, хорошо росли и развивались.
Изменение пищевых склонностей у животных особенно четко удалось проследить при различных патологических состояниях. Так, после удаления надпочечников резко возрастает аппетит к солям натрия, что связано с большими потерями этого элемента с мочой (Richter, 1936). Удаление паращитовидных желез повышает потребность организма в кальции, что вызывает у животных предпочтение пищи с высоким содержанием солей кальция. У крыс с удаленной поджелудочной железой снижается потребление углеводов и повышается потребление жиров.
Многочисленные примеры адаптивного изменения пищевого выбора в соответствии со сдвигами во внутренней среде организма (обзор:Young,1967)ужедавно позволили нам (Уголев, Кассиль, 1972) рассматривать специализированные аппетиты как механизм регуляции гомеостаза. Вместе с тем способность адекватного выбора пищи проявляется далеко не во всех случаях нарушения равновесия во внутренней среде организма. Имеется значительное число исследований, не подтверждающих наличие прямой связи между избытком или недостатком определенных веществ в организме, с одной стороны, и формированием пищевых реакций - с другой. Это обстоятельство приводит к тому, что до сих пор не существует единого мнения о формировании специализированных белкового, углеводного, жирового и витаминного аппетитов.
8.4. Аппетит и кишечная гормональная система
В течение последних десятилетий получено много данных о важной роли кишечных гормонов в регуляции потребления пищи. Кроме того, в течение последней четверти века представления о регуляции аппетита изменились в связи с открытием специализированных гормональных влияний на потребление пищи.
8.4.1.Арэнтерин
В 1960 г. нами (Уголев, 1960б) было продемонстрировано, что экстракты двенадцатиперстной кишки, но не желудка, печени, мышц и селезенки, вызывают специфическое торможение аппетита (рис. 8.1). После введения экстракта двенадцатиперстной кишки поведение голодных крыс напоминало поведение сытых животных. Снижение потребления пищи наблюдалось после введения таких экстрактов как сытым, так и голодным животным. На основании этих данных можно допустить, что существует кишечный гормон или фактор, осуществляющий торможение аппетита, т. е. торможение той важнейшей реакции, которая характеризует изменение поведения человека и животных после удовлетворения пищевых потребностей. В 1962 г. (Уголев, 1962) были получены сведения, которые позволили предположить, что такой фактор, скорее всего, является пептидом. Наличие дуоденального фактора, вызывающего сытость, который был назван нами арэнтерином (аппетитрегулирующим энтерином, т. е. кишечным гормоном), так же как и его пептидная природа получили подтверждение во многих работах. Все же следует отметить, что до сих пор арэнтерин в чистом виде не получен.
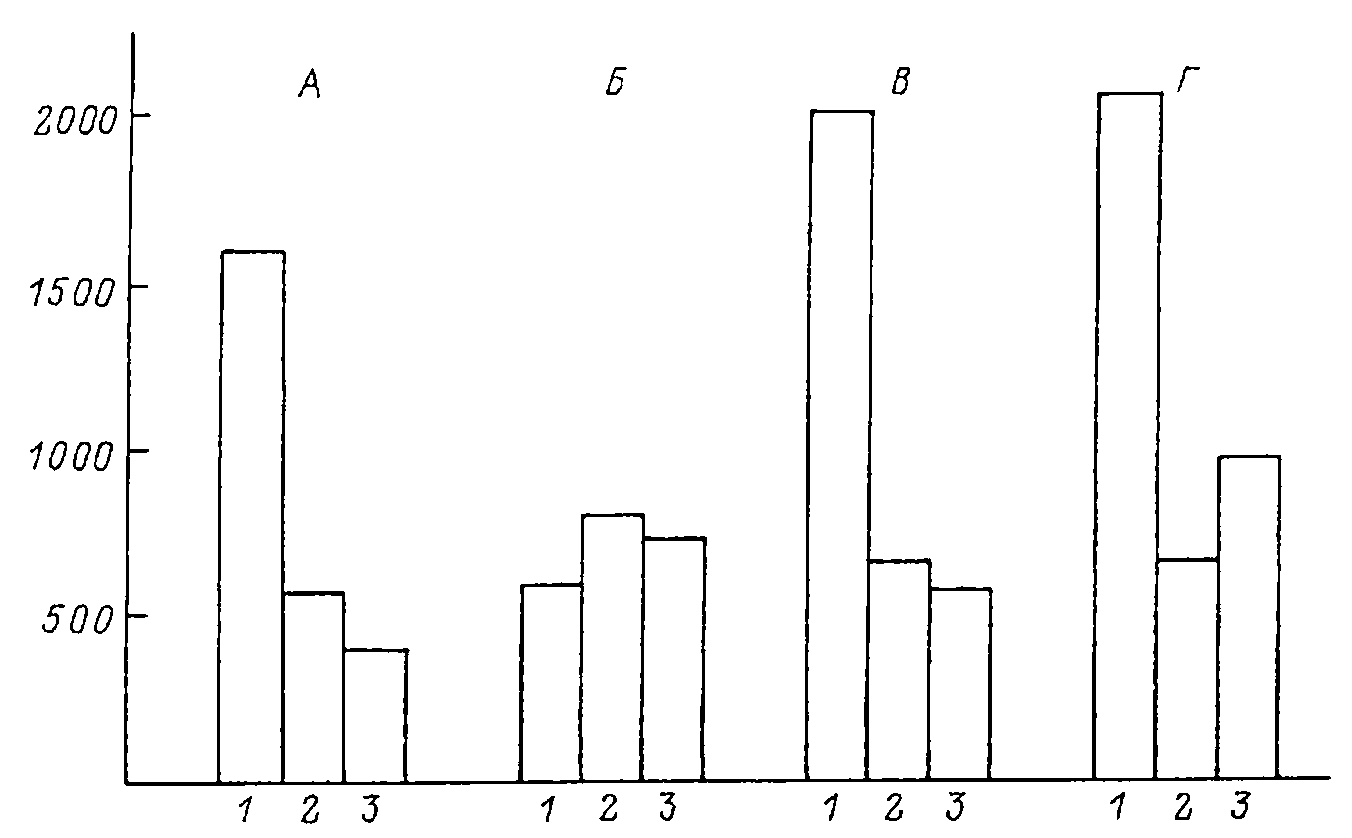
| Рис. 8.1. Потребление пищи предварительно голодавшими крысами после введения раствора Рингера (А), экстрактов двенадцатиперстной кишки (Б), желудка (В) и селезенки (Г) (по: Уголев, 1978). По горизонтали - время от начала кормления: 1 - 0-30 мин, 2 - 30-60 мин, 3 - 60-120 мин; по вертикали - количество потребляемой пищи (мг). |
Попытки охарактеризовать арэнтерин были предприняты группой чл.-корр. АН СССР А. С. Хохлова в Институте биоорганической химии им. М. М. Шемякина АН СССР и в нашей лаборатории. В середине 70-х годов обеими группами было продемонстрировано, что арэнтерин - это белок с молекулярной массой около 100000 (обзоры: Уголев, 1978, 1985).
8.4.2. Другие кишечные гормоны
В 70-х годах было обнаружено, что многие известные гормоны желудочно-кишечного тракта, в частности гастрин и секретин, не оказывают влияния на аппетит. В отличие от них холецистокинин вызывает сильное торможение пищевой активности. Первым, по-видимому, продемонстрировал специфическое влияние холецистокинина на потребление пищи X. Купманс с сотрудниками (Koopmansetal., 1972). В цикле исследований группы Дж. Смита (Smithetal., 1974) на крысах было показано, что холецистокинин может вызывать торможение аппетита. Авторы, однако, оценивали этот эффект, скорее, как фармакологический, чем физиологический. у обезьян также обнаружено торможение потребления пищи после введения холецистокинина. У человека потребление пищи зависит от дозы введенного холецистокинина и от способа его введения. Так, внутривенное введение гормона в дозе 0.5 ед/кг приводит к торможению аппетита, а постепенное внутривенное введение в дозе 1 ед/кг, напротив, вызывает его стимуляцию (Sturdevant, Goetze, 1976). Прямое действие холецистокинина на центры питания и другие нервные центры показано в электрофизиологическом исследовании Н. Дафни и Е. Джекобсона (Dafny, Jacobson, 1975). Наконец, продемонстрировано, что после введения глюкагона возрастает электрическая активность центра сытости. (Более подробно эти вопросы освещены в монографии: Уголев, 1978.).
В 80-е годы интенсивная работа в этом направлении продолжалась. На человеке и животных было вновь продемонстрировано, что в передаче сигнала насыщения большую роль играют кишечные гормоны. Суммируя полученные за эти годы данные, можно сказать, что экзогенный холецистокинин, в том числе его синтетический октапептид холецистокинин-8, вызывает снижение потребления пищи, которое зависит от дозы гормона и места его введения (периферического или центрального). При этом для развития эффекта насыщения необходим сульфатированный тирозин в 7-й позиции С-терминального конца цепи октапептида холецистокинина. Показана также физиологическая специфичность холецистокинина: он ингибирует потребление пищи, но не воды (Smith, 1983; Gibbs, Smith, 1986, и др.).
В последние годы дискутируется вопрос о периферическом и центральном механизмах действия холецистокинина на аппетит. (Физиологический и фармакологический эффекты гормона дифференцировать достаточно трудно.)
Так как систематические инъекции холецистокинина приводят к резкому изменению пищевого поведения, то предполагается, что гормон должен прямо или опосредованно вызывать изменения функционального состояния мозговых структур. Считается, что основным путем передачи информации после введения экзогенного холецистокинина служат афферентные волокна абдоминальной вагусной системы, с рецепторами которой связывается гормон. Кроме того, гормон может связываться и с рецепторами пилорического сфинктера желудка.
Для объяснения эффекта эндогенного холецистокинина привлекается гипотеза, согласно которой освобождение этого гормона, вызывая чувство насыщения, определяет окончание акта еды, следствием чего является соответствующее поведение. По-видимому, эндогенный холецистокинин может прямо влиять на функции мозга, вызывая торможение аппетита. Принято, что основную роль в этом эффекте играют вентромедиальная и латеральная области гипоталамуса.
В последние годы продемонстрировано, что такие кишечные пептиды, как глюкагон, соматостатин и бомбезин, также вызывают торможение потребления пищи, но в меньшей мере, чем холецистокинин. В отличие от этих гормонов секретин, гастрин и ГИП не обладают таким эффектом.
Подробно история развития проблемы и ее современное состояние освещены з ряде детальных сводок (Smith, 1982,1983,1984; Gibbs, Smith, 1986, 1988; Murphyetal., 1988; Кассиль, 1990, и др.).
Наконец, к кишечным пептидным гормонам, ингибирующим потребление пищи, относится также сатиетин (обзор: Замбржицкий, 1989).
Следует отметить, что влияние на аппетит холецистокинина, глюкагона, энтерогастрона и других гормонов, по-видимому, является важной, но скорее дополнительной (а не основной) функцией. По крайней мере в некоторых случаях можно думать об их фармакологическом, а не физиологическом действии. Эти же факты давали возможность предполагать, что среди кишечных гормонов, возможно, существуют такие, которые обладают преимущественно нейротропным действием, и их аппетиттормозящие эффекты будут выражены более отчетливо, чем у известных гормонов. Действительно, нами было продемонстрировано, что арэнтерин влияет на потребление пищевых веществ более эффективно, чем холецистокинин и секретин. В частности, при внутрибрюшинном введении препарата арэнтерина в дозе 0.1 мг на 100 г массы тела крысы наблюдается резкое торможение потребления раствора глюкозы (рис. 8.2). После введения заведомо большей дозы секретина (0.5 мг на 100 г массы тела) торможения аппетита не происходит. Введение холецистокинина также в дозе 0.5 мг на 100 г массы тела вызывает сравнительно слабый и кратковременный эффект (рис. 8.3) (Уголев, 1978).
Итак, эндокринные клетки тонкой кишки, по-видимому, продуцируют более чем один фактор, способный понижать пищевую возбудимость. В одних случаях некоторые из этих факторов - хорошо известные гормоны, проявляющие новые стороны физиологической (или фармакологической) активности, в других случаях - это «новые» гормоны. К числу последних относится арэнтерин. Заслуживает внимания, что арэнтерин обладает большей продолжительностью действия, чем холецистокинин. В этом смысле арэнтерин вообще отличается от большинства кишечных гормонов, эффект которых непродолжителен. Это означает, что кишечная гормональная система способна не только к кратковременным, но и более продолжительным регуляторным эффектам.
Рассмотрим более обобщенно влияние желудочно-кишечных гормонов на потребление пищи. Следует различать два типа эффектов: 1) прямые (гипоталамотропные) эффекты, в том числе арэнтерина и холецистокинина, на структуры гипоталамуса; 2) косвенные эффекты, которые, по-видимому, следует учитывать в комплексе реакций, связанных с нормальным насыщением. В частности, согласно дегидратационной теории регуляции аппетита, физиологическая дегидратация тканей, вызванная секрецией главных пищеварительных органов, служит одной из причин понижения аппетита и возникновения физиологической жажды. С этой точки зрения, можно думать, что в регуляции аппетита опосредованно участвуют: секретин, который стимулирует секрецию жидкой части поджелудочного сока, и гастрин, который вызывает значительную по объему секрецию желудочного сока. Кроме того, растяжение желудка, ацидификация желудка и верхних отделов двенадцатиперстной кишки являются также источником нервных сигналов, передаваемых главным образом по блуждающим нервам.
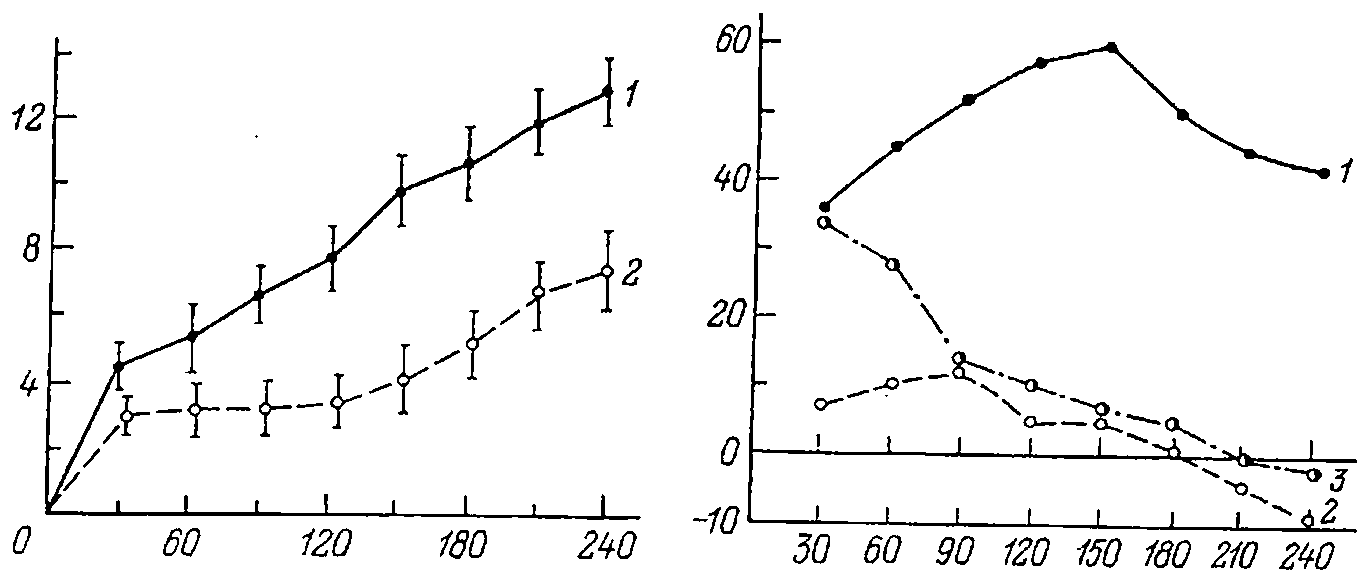
| Рис. 8.2. Потребление глюкозы после внутрибрюшинного введения раствора Рингера и препарата арэнтерина (по: Уголев, 1978). По оси абсцисс - время после потребления глюкозы (мин); по оси ординат - количество выпитого 40%-ного раствора глюкозы (мл). 1 - после введения раствора Рингера, 2 - после введения арэнтерина. Рис. 8.3. Торможение потребления глюкозы после внутрибрюшинного введения препаратов арэнтерина, секретина и холецистокинина (по: Уголев, 1978). По оси абсцисс - время после потребления глюкозы (мин); по оси ординат - торможение потребления 40%-ного раствора глюкозы (% по отношению к исходному уровню). 1 - после введения арэнтерина; 2 - после введения секретина; 3 - после введения холецистокинина. |
Особого рассмотрения заслуживает роль кишечной гормональной системы в потреблении пищи в связи с термостатической теорией регуляции аппетита. Ряд данных позволяет считать, что СДД пищи и изменение внутренней, в частности гипоталамической, температуры могут быть важным компонентом нормального насыщения. Так, показано, что повреждения ростральной области гипоталамуса, связанной с регуляцией как температуры, так и потребления пищи, приводят к нарушению обеих этих функций (обзор:Hamilton, 1967). Здесь необходимо напомнить о существовании обнаруженных нами компонентов СДД пищи (см. гл. 7), контролируемых кишечной гормональной системой и действием желудочного химуса при его прохождении через двенадцатиперстную кишку. Понижение пищевого возбуждения, связанное с интенсификацией обмена, и повышение внутренней температуры также в определенной мере обусловлены включением кишечного гормонального комплекса. В целом прохождение пищи через верхние отделы пищеварительного аппарата вызывает выделение ряда гормонов желудочно-кишечного тракта, прямо или косвенно влияющих на переход от голодного состояния к сытому и во многих случаях к появлению питьевых реакций. К гормонам, вызывающим физиологическую дегидратацию, которая благоприятствует понижению пищевого возбуждения и повышению питьевого, относятся гастрин и секретин. Дегидратация может влиять на пищевой центр как через периферические, так и через центральные осморецепторы.
В свете обсуждаемых данных обращает на себя внимание недавнее исследование, на основании которого высказано предположение, что мотилин играет важную роль в контроле моторной деятельности не только у собак и людей, но и у свиней (Bull, Sissons, 1988).
Совершенная регуляция потребления пищи включает в себя два типа регуляторов, различающихся по своим временным характеристикам: быстродействующие (кратковременные) и длительно действующие (долговременные). Как правило, регуляция первого типа обеспечивает срочные, но не вполне точные реакции, тогда как медленные регуляции обеспечивают точное соответствие между потребностью в калориях и их поглощением.
Таким образом, если существует несколько типов кишечных гормонов, влияющих на аппетит (а их должно быть несколько, в том числе арэнтерин и холецистокинин), то с их помощью реализуются как более быстрые, так и более медленные типы регуляции аппетита, или потребления пищи (рис. 8.4).

| Рис. 8.4. Схема нейрогуморалъной регуляции аппетита с участием арэнтерина (по: Уголев, 1978). |
До сих пор мы рассматривали влияние кишечной гормональной системы на пищевой центр, сузив эту проблему до регуляции потребления пищевых веществ. В действительности речь идет о том, что кишечная гормональная система путем изменения мотиваций участвует в переключении целенаправленного поведения, характерного для голодного животного, на поведение, свойственное сытому животному. Поэтому можно думать, что чем дальше будет развиваться эта проблема, тем больше места в ней будет занимать область нейротропных и психотропных влияний кишечной гормональной системы.
Как отмечено выше, Н. Дафни Е. Джекобсон (Dafny, Jacobson, 1975) показали, что гормоны желудочно-кишечного тракта, продуцируемые при потреблении пищи, индуцируют насыщение посредством изменения электрической активности центральной нервной системы. По мнению авторов, центр аппетита взаимодействует с вышележащими центрами, которые могут влиять на тонус сосудов, моторику пищеварительного аппарата и секреторную активность. Предполагается, что холецистокинин может действовать как модулятор одного из известных химических мессенджеров. Вместе с тем эти данные подтверждают высказанную нами мысль, что эффекты гормонов желудочно-кишечного тракта должны охватывать в конце концов более значительную сферу реакций, чем только контроль над пищеварительными процессами.
В целом приведенные сведения свидетельствуют, что кишечная гормональная система может играть важную роль не только в контроле обмена веществ за пределами пищеварительного аппарата, но и в управлении поведенческими реакциями, прямо или косвенно связанными с регуляцией потребления пищи.
Дата добавления: 2016-06-22; просмотров: 3423;











