Судьба глюкозы в клетке
Доставленный к клетке током крови моносахарид легко диффундирует в цитозоль. Для его проникновения в липо-, мио-, гепатоциты требуются специальные белки-переносчики – ГЛЮТ-4, которые активируются инсулином. По этой причине гипоинсулинизм в мышечной ткани вызывает энергетический голод, в адипоцитах тормозит синтез жиров, а в инсулиннезависимых органах избыток глюкозы оказывает токсическое действие.
У здорового человека данный моносахарид по мере поступления в цитозоль клеток активируется с помощью гексокиназы с образованием глюкозо-6-фосфата (рис. 1).

Рис. 1. Активация глюкозы
Его дальнейшая судьба в большинстве клеток однотипна (рис. 2). Большая часть подвергается распаду.

Рис. 2. Судьба глюкозы в клетке
Основной путь – гликолиз (греч. glucose – сладкий, lysis – распад) – распад глюкозо-6-фосфата, протекающий с высвобождением энергии. Этот процесс не зависит от наличия кислорода, но и количество образовавшихся в нем молекул АТФ при гипоксии – невелико. Причем конечным продуктом распада глюкозы в этих условиях является лактат, способный накапливаться, что проявляется местным ацидозом и болями в мышцах.
Этапы гликолиза
В гликолизе можно выделить два этапа: первый заключается в поляризации С–С-связи, что приводят после ее разрушения к образованию двух молекул триозофосфатов (ГА-3-Ф и ДГАФ) (Приложение, рис. 3). После изомеризации получившийся ГА-3-Ф подвергается дальнейшим преобразованиям: окислению и субстратному фосфорилированию. Если в митохондриях кислорода достаточно и скорость ЭТЦ адекватна, то НАДН, образовавшийся при окислении глицеральдегид-3-фосфата, отдает восстановительные эквиваленты в процесс биологического окисления. Для преодоления митохондриальных мембран в этом случае используется малат-аспартатный челночный механизм (рис. 3).
  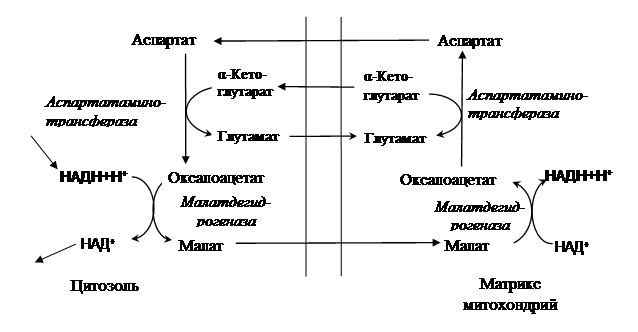 | |||
|
Продукт окисления триозофосфата – ПВК – легко преодолевает мембрану и подвергается окислительному декарбоксилированию до НАДН, ацетил-КоА, СО2. Первое соединение конденсируется с оксалоацетатом, образованным при карбоксилировании ПВК, запуская цикл трикарбоновых кислот. ЦТК – основной поставщик восстановительных эквивалентов для биологического окисления и сопряженного с ним окислительного фосфорилирования. В результате полного окисления 1 молекулы глюкозы может образоваться 38 молекул АТФ:
С6Н12О6 + 6О2 + 38АДФ + 38Фн = 6СО2 + 44 Н2О + 38 АТФ
Гипоксия сказывается на работе малат-аспартатного челночного механизма, накапливается НАДН+Н+, тем самым возникает, во-первых, угроза развития ацидоза, во-вторых, постоянно уменьшается концентрация окисленного НАД+, приводя к торможению скорости гликолиза. Для предотвращения подобных неблагоприятных последствий осуществляется следующая реакция:
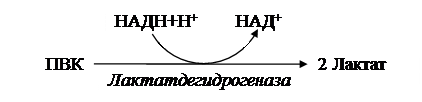
Дальнейшее преобразование лактата возможно только в условиях нормоксии и протекают в печени, куда названная кислота доставляется из мест образования током крови. Для эритроцитов, где отсутствуют митохондрии, характерен только анаэробный гликолиз. В других тканях этот процесс выходит на первое место как источник энергии при различных видах гипоксии (анемиях, легочно-сердечной недостаточности и т. д.). Поступившая в гепатоциты молочная кислота с участием ЛДГ окисляется до пирувата, судьба которой описано выше.
При избытке АТФ в митохондриях ингибируются ферменты ЦТК, что провоцирует накопление цитрата. Выйдя из митохондрий в цитозоль, это соединение под действием АТФ–цитратлиазы распадается на свои исходные компоненты, один из которых – ацетил-КоА может идти или на синтез высших жирных кислот (ВЖК), включающихся позднее в нейтральные жиры, или холестерола (ХС) (в основном, в клетках печени), или же участвовать в реакциях ацетилирования углеводов.
Дата добавления: 2019-12-09; просмотров: 1077;











