Примеры расчёта эквивалента элемента, оксида, основания, соли, кислоты, окислителя, восстановителя.
Эквивалент. Эквивалентная масса. Эквивалентный объём. Закон эквивалентов.
Эквивалентом вещества называется условная частица, в целое число раз меньшая (или равная), чем соответствующая ей структурная или формульная единица вещества (атом, молекула, ион), участвующая в конкретной реакции.
Эквивалентная массаравна отношению молярной массы элемента к его окислительному числу.
Эквивалентная масса оксида равна сумме эквивалентных масс данного элемента и кислорода.
Эквивалентная масса соли равна отношению молярной массы соли к произведению числа атомов металла на его валентность.
Эквивалентная масса основания равна отношению молярной массы основания к числу замещенных гидроксогрупп.
Эквивалентная масса кислоты равна отношению молярной массы кислоты к числу замещенных атомов водорода.

Эквивалентный объём
Объём, который занимает эквивалент вещества С, называется эквивалентным. Он может быть найден делением эквивалентной массы вещества на плотность или делением объема на число эквивалентов этого числа.
Закон эквивалентов.
Согласно закону эквивалентов, вещества взаимодействуют и образуются в эквивалентных количествах.
ВОПРОС 2.
Примеры расчёта эквивалента элемента, оксида, основания, соли, кислоты, окислителя, восстановителя.
- ЭЛЕМЕНТА. Определим эквивалентную массу серы в молекуле серной кислоты. Окислительное число серы в молекуле серной кислоты равно 6. По формуле эквивалентная масса серы равна M/B = 32/6 = 5,33 г/моль.
- ОКСИДА. Определим эквивалентную массу оксида серы. Окислительное число серы в молекуле оксида серы равно 4. По формуле эквивалентная масса серы рана М/В=32/4=8г/моль. Эквивалентная масса оксида по формуле равна ЭS+ЭO=8+8=16г/моль.
- ОСНОВАНИЯ. Определим эквивалентную массу молекулы оксида алюминия. По формуле ЭAl(OH)3=78/3=26г/моль.
- СОЛИ. Определим эквивалентную массу молекулы хлорида алюминия. В молекуле AlCl3 число атомов металла равно 1, а валентность равна 3. По формуле ЭAlCl3=133,5/(1*3)=44,5г/моль.
- КИСЛОТЫ. Определим эквивалентную массу молекулы серной кислоты. Серная кислота двуосновная. По формуле эквивалентная масса серной кислоты равна М/(чз Н)=98/2=49г/моль.
- ОКИСЛИТЕЛЯ.
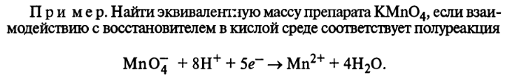
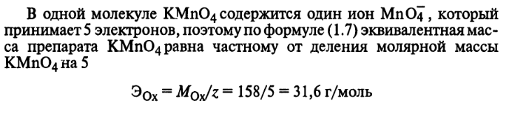
- ВОССТАНОВИТЕЛЯ. Найти эквивалентную массу Zn для данной реакции:
Zn + CuSO4 = ZnSO4 + Cu
Zn -2e → Zn2+-восстановитель
Cu2+ + 2e → Cu-окислитель
ЭZn=M/z=65/2=33
ВОПРОС 3.

Дата добавления: 2016-06-05; просмотров: 12065;











