Люминесцентный анализ
Явление люминесценции относится к оптической спектроскопии.
По определению С.И.Вавилова “люминесценцией тела» в данной спектральной области называют избыток излучения над температурным при условии, что это избыточное излучение обладает конечной длительностью, превышающей период световых колебаний”.
Такое предельно сжатое и точное определение позволяет отличать люминесценцию от других видов излучения: температурного, рассеяния света (Рэлеевского и комбинационного), отражение света, излучения Вавилова-Черенкова и др., которые прекращаются непосредственно вместе с прекращением возбуждения.
Люминесцировать могут вещества, находящиеся в газообразном, жидком и твердом состоянии.
Люминесценцию классифицируют по различным признакам: a) по методу возбуждения и его характеру; б) по длительности послесвечения; в) по внутриатомным процессам при возбуждении.
Классификация люминесценции по методу возбуждения имеет большое практическое значение в реализации методик анализа. Различают фотолюминесценцию – свечение возбуждаемое ультрафиолетовым или видимым излучением; катодолюминесценцию – свечение, возникающее под действием ускоренных электронов; хемилюинесценцию – свечение, сопровождающее ряд химических реакций; рентгено- и радиолюминесценцию – свечение, возбуждаемое рентгеновскими лучами, или быстрыми частицами, такими как продукты радиоактивного распада, космические лучи.
По длительности послесвечения люминесценцию классифицируют на флуоресценцию, т.е. свечение, затухающее после прекращения возбуждения, и фосфоресценцию, свечение, продолжающееся в течение более или менее длительного промежутка времени после прекращения возбуждения.
Квант флуоресценции всегда меньше кванта возбуждения, поглощенного ратомом или молекулой на величину энергии, израсходованной на колебания, а длина волны флуоресценции больше длины волны вызывающего ее ультрафиолетового излучения (правило Стокса). Расстояние на графике между максимумами спектра поглощения и спектра люминисценсии (флуоресценции) называется Стоксовым смещением, причем спектры могут располагаться изолированно или частично перекрываться.
Светопоглощение (445 нм) и флуоресценция (535 нм) раствора рибофлавина (витамина В2).
По характеру внутриатомных процессов при возбуждении люминисценцию классифицируют на спонтанную, вынужденную и рекомбинационную.
При спонтанной люминисценции излучение возникает при возращении предварительно возбужденной молекулы (или атома) в невозбужденное состояние. Излучаемая энергия может быть равна или меньше энергии поглощенного кванта света.


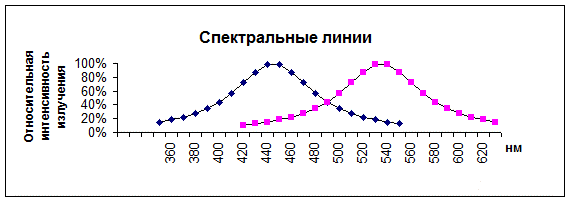
Рис. 11. Стоксово смещение
В процессе вынужденного излучения происходит переход молекулы из возбужденного состояния на промежуточный метастабильный уровень, непосредственный переход с которого на основной (невозбужденный) уровень является запрещенным (маловероятным). На метастабильном уровне молекула находится до тех пор, пока она не будет переведена вынужденным путем на энергетический уровень, переход с которого разрешен.
Длительность этих процессов свечения в значительный мере зависит от температуры. Эти явления, называемые длительным послесвечением или фосфоресценцией, характерны для органических соединений в твердых средах, замороженных и вязких растворах.
Спонтанное и вынужденное излучения, которые наиболее характерны для молекулярных систем, называют молекулярной люминесценсией.
Рекомбинационное свечение характерно тем, что при возбуждении люминесцирующего вещества не происходит перехода молекулы в возбужденное состояние (как при молекулярной люминесценсии), а происходит отрыв электронов от люминесцирующего центра с последующей рекомбинацией электронов и ионизированных центров свечения. Наблюдается рекомбинационное свечение в сложных неорганических веществах, называемых кристаллофосфорами, а также в газах.
Важнейшими характеристиками люминесцирующего вещества являются интенсивность люминесценции, спектры люминесценсии и возбуждения люминесценсии, выход люминесценции, длительность возбужденного состояния, степень поляризации, поляризационный спектр.
Интенсивность люминесценции (J) определяется как суммарное число квантов люминесценции, испускаемое единицей поверхности люминесцирующего вещества в единицу времени.
Для количественного анализа используют зависимость интенсивности люминесценции от концентрации вещества, имеющую линейный диапазон (10-4-10-7 моль/л).
При дальнейшем повышении концентрации выше пороговой сближение молекул вещества приводит к дополнительному расходу энергии на колебательное резонансное взаимодействие, вследствие чего интенсивность люминесценции падает и наступает концентрационное гашение люминесценции. Оно заметно выражено у органических окислителей. Убывание выхода люминесценции описывается соотношением:
η = ηоехр [-K(С-Сo)],
где К – постоянная;
Со – пороговая концентрация, по достижении которой начинается концентрационное гашение.
Различают и другие виды гашения. Гашение электролитами (введение посторонних веществ).
Гашение кислородом особенно сильно проявляется при свечении таких веществ, как нафталин, антрацен и др. полициклические углеводороды.
Повышение температуры люминесцирующих веществ обычно сопровождается уменьшением выхода свечения. Температурное гашение в той или иной степени проявляется у всех люминесцирующих веществ и лимитируется величиной константы скорости (β) безизлучательного перехода, определяемой формулой Больцмана:
β = βоехр (-ЕА/КТ),
где βо – постоянная, не зависящая от температуры;
К – постоянная Больцмана;
ЕА – энергия активации.
Определение концентрации вещества проводится методом построения граидуировочного графика, методом добавок.
Спектр люминесценции определяется как спектральная плотность излучения люминесцирующего вещества.
Φλ = dΦ/dλ; Φhν = dΦ/d(hυ), nhυ= dn/d(hυ),
где Φ – мощность излучения;
n ‑ число квантов, испускаемых в единицу времени,
hυ ‑ энергия испускаемых квантов,
λ ‑ длина волны.
Спектром возбуждения люминесценции называют зависимость интенсивности люминесценции от энергии квантов (или длины волны) возбуждающего света.
Эффективность процессов преобразования поглощенной в молекулах энергии в излучаемую характеризуется выходом люминесценции, под которым понимают отношение энергии (т.е. мощности или интенсивности излучения Φλ), к энергии поглощаемой веществом за то же время (т.е. к мощности поглощения ΦА):
η = Φλ/ΦА
Энергия возбуждающего света и света люминесценции может измеряться либо в энергетических единицах, например, в джоулях, либо в числах квантов.
Понятие квантового выхода используют только в случае оптического возбуждения.
Квантовый выход люминесценции определяется как отношение числа квантов люминесценции, используемых веществом за единицу времени (nл), к числу квантов возбуждающего света, поглощаемых им за то же время (nп):
η кв = nл/ nп
Дата добавления: 2022-02-05; просмотров: 543;











