Соотношение форм адсорбции тяжелых металлов в черноземе
и бурой лесной почве, % от общего количества адсорбированного
металла(составлено автором поданным В.С.Горбатова, 1983)
| Металл | Форма адсорбции, % | ||
| катионо-обменная | связанная с гумусом | связанная с гидроксидами Fe'+ | |
| Чернозем | |||
| Zn | 15,6 | 19,4 | 50,0 |
| Pb | 0,9 | 40,0 | 40,0 |
| Cd | 76,2 | 9,5 | 16,2 |
| Бурая лесная почва | |||
| Zn | 35,5 | 28,0 | 26,7 |
| Pb | 3,7 | 63,9 | 26,2 |
| Cd | 71,1 | 11,1 | 26,7 |
Комплексы металлов с гумусовым веществом и гидроксидами трехвалентного железа весьма устойчивы. Так же устойчивы хемосорбционные образования, имеющие межмолекулярные связи. Наиболее легко переходят в раствор металлы, находящиеся в катионообменной форме. Следовательно, чем большая часть металла адсорбирована органическим веществом, тем более прочно он закреплен в почве. Чем большая часть находится в катионообменной форме, тем легче мобилизуется металл. Из металлов, фигурирующих в табл. 5.10, наиболее подвижен кадмий, наименее — свинец. В органическом веществе металлы настолько прочно связаны, что недоступны растениям. Поэтому растения, произрастающие на осушенных заболоченных почвах, богатых слаборазложенным органическим веществом с высоким содержанием меди, цинка и марганца, часто испытывают физиологический дефицит этих металлов. Катионообменная адсорбция в основном связана с высокодисперсными глинистыми минералами. Наряду с этой формой часть металлов закрепляется в глинистых минералах более прочно, очевидно, проникая в межпакетные пространства кристаллической структуры этих минералов.
Металлы, адсорбированные гумусом, наиболее активно связываются с карбоксильными (СООН) и фенольными (ОН) группами, замещая водород. При этом образуются хелаты, в которых металл входит в анионную часть молекулы органического вещества. Согласно Л.Н.Александровой (1967), металл соединен координационными связями и не проявляет себя как катион. Схема образования комплекса следующая:
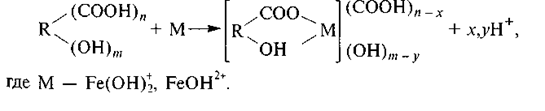
Комплекс может также присоединять металл в обмен на Н+ во внешних функциональных группах:
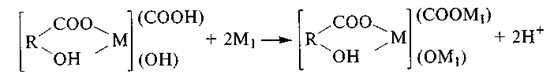
Следовательно, металл может входить как в анионную, так и в катионную часть молекулы гумусовой кислоты. Как отмечалось в разд. 5.2, молекулы гумусовых соединений различаются количеством функциональных групп и степенью сконденсированности «ядра». Поэтому на адсорбцию влияют не только свойства металлов, но и особенности строения гумусовых соединений.
При взаимодействии металлов с гидроксидами Fe3+ возникает связь между ионом металла и двумя группами (ОН)". На схеме представлено возможное взаимодействие металла с рентгеноаморф-ным гидроксидом Fe3+, состав которого отвечает гидрогетиту:
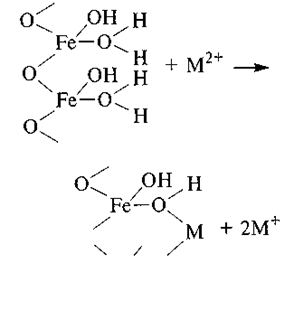
Адсорбция рассеянных элементов и равновесие между твердой и жидкой фазами почвы имеют важное значение для поступления этих элементов в растения. Установлено, что существует два типа поступления элементов в растения (Рубин Б. А., 1974). Первый из них — активный процесс поглощения элемента клеткой против градиента его концентрации, второй — пассивный перенос в направлении градиента. Активное поглощение происходит с затратой энергии и, как правило, селективно, обусловливая биогеохимическую дифференциацию элементов, рассмотренную в разд. 2.3. Пассивное поглощение осуществляется попутно с процессом транспирации.
Тип поступления элементов в растения зависит от концентрации их в почвенном растворе. При низких концентрациях, свойственных рассеянным элементам в условиях геохимического фона, основное значение имеет активное селективное поглощение элементов растениями. В случае аномально высокого обогащения раствора элементом, обычно содержащимся в ничтожном количестве, происходит его пассивное поступление в растения.
Уровни концентрации рассеянных элементов в почвенных растворах имеют исключительно важное значение для нормальной жизнедеятельности растений. В процессе эволюции у растений выработались некоторые механизмы блокирования излишнего количества рассеянных элементов, в первую очередь тяжелых металлов. В.Б.Ильин и М.Д.Степанова (1980) предположили, что рассеянные металлы в той или иной мере могут задерживаться на периферии корня в зоне пояска Каспари. Возможно, имеются физиологические механизмы, предохраняющие репродуктивные органы. Однако защитное действие растений весьма ограничено, а для некоторых элементов, например цинка, — отсутствует (Бан-сал Н. А. и др., 1982). Необходимая для растений низкая концентрация тяжелых металлов главным образом обеспечивается равновесиями между твердой и жидкой фазами почвы.
Концентрация рассеянных элементов в почвенных растворах является важным фактором нормальной жизнедеятельности не только высших растений, но и почвенной микробиоты. Имеющиеся данные свидетельствуют, что почвенные микроорганизмы адаптированы к неодинаковым уровням концентрации цинка, меди, свинца, кадмия, молибдена, кобальта и других рассеянных элементов. На этом основании В. В. Ковальский (1974) предположил, что в почвах существуют разные экологические типы одного и того же вида микроорганизмов, приспособленные к определенным уровням содержания рассеянных элементов.
С.В.Летунова (1978) изучила микроорганизмы в почвах Сум-сарского свинцово-цинкового месторождения и установила, что наиболее устойчивы к избытку тяжелых металлов грибы, наименее — бактерии. В то же время наибольшее содержание цинка обнаружено в сухом веществе спорообразующих бактерий (5154,1 мг/кг сухого вещества бактерий), актиномицетов (до 483,7 мг/кг), грибов (251,0 мг/кг) и неспороносных бактерий (до 118,0 мг/кг). Максимальное содержание свинца также относится к спорообразующим бактериям (1466,7 мг/кг), затем следуют неспорообразу-ющие бактерии (до 246 мг/кг), актиномицеты (101,7 мг/кг) и грибы (96,4 мг/кг).
Способность к аккумуляции металлов, по-видимому, является характерной биогеохимической особенностью почвенных бактерий. Возможно, они вырабатывают ферменты для трансформации водорастворимых соединений металлов в неактивные формы внутри клеток. В результате деятельности бактерий образованы крупные месторождения руд железа, марганца, меди, ванадия, урана и других металлов. Способность бактерий аккумулировать металлы использована при разработке технологий микробиологического извлечения металлов из бедных руд и микробиологической очистки сточных вод.
Несмотря на способность к аккумуляции металлов, микроорганизмы, населяющие почвы с нормальной, невысокой концентрацией металлов, чувствительно реагируют на возрастание их концентрации. Это проявляется в подавлении биогеохимической деятельности некоторых групп организмов, в частности фиксаторов атмосферного азота.
Опыты С. В.Летуновой (1978) на почвенных экстрактах и непосредственное микробиологическое изучение микроорганизмов почв показали, что азотфиксирующие бактерии Azotobacter chroococum из почв разных районов приспособлены к разным концентрациям меди. Azotobacter из почв Подмосковья существует в условиях низкой концентрации меди и молибдена, а из почв Узбекистана — при более высокой. Внесение дополнительных количеств меди и молибдена к экстракту из почвы Подмосковья подавляло рост и фиксацию им азота штамма Azotobacter, в то время как для Azotobacter из почвы Узбекистана эти концентрации не вызывали отрицательной реакции.
М.М.Умаров с коллегами (1980) установили, что наиболее сильно подавляют азотфиксирующую активность почвы избыточные количества кадмия, в меньшей степени — меди, наименее заметно влияние свинца. Возможно, что степень токсичного воздействия металлов связана с прочностью их адсорбции твердой фазой почвы, которая соответствует ряду Рb > Сu > Cd. Эффект подавления азотфиксирующей деятельности почв избыточными дозами металлов, к которым микроорганизмы не адаптированы, можно использовать для оценки интенсивности техногенного загрязнения почв.
По причине значительной сорбционной емкости и действию рассмотренных равновесий почва обладает замечательной способностью связывать массы тяжелых металлов и поддерживать их концентрацию в почвенном растворе на низком уровне, обеспечивающем селективное поглощение необходимого растениям количества металлов. В то же время при недостатке металла благодаря имеющемуся равновесию между твердой и жидкой фазами почва способна выделять этот металл в раствор.
Образование комплексных соединений металлов с органическим веществом почвы способствует выведению излишних масс металлов из миграционных циклов на длительное время. Прочность фиксации разных металлов в органическом веществе почв , неодинакова. Наиболее прочно закрепляется ртуть, прочно связывается свинец, менее прочно — медь, еще менее — цинк и кадмий. Поглощая и связывая избыточные массы рассеянных элементов, поступающие на поверхность суши в активной растворимой форме, педосфера выполняет функцию регулятора масс рассеянных элементов, поступающих в миграционные циклы. В процессах регулирования важную роль играют почвенное органическое вещество и гидроксиды железа.
Изложенные в этой главе данные позволяют рассматривать почву не только как основной источник производства продуктов питания для населения земного шара, но и как важнейшее звено глобальной системы всей биосферы. Ответственное значение почвы связано с ее ролью регулятора многих биогеохимических циклов. В почве систематически консервируется значительная масса синтезированного высшими растениями органического вещества, что обеспечивает нахождение в атмосфере свободного кислорода. В то же время в почве продуцируется углекислый газ, необходимый для непрерывного фотосинтеза и воспроизводства живого вещества. В почве осуществляется преобразование инертного молекулярного азота в формы, доступные для включения в биологический круговорот. В почве происходят сложные процессы трансформации соединений элементов-биогенов, в первую очередь серы и фосфора. В настоящее время в связи с интенсивной техногенной эмиссией металлов отчетливо выявляется роль педосферы как регулятора миграционных потоков масс тяжелых металлов и других элементов с переменной валентностью. Учитывая столь важную роль уникального биокосного образования, каким является педосфера, проблема охраны и рационального использования почв приобретает особо актуальное значение.
Рекомендуемая литература
Бирюкова О.Н., Орлов Д. С. Органические соединения и оксиды углерода в почве и биосфере // Почвоведение. — 2001. — № 2. — С. 180—191.
Вернадский В. И. О значении почвенной атмосферы и ее биогенной структуры // Почвоведение. — 1944. — № 4/5. — С. 137—143.
Глазовская М.А. Геохимия природных и техногенных ландшафтов СССР. - М.: Высш. шк., 1988. - 328 с.
Взаимодействие почвы с атмосферой / Г.А.Заварзин, Д.Г.Звягинцев, Л.О.Карпачевский и др. — М.: Изд-во МГУ, 1985.
Кабата-Пендиас И., Пендиас X. Микроэлементы в почвах и растениях. — М.: Мир, 1989. -439с.
Микроэлементы в почвах Советского Союза / Под ред. В. А. Ковды и Н.Г.Зырина. - М.: Изд-во МГУ, 1937. - 281 с.
Микроэлементы в почвах СССР / Под ред. Н. Г. Зырина и Г. Д. Белици-ной. - М.: Изд-во МГУ, 1981. - 252 с.
Орлов Д. С. Гумусовые кислоты почв. — М.: Изд-во МГУ, 1974. — 333с.
Химия тяжелых металлов, мышьяка и молибдена в почвах / Под ред. Н.Г.Зырина и Л.К.Садовниковой. — М.: Изд-во МГУ, 1985. — 208 с.
Контрольные вопросы
1. Дайте оценку педосфере как глобальному биогеохимическому фильтру газов, выделяемых в атмосферу.
2. Рассмотрите внутрипочвенные биогеохимические циклы газов, осуществляющиеся бактериальными системами.
3. В каких почвах продуцируется наибольшее количество СО2? В каких почвах, связанных системой геохимического сопряжения, углекислот-ное дыхание почвы подавляется?
4. Изложите представления о двух главных группах специфических органических образований почв.
5. Какие две противоположно направленные функции выполняет гумус почвы по отношению к рассеянным металлам?
6. Какова общая направленность биогеохимической трансформации минерального вещества почвы?
7. Назовите главные закономерности перераспределения тяжелых металлов при биогеохимической трансформации минерального вещества почвы.
8. Изложите представления о минералого-геохимических провинциях педосферы. Приведите примеры провинций, назовите их отличительные особенности.
9. Каков механизм фиксации избыточных масс тяжелых металлов и близких им поливалентных элементов в почвах?
10. Рассмотрите роль бактерий в процессах аккумуляции тяжелых металлов.
Дата добавления: 2021-11-16; просмотров: 484;











