Развитие представлений о строении атома. Опыт Резерфорда. Модель атома по Резерфорду. Постулаты Бора. Боровская теория атома водорода.
Представление об атомах как неделимых мельчайших частицах вещества возникло еще в античные времена, но только в XVIII веке трудами А. Лавуазье, М. В. Ломоносова и других ученых была доказана реальность существования атомов. Но вопрос об их внутреннем устройстве даже не возникал, и атомы по-прежнему считались неделимыми частицами. В XIX веке изучение атомистического строения вещества существенно продвинулось вперед. В 1833 году при исследовании явления электролиза М. Фарадей установил, что ток в растворе электролита это упорядоченное движение заряженных частиц – ионов. Фарадей определил минимальный заряд иона, который был назван элементарным электрическим зарядом. Его приближенное значение оказалось равным e = 1,60·10–19 Кл.
На основании исследований Фарадея можно было сделать вывод о существовании внутри атомов электрических зарядов.
Большую роль в развитии атомистической теории сыграл выдающийся русский химик Д. И. Менделеев, разработавший в 1869 году периодическую систему элементов, в которой впервые был поставлен вопрос о единой природе атомов.
Важным свидетельством сложной структуры атомов явились спектроскопические исследования, которые привели к открытию линейчатых спектров атомов. В начале XIX века были открыты дискретные спектральные линии в излучении атомов водорода в видимой части спектра. Впоследствии, в 1885 г. И. Бальмером были установлены математические закономерности, связывающие длины волн этих линий.
В 1896 году А. Беккерель обнаружил явление испускания атомами невидимых проникающих излучений, названное радиоактивностью. В последующие годы явление радиоактивности изучалось многими учеными (М. Склодовская-Кюри, П. Кюри, Э. Резерфорд и др.). Было обнаружено, что атомы радиоактивных веществ испускают три вида излучений различной физической природы (альфа-, бета- и гамма-лучи). Альфа-лучи оказались потоком ионов гелия, бета-лучи – потоком электронов, а гамма-лучи – потоком квантов жесткого рентгеновского излучения.
В 1897 году Дж. Томсон открыл электрон и измерил отношение e / m заряда электрона к массе. Опыты Томсона подтвердили вывод о том, что электроны входят в состав атомов.
Таким образом, на основании всех известных к началу XX века экспериментальных фактов можно было сделать вывод о том, что атомы вещества имеют сложное внутреннее строение. Они представляют собой электронейтральные системы, причем носителями отрицательного заряда атомов являются легкие электроны, масса которых составляет лишь малую долю массы атомов. Основная часть массы атомов связана с положительным зарядом.
Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах. Резерфорд предложил применить зондирование атома с помощью α-частиц, которые возникают при радиоактивном распаде радия и некоторых других элементов. Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду. В своих опытах Резерфорд использовал α-частицы с кинетической энергией около 5 МэВ (скорость таких частиц очень велика – порядка 107 м/с, но все же значительно меньше скорости света). α-частицы – это полностью ионизированные атомы гелия. Они были открыты Резерфордом в 1899 году при изучении явления радиоактивности. Этими частицами Резерфорд бомбардировал атомы тяжелых элементов (золото, серебро, медь и др.). Электроны, входящие в состав атомов, вследствие малой массы не могут заметно изменить траекторию α-частицы. Рассеяние, то есть изменение направления движения α-частиц, может вызвать только тяжелая положительно заряженная часть атома. Схема опыта Резерфорда представлена на рис. 6.1.2.
|
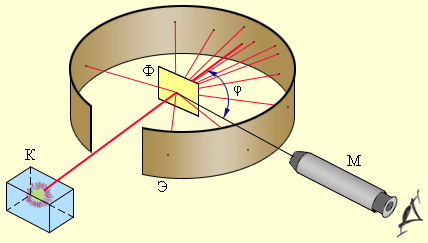
| Рисунок 6.1.2. Схема опыта Резерфорда по рассеянию α-частиц. K – свинцовый контейнер с радиоактивным веществом, Э – экран, покрытый сернистым цинком, Ф – золотая фольга, M – микроскоп |
От радиоактивного источника, заключенного в свинцовый контейнер, α-частицы направлялись на тонкую металлическую фольгу. Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались глазом с помощью микроскопа. Наблюдения рассеянных α-частиц в опыте Резерфорда можно было проводить под различными углами φ к первоначальному направлению пучка. Было обнаружено, что большинство α-частиц проходит через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные углы, превышающие 30°. Очень редкие α-частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к 180°.
Этот результат был совершенно неожиданным даже для Резерфорда. Его представления находил bcm в резком противоречии с моделью атома Томсона, согласно которой положительный заряд распределен по всему объему атома. При таком распределении положительный заряд не может создать сильное электрическое поле, способное отбросить α-частицы назад. Электрическое поле однородного заряженного шара максимально на его поверхности и убывает до нуля по мере приближения к центру шара. Если бы радиус шара, в котором сосредоточен весь положительный заряд атома, уменьшился в n раз, то максимальная сила отталкивания, действующая на α-частицу, по закону Кулона возросла бы в n2 раз. Следовательно, при достаточно большом значении n α-частицы могли бы испытать рассеяние на большие углы вплоть до 180°. Эти соображения привели Резерфорда к выводу, что атом почти пустой, и весь его положительный заряд сосредоточен в малом объеме. Эту часть атома Резерфорд назвал атомным ядром. Так возникла ядерная модель атома. Рис. 6.1.3 иллюстрирует рассеяние α-частицы в атоме Томсона и в атоме Резерфорда.
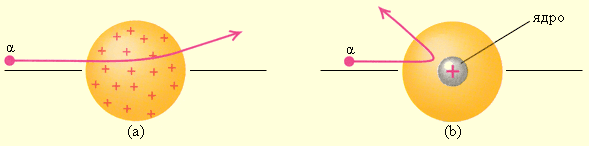
|
| Рисунок 6.1.3. Рассеяние α-частицы в атоме Томсона (a) и в атоме Резерфорда (b) |
Таким образом, опыты Резерфорда и его сотрудников привели к выводу, что в центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10–14–10–15 м. Это ядро занимает только 10–12 часть полного объема атома, но содержит весь положительный заряд и не менее 99,95 % его массы. Веществу, составляющему ядро атома, следовало приписать колоссальную плотность порядка ρ ≈ 1015 г/см3. Заряд ядра должен быть равен суммарному заряду всех электронов, входящих в состав атома. Впоследствии удалось установить, что если заряд электрона принять за единицу, то заряд ядра в точности равен номеру данного элемента в таблице Менделеева.
Радикальные выводы о строении атома, следовавшие из опытов Резерфорда, заставляли многих ученых сомневаться в их справедливости. Не был исключением и сам Резерфорд, опубликовавший результаты своих исследований только в 1911 г. через два года после выполнения первых экспериментов. Опираясь на классические представления о движении микрочастиц, Резерфорд предложил планетарную модель атома. Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, под действием кулоновских сил со стороны ядра вращаются электроны (рис. 6.1.4). Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
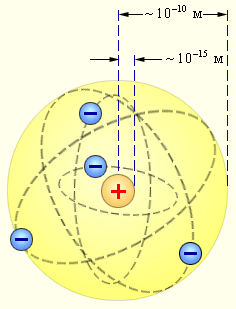
| Рисунок 6.1.4. Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов |
Датский физик Нильс Бор (1885–1962) в 1913 г. создал первую квантовую теорию атома, связав в единое целое эмпирические закономерности линейчатых спектров водорода, ядерную модель атома Резерфорда и квантовый характер излучения и поглощения света.
В основу своей теории Бор положил три постулата, по поводу которых американский физик Л. Купер заметил: «Конечно, было несколько самонадеянно выдвигать предложения, противоречащие электродинамике Максвелла и механике Ньютона, но Бор был молод».
Первый постулат (постулат стационарных состояний): в атоме электроны могут двигаться только по определенным, так называемым разрешенным, или стационарным, круговым орбитам, на которых они, несмотря на наличие у них ускорения, не излучают электромагнитных волн (поэтому эти орбиты названы стационарными). Электрон на каждой стационарной орбите обладает определенной энергией En.
Второй постулат (правило частот): атом излучает или поглощает квант электромагнитной энергии при переходе электрона с одной стационарной орбиты на другую:
hv = E1 – E2,
где E1 и E2 – энергия электрона соответственно до и после перехода.
При E1 > E2 происходит излучение кванта (переход атома из одного состояния с большей энергией в состояние с меньшей энергией, то есть переход электрона с любой дальней на любую ближнюю от ядра орбиту); при E1 < E2 – поглощение кванта (переход атома в состояние с большей энергией, то есть переход электрона на более удаленную от ядра орбиту).
Будучи уверенным, что постоянная Планка должна играть основную роль в теории атома, Бор ввел третий постулат (правило квантования): на стационарных орбитах момент импульса электрона
Ln= menrn
menrn = nh, n = 1, 2, 3, …,
где = 1,05 · 10-34 е = 9,1 · 10-31 кг – масса электрона; rп n – скорость электрона на этой орбите.
Корпускулярно-волновой дуализм. Гипотеза де Бройля. Дифракция электронов. Волновые свойства вещества. Корпускулярно-волновая природа микрочастиц. Соотношение неопределенностей Гейзенберга.
Корпускулярно-волновой дуализм (от лат. dualis — двойственный) — является важнейшим универсальным свойством природы, которое состоит в том, что каждому микрообъекту присущи сразу и корпускулярные, и волновые характеристики.
Например, электрон, нейтрон, фотон в одних условиях ведут себя как частицы, которые двигаются по классическим траекториями имеют определенную энергию и импульс, а в других — обнаруживают свою волновую природу, которая характерна для явлений интерференции и дифракции частиц.
Ранее всего корпускулярно-волновой дуализм был определен для света. Распространение света как потока фотонов и квантовый характер взаимодействия света с веществом подтверждаются многочисленными экспериментами. Но ряд оптических явлений (интерференция, поляризация, дифракция) неоспоримо говорят о волновых свойствах света.
Классическая физика всегда отчетливо разделяла объекты, которые обладают волновой природой (например, свет и звук), и объекты, которые обладают дискретной корпускулярной структурой (например, системы материальных точек). Одним из самых важных достижений современной физики является убеждение в ложности противопоставления волновых и квантовых свойств света. Если рассматривать свет как поток фотонов, а фотоны — как кванты электромагнитного излучения, которые обладают в одно время и волновыми, и корпускулярными свойствами, современная физика может объединить антагонистичные теории — волновую и корпускулярную. В результате создалось представление о корпускулярно-волновом дуализме, которое лежит в основе современной физики (корпускулярно-волновой дуализм оказывается первичным принципом квантовой механики и квантовой теории поля).
Квант света — не является ни волной и ни корпускулой в понимании Ньютона. Фотоны — это специфические микрочастицы, у которых энергия и импульс (в отличие от обычных материальных точек) выражаются при помощи материальных характеристик — частоту и длину волны.
В 1924 г. французским ученым Луи де Бройлем была озвучена гипотеза о том, что корпускулярно-волновой дуализм присущ каждому без исключения виду материи — электронам, протонам, атомам, причем количественные соотношения между волновыми и корпускулярными свойствами частиц те же, что и установленные раньше для фотонов. Т.е., если частица обладает энергией Е и импульсом, абсолютное значение которого равняется p, значит, с этой частицей связана волна частотой v=E/h и длиной
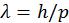 ,
,
где h — в данном случае является постоянной Планка.
Это знаменитая формула де Бройля — одна из важнейших формул в физике микромира.
Стоит заметить, что длина волны де Бройля уменьшается с увеличением массы частицы m и ее скорости v: для частиц с 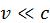 правдиво
правдиво  .
.
Таким образом, частице массой 1 г, которая движется со скоростью 1 м/с, соответствует волна де Бройля длиной  , настолько маленькой, что это невозможно наблюдать. Поэтому волновые свойства являются несущественными в механике макроскопических тел, что полностью согласуется с принципом соответствия.
, настолько маленькой, что это невозможно наблюдать. Поэтому волновые свойства являются несущественными в механике макроскопических тел, что полностью согласуется с принципом соответствия.
В 20-х годах XX столетия было установлено, что любая частица имеет корпускулярно-волновую природу. Согласно теории Л. де Бройля (1924 г.), каждой частице с импульсом 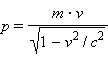 соответствует волновой процесс с длиной волны λ, т.е. λ = h / p. Чем меньше масса частицы, тем больше длина волны. Для элементарных частиц В. Гейзенберг сформулировал принцип неопределенности, согласно которому невозможно одновременно определить положение частицы в пространстве и ее импульс. Следовательно, нельзя рассчитать траекторию движения электрона в поле ядра, можно лишь оценить вероятность его нахождения в атоме с помощью волновой функции ψ, которая заменяет классическое понятие траектории. Волновая функция ψ характеризует амплитуду волны в зависимости от координат электрона, а ее квадрат ψ2 определяет пространственное распределение электрона в атоме. В наиболее простом варианте волновая функция зависит от трех пространственных координат и дает возможность определить вероятность нахождения электрона в атомном пространстве или его орбиталь. Таким образом, атомная орбиталь (АО) – область атомного пространства, в котором вероятность нахождения электрона наибольшая.
соответствует волновой процесс с длиной волны λ, т.е. λ = h / p. Чем меньше масса частицы, тем больше длина волны. Для элементарных частиц В. Гейзенберг сформулировал принцип неопределенности, согласно которому невозможно одновременно определить положение частицы в пространстве и ее импульс. Следовательно, нельзя рассчитать траекторию движения электрона в поле ядра, можно лишь оценить вероятность его нахождения в атоме с помощью волновой функции ψ, которая заменяет классическое понятие траектории. Волновая функция ψ характеризует амплитуду волны в зависимости от координат электрона, а ее квадрат ψ2 определяет пространственное распределение электрона в атоме. В наиболее простом варианте волновая функция зависит от трех пространственных координат и дает возможность определить вероятность нахождения электрона в атомном пространстве или его орбиталь. Таким образом, атомная орбиталь (АО) – область атомного пространства, в котором вероятность нахождения электрона наибольшая.
Волновые функции получаются при решении основополагающего соотношения волновой механики – уравнения Шредингера. Точное решение существует для атома водорода или водородоподобных ионов, для многоэлектронных систем используются различные приближения. Поверхность, ограничивающая 90–95 % вероятности нахождения электрона или электронной плотности, называют граничной. Атомная орбиталь и плотность электронного облака имеют одинаковую граничную поверхность (форму) и одинаковую пространственную ориентацию. Атомные орбитали электрона, их энергия и направление в пространстве зависят от четырех параметров – квантовых чисел.
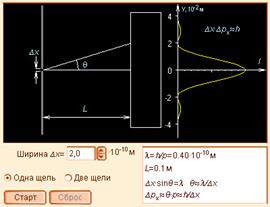
|
| Модель 2.1. Принцип неопределенности |
Уравнение Шредингера. Волновая функция и ее статистический смысл. Применение уравнения Шредингера: частица в одномерной бесконечно глубокой потенциальной яме; прохождение частиц через потенциальный барьер.
Дата добавления: 2017-11-21; просмотров: 4255;











