Металлическая связь
Эта связь реализуется в металлах и сплавах. Атомы большинства металлов имеют на своём внешнем энергетическом уровне небольшое число валентных электронов 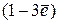 , поэтому им легче отдать их, чем принять от другого элемента. В соответствии с современными представлениями металл имеет кристаллическую решетку, в узлах которой располагаются положительно заряженные ионы или нейтральные атомы, связанные между собой свободными валентными электронами.
, поэтому им легче отдать их, чем принять от другого элемента. В соответствии с современными представлениями металл имеет кристаллическую решетку, в узлах которой располагаются положительно заряженные ионы или нейтральные атомы, связанные между собой свободными валентными электронами.
Следовательно, кристаллическую решетку металла схематически можно изобразить в виде равновесия:
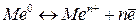
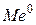 и
и 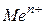 – нейтральные атомы и положительно заряженные ионы находятся в узлах кристаллической решетки;
– нейтральные атомы и положительно заряженные ионы находятся в узлах кристаллической решетки;
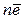 – свободно перемещающиеся по всему объёму кристалла валентные электроны.
– свободно перемещающиеся по всему объёму кристалла валентные электроны.
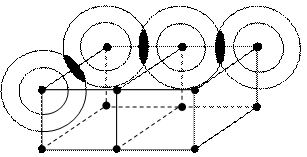 |
Возможность свободного перемещения валентных электронов иллюстрирует рисунок 4.9.
Рисунок 4.9 – Перекрывание электронных облаков атомов в металле
Благодаря обобществлению свободных электронов между всеми атомами металла, металлы обладают высокой прочностью и высокой электропроводностью.
Дата добавления: 2016-06-05; просмотров: 1258;











