ЗАДАЧИ ПО ДИАГРАММАМ СОСТОЯНИЯ ДВОЙНЫХ СПЛАВОВ
Диаграммы состояния показывают в условиях равновесия фазовый состав сплава в зависимости от температуры и концентрации и позволяют качественно характеризовать многие физико-химические, механические и технологические свойства сплавов.
Существенно, что анализ диаграмм состояния позволяет, кроме того, решать важные инженерные задачи; на основании диаграмм можно определить, какие именно сплавы, и в каком направлении изменяют свою структуру, и многие свойства при переходе к неравновесному состоянию, зависящему от реальных условий литья, обработки давлением и специально выполняемой термической обработки.
В приводимых ниже задачах показаны методические пути и возможность решения этих вопросов на основании рассмотрения превращений, протекающих в сплавах и указанных в диаграммах состояния. В связи с этим в задачах приведены преимущественно те диаграммы состояния, которые характеризуют фазовый состав сплавов, близких к широко применяемым в технике.
Решение проводимых ниже задач включает выполнение следующих заданий:
1. Начертить заданную диаграмму состояния (как указано на рис. 1).
2. В каждой области диаграммы указать структуры, образующиеся в сплавах данной системы в состоянии равновесия.
3. Указать на диаграмме состояния заданные в задаче сплавы и провести соответствующие и провести соответствующие им вертикальные линии (рис.1).
4. Построить в координатах температура – время кривые охлаждения сплавов.
5. Построить схему кристаллизации заданных сплавов, показать графически структуры, образующиеся в процессе кристаллизации, а также превращения, протекающие в сплавах при охлаждении.
6. Дать характеристику состояния заданных сплавов при температурах, указанных в задаче.
7. Ответить в результате сделанного анализа превращений на основной вопрос задачи о структуре, свойствах, обработке и области применения заданных в ней сплавов.

Таблица 1
Характеристика состояния сплавов при различных температурах
| Сплав | Темпера-тура, 0С | Фазовый или структурный состав сплава | Расчет количества фазовых и структурных составляющих по правилу фаз |
| I II II III III | Однородный твердый раствор на основе α-железа Кристаллы твердого α-раствора концентрации 0,9% Р (точка а) и жидкая фаза, содержащая 4,6% Р (точка в) Основная структура твердого раствора концентрации 1,2% Р (точка д) и небольшое количество вторичных кристаллов химического соединения Fe3P (магнитное) Кристаллы химического соединения Fe2P и жидкая фаза, по концентрации соответствующая точке и -16% Р Смесь двух химических соединений Fe3P и Fe2P | Количество жидкости (Qж): Qж = аб 100 = 1,1· 100 ав 3,7 = 30% Количество α-фазы (Qα): Qα = зж 100 = 13,5· 100 дж 14,5 = 94% Количество Fe3P (Q Fe3P): Q Fe3P = 100 - 94= 6% Qж = кл 100 = 4· 100 = ил 5 =80% Q Fe3P = но100 = 4· 100 мо 5,5 = 73% Q Fe2P =27% |
ЗАДАЧИ
№ 1. Разобрать диаграмму состояния Fe-P в части, ограниченной областью Fe —Fe2P, и процессы превращения в сплавах I, II и III, содержащих: I — 0,05, II — 2, 111 — 17% Р.
Определить фазовый состав и количественное соотношение фаз: сплава I при 20° С, сплава II при 100 и 1350° С, сплава III при 20 и 1200° С.
Указать, какие отклонения в структуре при первичной кристаллизации сплавов этой системы можно ожидать в условиях ускоренного охлаждения.
Решение задачи № 1.
Решение по первым вопросам задачи дано в диаграммах и таблице на рис. 1. Ответ на последний вопрос приведен ниже.
Разбираемая диаграмма состояния является равновесной. Между тем некоторые превращения в сплавах протекают настолько медленно, что практически не заканчиваются полностью даже при очень длительном охлаждении. К таким превращениям относится, в частности, образование по перитектической реакции твердых растворов или неустойчивых химических соединений.
Изменение скорости охлаждения смещает отдельные точки и линии превращений на диаграмме, причем величина смещения зависит от степени отклонения сплава от равновесного состояния. Поэтому структуры, наблюдаемые в промышленных сплавах, могут отличаться от ожидаемых на основании равновесной диаграммы состояния.
Для полной характеристики данной системы следовало бы иметь не только плоскостную равновесную диаграмму в координатах температура—концентрация, но и пространственную диаграмму в координатах температура—концентрация—время, которая показывала бы переход от неравновесного к равновесному состоянию. Однако такая диаграмма была бы очень сложной. Рассмотрение равновесной диаграммы на основе более подробного разбора процессов, протекающих в сплавах, и закономерностей, которым эти процессы подчиняются, позволяет с достаточной вероятностью указать характер превращений при ускоренном охлаждении (особенно при первичной кристаллизации). Рассмотрим с этой точки зрения процесс кристаллизации.
Сплав I, согласно диаграмме, кристаллизуется с образованием однородной структуры α-твердого раствора. Затвердевание его протекает между 1520 и 1500° С при изменении концентрации жидкости и выделяющейся твердой фазы между сотыми долями процента и 1,8% Р. Следовательно, сплав подвержен ликвации.
При ускоренном охлаждении состав кристаллов твердого раствора не будет однородным, однако концентрация их не превысит предела растворимости фосфора в железе α (β). Поэтому сплав после
затвердевания в реальных условиях охлаждения не будет отличаться по фазовому составу от равновесного. Однако отдельные кристаллы (зерна) сплава по химическому составу будут неоднородными.
Получающаяся неоднородность химического состава кристаллов твердого раствора называется внутрикристаллической или внутридендритной ликвацией и соответственно влиянию фосфора на свойства железа дополнительно снижает ударную вязкость и пластичность, особенно при низких температурах. Это снижение тем значительнее, чем выше концентрация фосфора. Поэтому в высококачественной стали содержание фосфора ограничивается до 0,02— 0,03%, а в качественной — до 0,04—0,05%.
Сплав II с 2% Р в равновесном состоянии после затвердевания должен, как и сплав I, иметь структуру однородного твердого раствора. Однако и у этого сплава наблюдается большое расхождение между линиями ликвидуса и солидуса по температуре, а также по концентрации; следовательно, он должен быть склонен к ликвации, подобно сплаву I (c 0,05% P). Затвердевание сплава II начинается при температуре около 1500° С и заканчивается при температуре около 1200° С. Уже при 1350° С, как это видно из диаграммы и из таблицы (рис. 1), жидкая фаза (точка б) содержит примерно 4,6% Р, т. е. в полтора раза больше, чем может быть растворено в железе в твердом состоянии при эвтектической температуре. Предел растворимости фосфора в железе (точка В), как показывает диаграмма (см. рис. 1), равен 2,6% Р. К концу затвердевания состав жидкой фазы будет соответствовать точке с, что соответствует примерно 7,5% Р. При ускоренном охлаждении не успевает пройти полностью диффузия, выравнивающая состав сплава. Поэтому последняя «порция» жидкой фазы состава с затвердевает подобно до-эвтектическому сплаву такой же концентрации, т. е. образуя некоторое количество кристаллов α-твердого раствора и эвтектическую смесь, состоящую из кристаллов а и химического соединения Fe3P.
Таким образом, при ускоренном охлаждении в сплаве II наряду с кристаллами α-твердого раствора переменной концентрации может присутствовать некоторое количество эвтектики. Наличие эвтектики с низкой температурой плавления улучшает жидкотекучесть. В то же время эвтектика вследствие повышенной хрупкости ухудшает механические свойства.
Сплав III в процессе затвердевания, кроме химического соединения Fe2P, образует еще неустойчивое при высоких температурах хи-
мическое соединение Fe3P. Поэтому сплав III при нормальной температуре, как следует из диаграммы состояния, должен состоять из смеси кристаллов двух химических соединений Fe3P + Fe2P. Количество каждого из этих соединений в сплаве III определяется по правилу отрезков и составляет 73% Fe3P и 27% Fe2P (табл. 1).
Образование химического соединения Fe3P происходит по реакции между жидкой фазой состава с и химическим соединением Fe2P, т. е. по типу перитектической реакции, протекающей, как известно, на поверхности раздела фаз.
В условиях ускоренного охлаждения такие реакции не идут до конца, и сплав будет содержать значительно меньшее количество соединения Fe3P, чем это следует из диаграммы, или даже вовсе не содержит его. Более того, в некоторых случаях последние порции жидкой фазы, содержащие больше железа, чем это соответствует составу химического соединения Fe3P (например, точка д), могут при затвердевании образовать некоторое количество эвтектики, состоящей из мелкодисперсной смеси Fe3P (Fe2P) и α-твердого раствора. Таким образом, и сплав III при некоторых условиях (ускоренное охлаждение) может иметь структуру, значительно отличающуюся от ожидаемой по диаграмме состояния.
Магнитные превращения α-твердого раствора и Fe3P, протекающие в этих сплавах и показанные пунктирными линиями на диаграмме (рис. 1), не вызывают изменений в структуре.
№ 2. Мартенситно-стареющие сплавы на основе системы железо—никель приобретают при закалке мартенситную структуру даже при замедленном охлаждении, если они имеют определенное содержание никеля.
Определить, при какой концентрации никеля: 5; 10 или 20% превращение γ→α протекает как мартенситное, а не как диффузионное.
Для решения задачи учесть температуры превращения и по диаграмме сплавов системы Fe—Ni (рис. 2) рассмотреть процессы превращений в указанных сплавах и количественное соотношение фаз в них при 200° С.
№ 3. Термическая обработка некоторых высокохромистых сталей с пониженным содержанием углерода существенно улучшает их вязкость и пластичность. Указать, для каких сплавов системы Fe—Сr применима такая обработка, в чем она заключается, и какое влияние она оказывает на структуру такой стали.
Для решения задачи рассмотреть процессы превращений в сплавах с 10, 20 и 30% Сr (рис. 3) и указать их фазовый состав и количественное соотношение фаз: для сплава I при 20 и 10000C, а для сплавов с 20 и 30% Сr при 20° С.
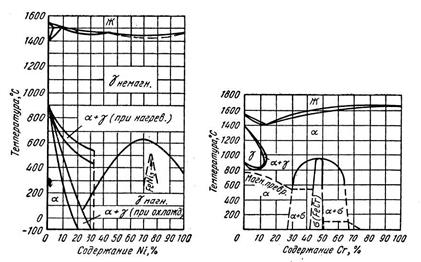
Рис.2. Диаграмма состояния сплавов Fe-Ni Рис.3. Диаграмма состояния
сплавов Fe-Cr
№ 4. Сплавы хрома с железом приобретают стойкость против эрозии, если содержание хрома составляет 12%; при еще большем повышении содержания хрома: до 25% и выше стойкость против коррозии дополнительно возрастает (см. рис. 3). Однако в этом случае снижается пластичность сплавов, что затрудняет использование для ряда назначений.
Объяснить причины указанного влияния хрома на механические свойства. Для этой цели рассмотреть процессы превращений и структуру сплавов с 12, 25 и 35% Сr. Определить фазовый состав сплава I при 1000 и 20° С, сплавов II и III при 20° С.
№ 5. Сплавы системы Fe—W (см. рис. 4) определенной концентрации получают очень высокую твердость (HRC 63—65) и высокую коэрцитивную силу в результате дисперсионного твердения при отпуске 600—650° С.
Указать: а) примерное содержание вольфрама в таких сплавах; б) термическую обработку, которая должна предшествовать отпус-
ку, и какую структуру она создает в сплаве; в) причины возрастания твердости и коэрцитивной силы при отпуске. Для решения задачи рассмотреть процессы превращений в сплавах с 1; 10 и 45% W и указать их фазовый состав и количественное соотношение фаз при 400° С.
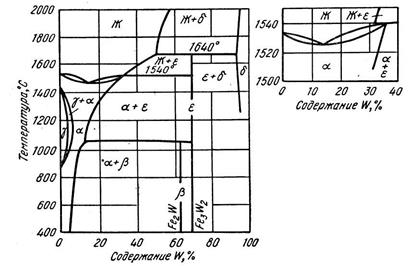
Рис.4. Диаграмма состояния сплавов Fe-W
№ 6. В некоторых сплавах системы Fe—W протекают превращения в твердом состоянии. Развитие превращений зависит от термической обработки и может сильно изменять механические свойства сплавов.
Рассмотреть превращения в сплавах с 2, 15 и 75% W (см. рис. 4).
Определить фазовый состав и количественное соотношение фаз сплавов: I при 1200° С, II при 400° С и сплава III при 1400° С. Указать, в каких сплавах из числа заданных можно изменить структуру и свойства путем термической обработки и какой именно, и объяснить, в какой степени (качественно) она может изменить свойства.
Приложение 2
Дата добавления: 2017-09-01; просмотров: 3621;











