Вырожденный Ферми-газ.

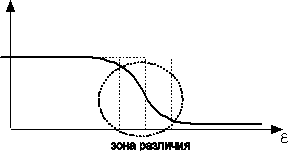
Обратимся теперь к Ферми-частицам. Условие нормировки и здесь даёт, что при уменьшении T (μ<0) |μ| растёт, при некотором T=Tвыр μ=0. Однако здесь ничто не мешает μ стать положительным при 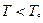 (см. рис.). Рассмотрим сначала газ фермионов при T→0. Функция распределения даёт:
(см. рис.). Рассмотрим сначала газ фермионов при T→0. Функция распределения даёт:
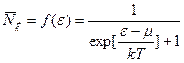 (11)
(11)
При T→0 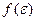 стремится к единичной функции хевисаиде:
стремится к единичной функции хевисаиде:
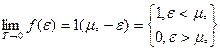 , где
, где 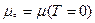

И видно, что 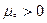 , иначе частицам некуда деться
, иначе частицам некуда деться
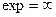 при
при 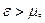
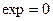 при
при 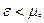
Здесь рисунок
Имеем в виду наиболее важные приложения, будем говорить об электронном газе g=2s+1=2, s=1/2. На каждом уровне в металле согласно принципу запрета Паули может находиться не более двух электронов с противоположно направленными спинами. Так как на нижнем (0-м уровне) – только два электрона, то 3-й и 4-й вынуждены занимать 1-й возбуждённый уровень, 5-й и 6-й – 2-й и т.д. Если полное число электронов N – то занятыми будут N/2 (или (N+1)/2) уровней с энергиями 0≤ε≤μ°. Остальные уровни с ε≥εmax – свободны. Таким образом, благодаря принципу запрета, электроны вынуждены попадать в возбуждённое состояние даже при абсолютном нуле температуры.
εmax= μ° - энергия Ферми. Найдём её из условия нормировки:
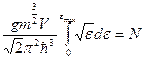
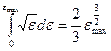
отсюда для электронов (g = 2) энергия Ферьми:
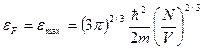 (39)
(39)
Аналогичное «плотное заполнение» будет при Т = 0 и в пространстве импульсов – внутри сферы с радиусом pmax=(2mε)1/2 – поверхность Ферми (при εi << m0c2),
Полная внутренняя энергия, при Т = 0:
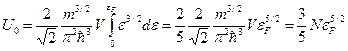 (40)
(40)
Из уравнения состояния pV = 2U/3
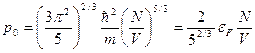 (41)
(41)
Даже при Т= 0 давление ферми газа отлично от нуля.
В метане: N/V = 5*1022cm-3, p0 = 5*104atm
Формулы (40), (41) справедливы приближенно также при температурах близких к абсолютному нулю:
kT << εF; kT << 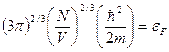 (42
(42
(TF = εF/k), TF по порядку величины, естественно, совпадает с температурой вырождения. Еще раз численная оценка: TF~104 105 (εF~10-12 эрг). Т.е. электронный газ в металлах при любых Т, вплоть до Т плавления можно считать вырожденным. TF – температура вырождения.
Электронный газ обладает своеобразной особенностью – он становится тем более идеальным, чем выше его плотность. Почему? Рассмотрим плазмы: электроны и ионы(ядра)(Наличие ядер не сказывается на ТД величинах электронного газа)
Энергия кулоновского взаимодействия электронов с ядрами, на один электрон: ze2/a, где ze – заряд ядра, а ~ 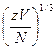 - среднее расстояние от электрона до иона. Условие идеальности: энергия взаимодействия ze2/a ~ εF, ze2/a << εF. Подставим а и получим:
- среднее расстояние от электрона до иона. Условие идеальности: энергия взаимодействия ze2/a ~ εF, ze2/a << εF. Подставим а и получим:
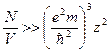 - выполняется тем лучше, чем больше N/V.
- выполняется тем лучше, чем больше N/V.
Для невырожденного газа(обычной плазмы):
ze2/a << kT => 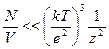 - наоборот.
- наоборот.
Практическое значение имеет выход электронов в теплоемкость металла. В 0-м приближении T << TF C = 0: U0(40) не зависит от Т. Но надо более подробно рассмотреть частицы в зоне разности, где ε(Т) – сущетсв. зависимость. По классической теории, если электроны в идеальном газе, то они должны в одновалентном газе (z = 1) давать в теплоемкость вклад 3R/2 – на эксперименте на два порядка меньше. Почему? Электронный газ сильно вырожден при обычных Т, и доля электронов дающих вклад в теплоемкость можно оценить, как отношение kT и εF:
Сe ~ (3R/2)(kT/εF).
Взяв за основу формулы (22) и (26):
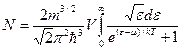
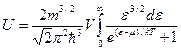
Попробуем получить результат более точно. Интегралы: 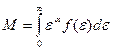 (П1);
(П1);
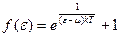 – ф.р. Ферми
– ф.р. Ферми
Пусть kT << μ
Интегрируем (П1) по частям:
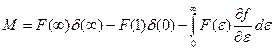 (П2), где
(П2), где 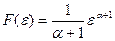
F(0) = 0, f(∞) = 0, и 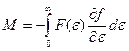
Перейдем к переменной x = (ε - μ)/kT:
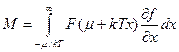 , μ >> kT => нижний предел à -∞
, μ >> kT => нижний предел à -∞
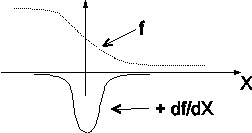
Вклад дают только малые x
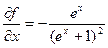 - четная, острая
- четная, острая
Тогда F(μ + kTx) в ряд Тейлора и берем несколько первых членов:
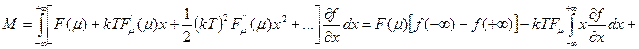
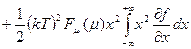
1) f(-∞) = 1; f(+∞) = 0;
2) 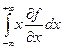 = 0
= 0
3) 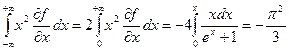
Итак, 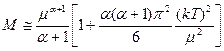 (П4)
(П4)
Тогда 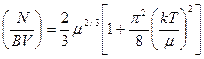 (43)
(43)
При Т = 0, μ = μ0 = εF
При Т ≠ 0 (43) можно переписать как:
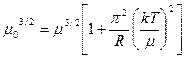 , причем во втором слагаемом можно положить μ = μ0, тогда с точностью до
, причем во втором слагаемом можно положить μ = μ0, тогда с точностью до 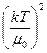 , имеем:
, имеем:
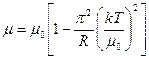 (44)
(44)
Теперь положим 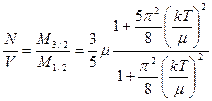 , и с помощью (44) до ~
, и с помощью (44) до ~ 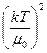 имеем:
имеем:
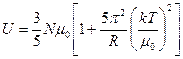 (45)
(45)
и для теплоемкости идеального газа
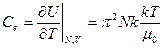 (46)
(46)
Сe ~ T, à 0 при T à 0. Но Среш ~ T3, и Сe > Среш при T à 0.
Для вычисления энтропии вычислим Ω = -2U/3 = 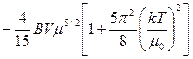 (47)
(47)
Отсюда найдем энтропию:
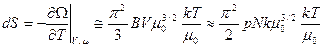 (48)
(48)
И, наконец, найдем давление p = -Ω/V => 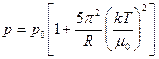 (49)
(49)
Тепловое движение дает только маленькую добавку в давление электронного газа в металле.
Дата добавления: 2021-05-28; просмотров: 526;











