Фазовое равновесие теплоносителей.
· Правило фаз:
s=k-f+2 (1),
где s - число степеней свободы данной системы;
f - число фаз системы;
k - число компонентов системы.
· для трехфазной однокомпонентной системы:
s=1-3+2=0.
· для двухфазной однокомпонентной системы:
s=1-2+2=1.
· для однофазной однокомпонентной системы:
s=1-1+2=2.
Фазовые переходы в однокомпонентных системах.
· Уравнение Клапейрона-Клаузиуса 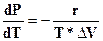 (2),
(2),
где Р - давление;
r - молярная теплота фазового перехода;
Т - температура фазового перехода (испарения, плавления, возгонки);
∆V - изменение объема 1 моля вещества при переходе его из одной фазы в другую.
Фазовые переходы в многокомпонентных системах.
· Закон Генри: 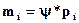 (3),
(3),
где mi - молекулярная доля газа в растворе;
ψ - константа Генри;
pi - парциальное давление газа над жидкостью.
· Закон Рауля: 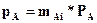 (4),
(4),
где рА - парциальное давление компонента А в парах;
РА - давление паров чистого компонента А;
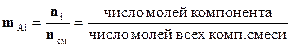 - молекулярная доля этого компонента в растворе.
- молекулярная доля этого компонента в растворе.
· Закон распределения: 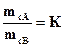 (5),
(5),
где К - молярный коэффициент распределения;
mCA - концентрация вещества С в жидкости А
в г-моль/л;
mCВ - концентрация вещества С в жидкости B.
Дата добавления: 2021-01-11; просмотров: 567;











