Кинетика электролитной коагуляции
Устанавливает закономерности электролитной коагуляции во времени.
основная характеристика – скорость коагуляции Vк .
 Vк –изменение общего числа частиц дисперсной фазы в единицу времени в единице объема: Vк = -
Vк –изменение общего числа частиц дисперсной фазы в единицу времени в единице объема: Vк = - 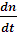
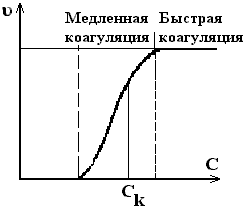
Ход коагуляции в зависимости от С коагулирующего электролита можно разделить на 2 стадии: медленную и быструю
Рис.6.6. Зависимость скорости электролитной коагуляции от концентрации электролита
Концентрация электролита, начиная с которой скорость не зависит от концентрации, называется порогом быстрой коагуляции.Быстрая коагуляция начинается при ΔU=0.
Если ΔU >кТ частиц, то коагуляция происходит за счет особо активных, энергия которых больше ΔU – медленная коагуляция.
При ΔU =0 – быстрая коагуляция.
Кинетика быстрой коагуляции разработана Смолуховским.
Приняв кинетические закономерности коагуляции аналогичными реакции второго порядка, в элементарном акте которой участвуют две частицы, Смолуховский получил уравнение для расчета числа частиц, оставшихся в золе ко времени t:
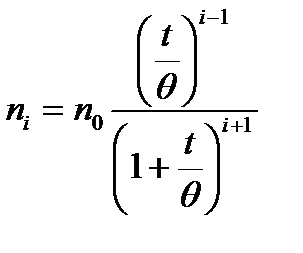 , (6.5)
, (6.5)
где n0 — первоначальное число частиц; i — порядок частиц (одиночные, двойные, тройные и т. д.); t - время от начала коагуляции; q - время половинной коагуляции, т.е. время, в течение которого число частиц уменьшается в два раза.
Суммарное число частиц ån всех кратностей, оставшихся в золе ко времени t, выражается уравнениями:
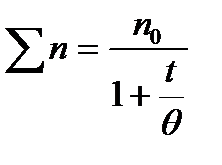 или
или 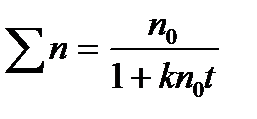 , (6.6)
, (6.6)
где k — константа скорости коагуляции, при t = q Sn = n0/2. Величины k и q связаны между собой соотношением
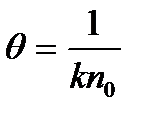 (6.7)
(6.7)
На рис. 6.7. представленыкривые, показывающие изменение во времени относительного числа частиц различной кратности в процессе коагуляции. Как видно из рисунка, общее число частиц непрерывно уменьшается, причём число одинарных частиц уменьшается с максимальной скоростью. Число двойных, тройных и т.д. частиц проходит через максимум (в начальный момент их не было в системе), причём высота максимума падает с увеличением кратности.
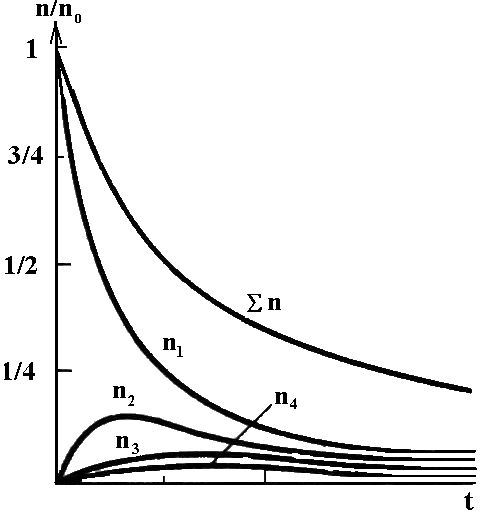
Рис. 6.7. Кинетические кривые изменения относительного числа частиц различной кратности во времени в процессе коагуляции
Принимая, что ΔU =0, все соударения эффективны, теория дает для константы скорости быстрой коагуляции выражение:
Кб= 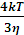 (6.8)
(6.8)
Впоследствии теория Смолуховского была блестяще экспериментально подтверждена и развита другими учеными: Зигмонди(*), Мюллером(*).
В частности, в теории быстрой коагуляции полидисперсных золей Мюллером было объяснено, почему полидисперсные золи коагулируют быстрее монодисперсных. Крупные частицы выступают в виде зародышей коагуляции, в их присутствии маленькие частицы исчезают быстрее, чем в их отсутствии.
Если DU ¹ 0 и P ¹ 1, то не все соударения частиц эффективны, в этом случае происходит медленная коагуляция. Кинетика медленной коагуляции развита Н. А. Фуксом(*) во время его работы в Научно-исследовательском физико-химический институте имени Л.Я. Карпова. Фуксом показано, что если DU >> kT, то скорость коагуляции близка к нулю и система может рассматриваться как агрегативно устойчивая. Константа скорости k в этом случае определяется соотношением:
k = kБ×P×exp(- DU/RT)
или
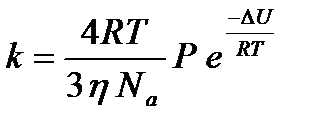 , (6.9)
, (6.9)
где kБ - константа быстрой коагуляции; P - стерический множитель, учитывающий благоприятные пространственные расположения частиц при их столкновении.
Вероятность слипания частиц выше, если они столкнутся сторонами, гидратированными в меньшей степени. При таком подходе быстрая коагуляция является лишь частным случаем медленной коагуляции, когда выполняется условие, что DU = 0 и P = 1. Замедление коагуляции, обусловленное потенциальным барьером отталкивания, характеризуется фактором устойчивости W (коэффициентом стабильности):
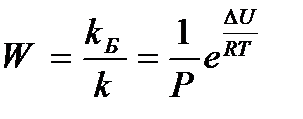 (6.10)
(6.10)
Дата добавления: 2016-07-27; просмотров: 2292;











