Внутренняя энергия. Первый закон термодинамики. Применение первого закона термодинамики. Применение первого закона термодинамики к изопроцессам. Адиабатный процесс.
Каждое тело имеет вполне определенную структуру, оно состоит из частиц, которые хаотически движутся и взаимодействуют друг с другом, поэтому любое тело обладает внутренней энергией. Внутренняя энергия — это величина, характеризующая собственное состояние тела, т.е. энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, ионов) и энергия взаимодействия этих частиц Внутренняя энергия одноатомного идеального газа определяется по формуле
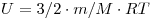 .
.
Внутренняя энергия тела может изменяться только в результате его взаимодействия с другими телами. Существует два способа изменения внутренней энергии: теплопередача и совершение механической работы (например, нагревание при трении или при сжатии, охлаждение при расширении).
Теплопередача — это изменение внутренней энергии без совершения работы: энергия передается от более нагретых тел к менее нагретым. Теплопередача бывает трех видов: теплопроводность (непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела); конвекция (перенос энергии потоками жидкости или газа) и излучение (перенос энергии электромагнитными волнами). Мерой переданной энергии при теплопередаче является количество теплоты ( 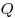 ).
).
Эти способы количественно объединены в закон сохранения энергии, который для тепловых процессов читается так: изменение внутренней энергии замкнутой системы равно сумме количества теплоты, переданной системе, и работы внешних сил, совершенной над системой. 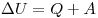 , где
, где 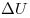 — изменение внутренней энергии,
— изменение внутренней энергии, 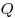 — количество теплоты, переданное системе,
— количество теплоты, переданное системе, 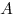 — работа внешних сил. Моли система сама совершает работу, то ее условно обозначают
— работа внешних сил. Моли система сама совершает работу, то ее условно обозначают 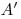 . Тогда закон сохранения энергии для тепловых процессов, который называется первым законом термодинамики, можно записать так:
. Тогда закон сохранения энергии для тепловых процессов, который называется первым законом термодинамики, можно записать так: 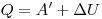 , т. е. количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии.
, т. е. количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии.
При изобарном нагревании газ совершает работу над внешними силами 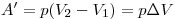 , где
, где 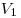 и
и 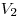 — начальный и конечный объемы газа.
— начальный и конечный объемы газа.
Если процесс не является изобарным, величина работы может быть определена площадью фигуры ABCD, заключенной между линией, выражающей зависимость 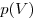 , и начальным и конечным объемами газа (рис. 13).
, и начальным и конечным объемами газа (рис. 13).
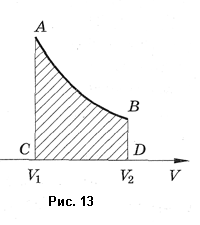
Рассмотрим применение первого закона термодинамики к изопроцессам, происходящим с идеальным газом.
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение первого закона термодинамики примет вид: 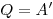 , т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы: 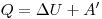 .
.
При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. 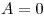 , и уравнение первого закона имеет вид
, и уравнение первого закона имеет вид 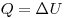 , т.е. переданное количество теплоты идет на увеличение внутренней энергии газа.
, т.е. переданное количество теплоты идет на увеличение внутренней энергии газа.
Адиабатным называют процесс, протекающих без теплообмена с окружающей средой. 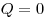 , следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается,
, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается, 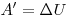 . Кривая, изображающая адиабатный процесс, называется адиабатой.
. Кривая, изображающая адиабатный процесс, называется адиабатой.
Дата добавления: 2016-07-18; просмотров: 2061;











