ПРИМЕРЫ ИСПОЛЬЗОВАНИЯ ТЕРМИНОВ И ПРЕДСТАВЛЕНИЙ ФИЗИЧЕСКОЙ ХИМИИ ПРИ РЕШЕНИИ ПРАКТИЧЕСКИХ ЗАДАЧ
Пример 1.Рассмотрим реакцию окисления марганца, растворенного в жидком железе:
[Мп] + (Fe) = (МпО) + Fe ж,
ΔG0=-120 000+ 60 T.
Из соотношения для ΔG ° следует, что: а) при окислении марганца выделяется тепло; б) при повышении Т знак «минус» может поменяться на «плюс».
Какие факторы могут влиять на концентрацию Мп?
Из выражения для константы равновесия KМп = a(МnO)/[Mn] - a(Fe0) следует, что [МП] = (1/КМп)(а(Mn))/a(FeO)), т. е. чем меньше a(FeO) , тем больше [Мп].
Как уменьшить a(FeO)? a. Можно раскислить ванну, т. е уменьшить окисленность и металла, и шлака. б. Создать благоприятные условия для протекания реакции [С] + (FeO) = = СОГ + Fеж, тогда окисленность шлака (a(FeO)) уменьшится и произойдет восстановление марганца из шлака.
Пример 2. Рассмотрим процессы удаления неметаллических включений (НВ). Если 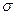 нв-газ <
нв-газ < 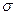 нв-Ме, то включение будет «прилипать» к пузырьку газа и всплывать вместе с ним (флотация включений). Если
нв-Ме, то включение будет «прилипать» к пузырьку газа и всплывать вместе с ним (флотация включений). Если 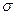 нв.нв <
нв.нв < 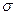 нв-Ме, то будут наблюдаться коалесценция включений, их укрупнение.
нв-Ме, то будут наблюдаться коалесценция включений, их укрупнение.
Пример 3.Если в системе металл-шлак значение степени растекания Sр = WАДГ - WKor, большое (работа адгезии значительно больше работы коге-зии), то взаимное смачивание металла и шлака хорошее и отделить шлак от металла трудно. Если же WKor,» WАДГ, то шлак не растекается по металлу, т. е. металл «оголяется», возрастает угар железа и т. п.
Дата добавления: 2016-06-22; просмотров: 1781;











