Фермент: Триозофосфатизомераза
ФГА служит промежуточным продуктом гликолиза и глюконеогенеза.
Таким образом, в печени, содержащей соответствующие ферменты, глицерол может превратиться в пируват (ПВК), который в аэробных условиях через цикл Кребса и окислительное фосфорилирование полностью окисляется до углекислого газа и воды. Энергия 1 моль глицерина аккумулируется (трансформируется) в 22 моль АТФ.
1.3. β - Окисление жирных кислот
Как уже указывалось, значительную часть энергии, извлекаемой в процессе окисления, животный организм получает из жирных кислот, которые расщепляются путем окисления при β-углеродном атоме.
β-Окисление жирных кислот было впервые изучено в 19004 г. Ф. Кноопом. В дальнейшем было установлено, что β-окисление осуществляется только в митохондриях. Благодаря работам Ф. Линена с сотрудниками (1954-1958 г.г.) были выяснены основные ферментативные процессы окисления жирных кислот. В честь ученых, открывших данный путь окисления жирных кислот, процесс β-окисления получил название цикла Кноопа-Линена.
β-Окисление — специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно отделяется по 2 атома углерода в виде ацетил-КоА. Метаболический путь - β-окисление - назван так потому, что реакции окисления жирной кислоты происходят у β-углеродного атома. Реакции β-окисления и последующего окисления ацетил-КоА в ЦТК (цикле трикарбоновых кислот) служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования. β-Окисление жирных кислот происходит только в аэробных условиях.
Все реакции многостадийного окисления ускоряются специфическими ферментами. β-окисление высших жирных кислот является универсальным биохимическим процессом, протекающим во всех живых организмах. У млекопитающих этот процесс происходит во многих тканях, в первую очередь в печени, почках и сердце. Окисление жирных кислот происходит в митохондриях. Ненасыщенные высшие жирные кислоты (олеиновая, линолевая, линоленовая и др.) предварительно восстанавливаются до предельных кислот.
Проникновению жирных кислот в митохондриальный матрикс предшествует их активация путем образования соединения с коэнзимом А (НS~КоА), содержащего макроэргическую связь. Последняя, видимо, способствует более гладкому протеканию реакций окисления образовавшегося соединения, которое называют ацилкоэнзимом А(ацил-КоА).
Взаимодействие высших жирных кислот с КоА ускоряется специфическими лигазами - ацил-КоА-синтетазамитрех видов, специфичных соответственно для кислот с коротким, средним и длинным углеводородными радикалами. Они локализованы в мембранах эндоплазматической сети и в наружной мембране митохондрий. По-видимому, все ацил-КоА-синтетазы являются мультимерами; так, фермент из микросом печени имеет молекулярную массу 168 кДа и состоит из 6 идентичных субъединиц. Реакция активации жирных кислот протекает в 2 этапа:
а) сначала жирная кислота реагирует с АТФ с образаванием ациладенилата:
RCOOH + ATФ → RCO~AMФ + ФФ
б) затем идет образование активированной формы ацил-КоА:
RCO~AMФ + НS~КоА → RCO~SKoA + AMФ
Пирофосфат (ФФ) быстро гидролизуется под действием пирофосфатазы, в результате чего вся реакция оказывается необратимой: ФФ + H2O → 2Ф
Суммарное уравнение:
RCOOH + ATФ+ НS~КоА→ RCO~SKoA + AMФ + 2Ф
Жирные кислоты с короткой и средней длиной цепи (от 4 до 12 атомов углерода) могут проникать в матрикс митохондрий путём диффузии, там происходит их активация. Жирные кислоты с длинной цепью, которые преобладают в организме человека (от 12 до 20 атомов углерода), активируются ацил-КоА синтетазами, расположенными на внешней мембране митохондрий.
Внутренняя мембрана митохондрий непроницаема для длинноцепочных ацил-КоА, образовавшихся в цитоплазме. Переносчиком активированных жирных кислот служит карнитин (витамин Вт), который поступает с пищей или синтезируется из незаменимых аминокислот лизина и метионина.
В наружной мембране митохондрий находится фермент карнитинацилтрансфераза I(карнитин-палъмитоилтрансфераза I), катализи- рующий реакцию с образованием ацилкарнитина:
 H3C H3C
H3C H3C
RCO~SKoA + H3C- N+-CH2-CH-CH2-COOH ↔ H3C- N+-CH2-CH-CH2-COOH + HS~KoA
H3C H3C О
OH O-C – R
Ацил-КоА Карнитин (Вт) Ацилкарнитин Кофермент А
Этот фермент является регуляторным, он регулирует скорость поступления ацильных групп в митохондрии, а, следовательно, и скорость окисления жирных кислот.
Образовавшийся ацилкарнитин проходит через межмембранное пространство к наружной стороне внутренней мембраны и транспортируется с помощью карнитинацилкарнитинтранслоказы на внутреннюю поверхность внутренней мембраны митохондрий, где фермент карнитинацилтрансфераза II катализирует перенос ацила на внутримитохондриальный КоА, то есть обратную реакцию (рис.9).
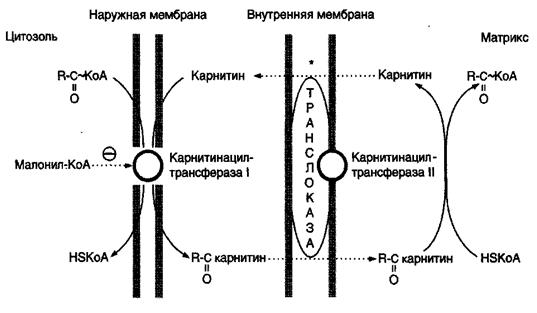
Рис.9. Перенос жирных кислот с длинным углеводородным радикалом через мембраны митохондрий
Итак, ацил-КоА становится доступным для ферментов β-окисления. Свободный карнитин возвращается на цитозольную сторону внутренней мембраны митохондрий той же транслоказой. После этого ацил-КоА включается в реакции β-окисления.
В матриксе митохондрий происходит катаболизм (распад) ацил-КоА в результате повторяющейся последовательности из четырех реакций.
1) Первой реакцией в каждом цикле является его окисление ферментом ацил-КоА-дегидрогеназой, коферментом которого является ФАД. Дегидрирование происходит между β - и α - атомами углерода, в результате чего в углеродной цепи образуется двойная связь и продуктом этой реакции является еноил-КоА:
R-CH2-CH2CO~SKoA + ФАД → R-CH=CHCO~SKoA + ФАДН2
Ацил-КоА Еноил-КоА
2) На втором этапе цикла окисления жирных кислот происходит гидратация двойной связи еноил-КоА, в результате чего образуется β-гидроксиацил-КоА. Реакция катализируется ферментом еноил-КоА-гидратазой:
OH

R-CH=CHCO~SKoA +Н2О → R-CH-CH2CO~SKoA
Еноил-КоА β- гидроксиацил-КоА
3) На третьем этапе цикла β-гидроксиацил-КоА подвергается дегидрированию (второму окислению) при участии фермента β-гидроксиацил-КоА-дегидрогеназы, коферментом которой является НАД+. Продуктом данной реакции является β-кетоацил-КоА:
OH

R-CH-CH2CO~SKoA + НАД+ → R-CОCH2CO~SKoA + НАДН + Н+
β- гидроксиацил-КоА β- кетоацил-КоА
4) Последняя реакция цикла окисления жирных кислот катализируется ацетил-КоА-ацилтрансферазой (тиолазой). На этом этапе β-кетоацил-КоА взаимодействует со свободным КоА и расщепляется с образованием, во-первых, двухуглеродного фрагмента, содержащего два концевых углеродных атома исходной жирной кислоты в виде ацетил-КоА, и, во-вторых, КоА-эфира жирной кислоты, укороченной теперь на два атома углерода. По аналогии с гидролизом эту реакцию называют тиолизом:
R-CОCH2CO~SKoA + НS~KoA → CH3CO~SKoA + R1CO~SKoA
β- кетоацил-КоА Ацетил-КоА Ацил-КоА,
укороченный на
2 углеродных атома
Укороченный ацил-КоА подвергается далее следующему циклу окисления, начинающемуся с реакции, катализируемой ацил-КоА-дегидрогеназой (окисление), затем следует реакция гидратации, реакция второго окисления, тиолазная реакция, то есть этот процесс многократно повторяется (рис.10).
β- Окисление высших жирных кислот протекает в митохондриях. В них же локализованы ферменты дыхательного цикла, ведущие передачу атомов водорода и электронов на кислород в условиях окислительного фосфорилирования АДФ, поэтому β-окисление высших жирных кислот является источником энергии для синтеза АТФ.
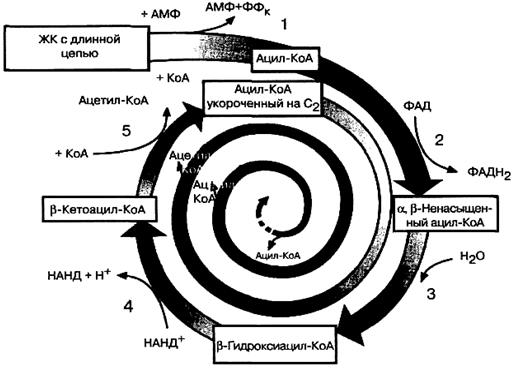
Рис.10. Окисление жирной кислоты
Окончательным продуктом β-окисления высших жирных кислот с четным числом углеродных атомов является ацетил-КоА, а с нечетным- пропионил-КоА.
Если бы ацетил-КоА накапливался в организме, то запасы HS~KoA скоро исчерпались бы, и окисление высших жирных кислот остановилось. Но этого не происходит, так как КоА быстро освобождается из состава ацетил-КоА. К этому приводит ряд процессов: ацетил-КоА включается в цикл трикарбоновых и дикарбоновых кислот или весьма близкий к нему глиоксилевый цикл, или ацетил-КоА используется для синтеза стеролов и соединений, содержащих изопреноидные группировки и т.п.
Пропионил-КоА, являющийся конечным продуктом β-окисления высших жирных кислот с нечетным числом углеродных атомов, превращается в сукцинил-КоА, который утилизируется через цикл трикарбоновых и дикарбоновых кислот.
Около половины жирных кислот в организме человека ненасыщенные.
β-Окисление этих кислот идёт обычным путём до тех пор, пока двойная связь не окажется между третьим и четвёртым атомами углерода. Затем фермент еноил-КоА-изомераза перемещает двойную связь из положения 3—4 в положение 2-3 и изменяет цис-конформацию двойной связи на транс-, которая требуется для β-окисления. В этом цикле β-окисления первая реакция дегидрирования не происходит, так как двойная связь в радикале жирной кислоты уже имеется. Далее циклы β-окисления продолжаются, не отличаясь от обычного пути. Основные пути метаболизма жирных кислот демонстрирует ри.11.
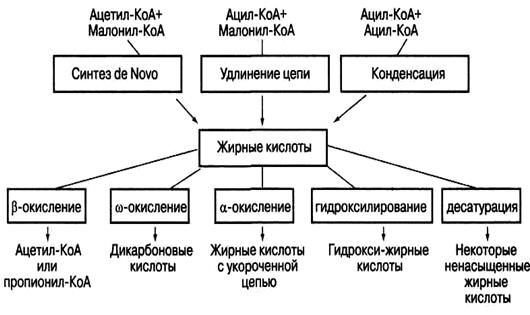
Рис.11.Основные пути метаболизма жирных кислот
Недавно было обнаружено, что помимо β-окисления – основного пути катаболизма жирных кислот, в тканях мозга происходит α-окисление жирных кислотс числом атомов углерода (С13-С18), то есть последовательное отщепление одноуглеродных фрагментов от карбоксильного конца молекулы.
Этот тип окисления наиболее характерен для растительных тканей, но может происходить и в некоторых тканях животных. α-Окисление имеет циклический характер, причем цикл состоит из двух реакций.
Первая реакция заключается в окислении жирной кислоты пероксидом водорода в соответствующий альдегид и СО2 с участием специфической пероксидазы:
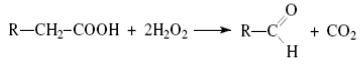
В результате этой реакции углеводородная цепь укорачивается на один атом углерода.
Суть второй реакции заключается в гидратации и окслении образовавшегося альдегида в соответствующую карбоновую кислоту под действием альдегиддегидрогеназы, содержащей окисленную форму кофермента НАД:
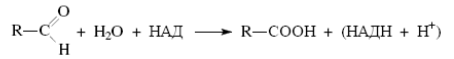
Затем цикл α-окисления повторяется снова. В сравнении с β-окислением этот тип окисления энергетически менее выгоден.
ω-Окисление жирных кислот. В печени животных и у некоторых микроорганизмов существует ферментная система, обеспечивающая ω-окисление жирных кислот, то есть окисление по концевой СН3-группе, обозначаемой буквой ω. Сначала под действием монооксигеназыпроисходят гидроксилирование с образованием ω-оксикислоты:
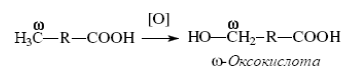
Затем ω-оксикислота окисляется в ω-дикарбоновую кислоту под действием соответствующей дегидрогеназы:
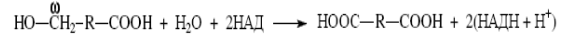
Полученная таким образом ω-дикарбоновая кислота укорачивается с любого конца с помощью реакций β-окисления.
Дата добавления: 2016-06-09; просмотров: 4483;











