Квантовая теория строения атома водорода.
В атоме водорода вокруг ядра (протона), несущего заряд e, движется один электрон. Ядро можно считать неподвижным, поскольку его масса в 1840 раз больше массы электрона; орбиты электрона в первом приближении можно считать круговыми.
Центростремительной силой, удерживающей электрон на орбите радиусом r, является кулоновская сила притяжения между электроном и ядром:
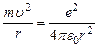 , (14)
, (14)
m - масса электрона, 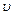 - его скорость,
- его скорость,  .
.
Решая (14) совместно с (12), получим выражение для радиуса стационарной орбиты атома водорода:
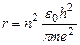 , (15)
, (15)
где n = 1, 2, 3, … . Для n = 1, r1 ≈ 0.53 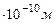 .
.
Полная энергия W электрона в атоме слагается из кинетической энергии Wк поступательного движения электрона по орбите и потенциальной энергии Wп притяжения электрона к ядру.
Учитывая (14), получим
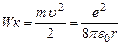 (16)
(16)
Потенциальная энергия должна быть отрицательна и равна
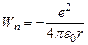 (17)
(17)
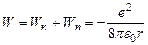 (18)
(18)
Т.е. полная энергия электрона оказывается отрицательной и равной по абсолютной величине его кинетической энергии. Подставляя в (18) выражение для r из (15), получим
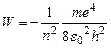 (19)
(19)
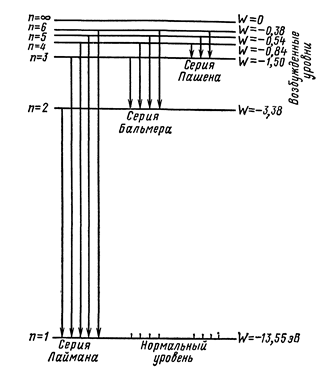
По этой формуле можно рассчитать энергию электрона для любой стационарной орбиты. Величина полной энергии электрона, находящегося на стационарной орбите, называется уровнем энергии атома.
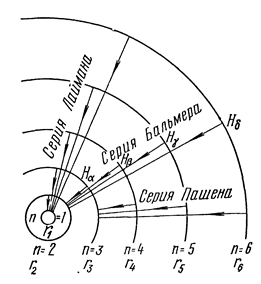
Согласно (19), энергия атома возрастает с увеличением квантового числа n, или с увеличением радиуса электронной орбиты. Так как W отрицательна, уменьшение ее абсолютной величины соответствует возрастанию энергии.
| 
|
Энергетический уровень W = - 13,55 эВ называется нормальным уровнем, все остальные уровни называются возбужденными.
Выведем общую формулу для частоты 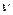 излучения атома. Для этого (19) подставим в (13):
излучения атома. Для этого (19) подставим в (13):
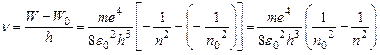 , (20),
, (20),
где n и W соответствуют начальным состояниям атома (до излучения), а n0 и W0 – после излучения,
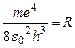 , (21)
, (21)
– постоянная Ридберга,
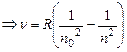 (22)
(22)
Эмпирические формулы (9), (10) и (11) являются частными случаями (22).
Дата добавления: 2017-11-21; просмотров: 1216;











