Топливо Уд. теплота сгорания
ОСНОВНЫЕ ПОНЯТИЯ
Технология, система технологий
Реализация технологий
Триада составных производства
Промышленная технология
Научная технология
Комплексная отрасль
Экономическое назначение продукции
Производственный процесс
Технологический процесс
Основной процесс
Вспомогательный процесс
Технологический регламент
Химико-технологический процесс
Экономическая оценка технологического процесса
Денежные и материально-энергетические потоки
Себестоимость
Единичное производство
Серийное производство
Массовое производство
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
1. Что такое технология и система технологий?
2. Чем отличается промышленная технология от научной?
3. Что включает в себя триада составных производств?
4. Раскройте сущность производственного технологического
процесса?
5. Назовите составные части технологического регламента?
ГЛАВА 2. СЫРЬЕ, ТОПЛИВО, ВОДА И ВОЗДУХ
В ТЕХНОЛОГИЧЕСКИХ ПРОЦЕССАХ
2.1. Определение сырья и его классификация
Сырьем называют вещество природного и синтетического происхождения, используемое для производства промышленной продукции.
Так, добытая железная руда является сырьем в металлургической промышленности, вискозное волокно – сырьем в текстильной промышленности.
Основное сырье даёт природа – 75% полезные ископаемые,
25% сельское хозяйство, морское и лесное хозяйство.
Природное сырье характеризуется тем, что его получают в готовом виде из недр земли, из различных горных пород, растений. Искусственное сырье характеризуется тем, что его получают из разных природных материалов. К этому классу можно отнести химические волокна, синтетические каучуки и др.
Искусственное сырье подразделяется на два подкласса – органическое (вискозные, ацетатные волокна) и минеральные (силикатные волокна).
По агрегатному состоянию сырье бывает твердое, жидкое и газообразное.
По происхождению – минеральное, растительное и животное.
По составу – органическое и неорганическое (минеральное). В природе встречается примерно 2500 минералов, отличающихся друг от друга по химическому составу, физическим свойствам, кристаллической форме и прочим признакам.
Минеральное сырье делится на 3 вида: рудное, нерудное и горючее.
Рудное сырье классифицируется по числу содержащихся в нем металлов, химическому составу минералов и пустой породы.
Нерудное сырье – горные породы, используемые в производстве химических, строительных и других неметаллических материалов (фосфориты, апатиты, природные калийные соли, поваренная соль, песок, гравий, глина и т.п.).
Горючее минеральное сырье, включающее угли, нефть, торф, горючие сланцы, природный газ и т. д., служит источником получения разнообразнейших продуктов.
Растительное и животное сырье по своему назначению делится на пищевое и техническое.
Пищевое сырье – продукты сельского, лесного и рыбного хозяйства, которые используются для пищевых целей (картофель, сахарная свекла, хлебные злаки, пищевые жиры и т. п.).
Кроме минерального, растительного и животного, сырьем для промышленности служит воздух и вода.
2.2. Обогащение сырья
Добываемое из недр Земли сырье, как правило, подвергается обогащению с целью получения сырья в концентрированном виде, т.е. с повышенным содержанием в нем полезного компонента.
Если обогащаются твердые породы (например, горные породы, уголь), то полученный продукт, обогащенный полезной составной частью, называют концентратом, а отходы, содержащие пустую породу, – хвостами.
Методы обогащения твердых материалов основаны на различии физических и химических свойств составляющих компонентов сырья: плотности, твердости, растворимости, температуры плавления и возгонки, электропроводности, магнитной проницаемости, смачиваемости отдельными жидкостями.
Применяется грохочение, гравитационное обогащение, мокрое гравитационное обогащение, магнитная сепарация, флотационный и другие методы.
Рассеивание (грохочение) основано на том, что минералы, входящие в состав сырья, имеют различную прочность, поэтому при дроблении менее прочные (хрупкие) минералы дробятся на более мелкие зерна, чем более прочные (вязкие). Если после измельчения такое сырье просеять через сита с различной величиной отверстий, то с отдельных сит можно получить фракции, обогащенные тем или иным минералом. Применяемые для рассеивания сита называют грохотами.
Грохочение часто производят и для разделения однородного материала на куски или зерна определенного размера; грохоты могут быть плоские с небольшим наклоном сита для скольжения крупной фракции, которые часто снабжаются механизмами для сотрясения, вибрации или качания, и цилиндрические – наклонные вращающиеся барабаны с отверстиями, которые рассеивают материал, поступающий внутрь цилиндра.
Гравитационное разделение основано на различии скоростей падения частиц различной плотности или крупности в потоке жидкости (чаще всего в воде) – мокрое гравитационное обогащение; воздуха или инертного газа – сухое гравитационное обогащение.
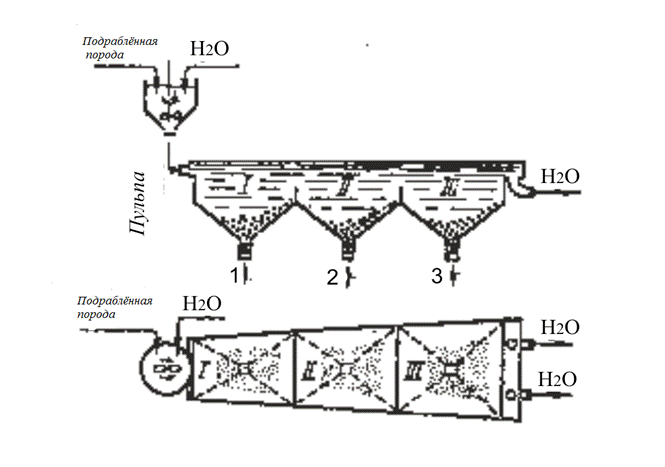
Мокрое гравитационное обогащение осуществляется следующим образом (рис.2.1). Измельченное сырье смешивается с водой в баке с мешалкой и в виде пульпы (взвесь твердого материала в жидкости) подается в осадительные камеры (корыта) І, ІІ, ІІІ с конусообразными днищами (бункерами).
| |
Рис. 2.1. Принципиальная схема мокрого гравитационного обогащения
Так как ширина камер постепенно увеличивается, происходит замедление движения пульпы через камеры, что облегчает осаждение твердых частиц. В камере І выпадает из воды наиболее тяжелая (крупно-зернистая фракция), в камере ІІ – средняя и в камере ІІІ- легкая (мелкозернистая). В зависимости от того, на сколько фракций требуется разделить сырье, аппараты – классификаторы состоят из одной, двух и более камер. Фракции из камер выгружают через отверстия 1, 2, 3. Наряду с рассмотренным класификатором применяются и другие типы аппаратов – концентрационные столы, отсадочные машины.
При сухом гравитационном обогащении применяют воздушные сепараторы центробежного типа (рис 2.2).
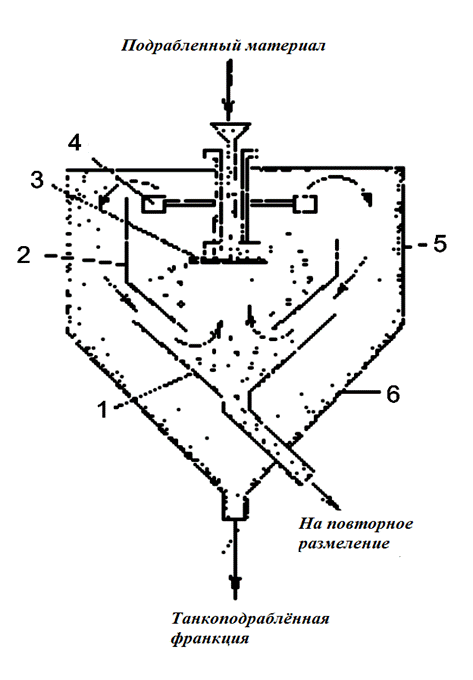 Сепаратор состоит из цилиндра 5, который заканчивается конусом 6.
Сепаратор состоит из цилиндра 5, который заканчивается конусом 6.
В цилиндре 5 помещен внутренний цилиндр 2 с конусом 1, в котором имеется тарелка 3 и крыльчатка вентилятора 4, которая приводится во
вращательное движение от электромотора. При вращении тарелки и
крыльчатки вентилятора внутри сепаратора образуются воздушные потоки, показанные на схеме стрелками. Измельченный материал, подаваемый на вращающуюся тарелку, разбрасывается по сечению внутреннего цилиндра.
Мелкие частицы материала подхватываются воздушным потоком и выносятся в пространство между внешним и внутренним цилиндрами, где, ударяясь об стенки (теряя скорость движения), опускаются вниз и выводятся через конус 6 в виде тонкоизмельченной фракции. Крупные частицы падают и выводятся через внутренний конус 1 на повторное измельчение.
Магнитная сепарация применяется для разделения магнитно-восприимчивых материалов от немагнитных и для удаления стальных предметов, случайно попавших в руду, например магнитный железняк отделяется от пустой породы руды. Разделение руды осуществляется в электромагнитных сепараторах (рис. 2.3).
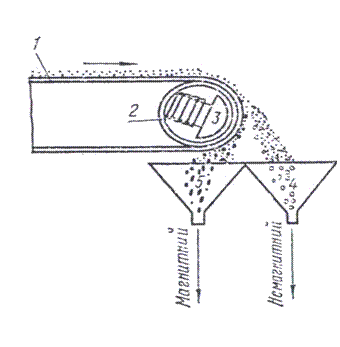 После измельчения материал поступает на движущейся ленточ-ной транспортер 1, имеющий барабан 2, снабженный электромаг-нитом 3. При соприкосновении ленты с поверхностью барабана частицы материала, не обладающие магнитной восприимчивостью, ссыпаются с ленты в бункер 4, а частицы магнитного материала, прилипшие к ленте, продолжают двигаться до тех пор, пока лента не пройдет магнитную поверхность барабана и они не отвернутся от нее, после чего частицы ссыпаются в бункер 5.
После измельчения материал поступает на движущейся ленточ-ной транспортер 1, имеющий барабан 2, снабженный электромаг-нитом 3. При соприкосновении ленты с поверхностью барабана частицы материала, не обладающие магнитной восприимчивостью, ссыпаются с ленты в бункер 4, а частицы магнитного материала, прилипшие к ленте, продолжают двигаться до тех пор, пока лента не пройдет магнитную поверхность барабана и они не отвернутся от нее, после чего частицы ссыпаются в бункер 5.
|
 Флотационный метод обогащения основан на различной смачиваемости зерен отдельных материалов водой. Частицы несмачиваемого (гидрофобного) минерала А будут как бы вдавливаться в жидкость (рис 2.4), но не преодалев сил поверхностного натяжения воды, оставаться на ее повер-хности, тогда как частицы смачиваемого (гидрофильного) материала Б обволакиваются пленкой жидкости и, преодалев силы поверхностного натяже-ния жидкости, опускаются на дно аппарата.
Флотационный метод обогащения основан на различной смачиваемости зерен отдельных материалов водой. Частицы несмачиваемого (гидрофобного) минерала А будут как бы вдавливаться в жидкость (рис 2.4), но не преодалев сил поверхностного натяжения воды, оставаться на ее повер-хности, тогда как частицы смачиваемого (гидрофильного) материала Б обволакиваются пленкой жидкости и, преодалев силы поверхностного натяже-ния жидкости, опускаются на дно аппарата.
Частицы несмачиваемого минерала снимаются с поверхности жидкости, и таким образом происходит разделение руды на фракции. Для ускорения флотации применяют ряд технологических приемов, в часности создают условия неодинаковой смачиваемости водой зерен минералов.
Флотацию проводят во флотационных машинах различного типа (схематичный поперечный разрез машины с воздушным перемешиванием пульпы приведен на рис. 2.5).
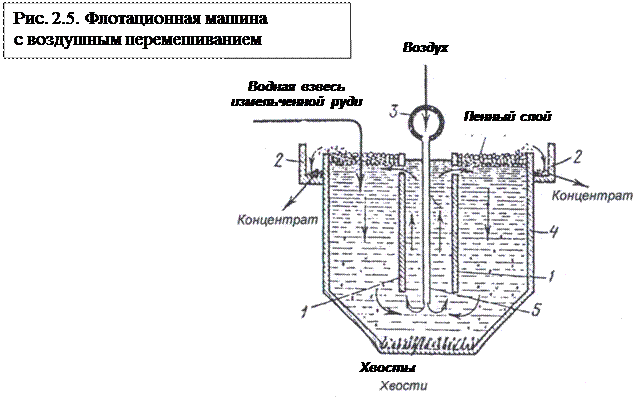
Тонкоизмельченная взвесь породы с флотореагентами подается в машину, состоящую из корытообразного резервуара-камеры 4, внутри которого установлены перегородки 1, а между ними расположены трубки 5. По трубкам 5 из коллектора 3 в камеру 4 подается воздух под давлением, который перемешивает пульпу, и пузырьки его, поднимаясь вверх, увлекают за собой частицы гидрофобного материала, всплывающего на поверхность воды. Кроме того, воздух обеспечивает циркуляцию суспензии в камере. Для удержания на поверхности всплывающих частиц гидрофобного минерала в водную взвесь (суспензию) вводят вещества (сосновое масло, древесный деготь и др.), образующие пену, – пенообразователи. Пену вместе с частицами гидрофобного материала снимают с поверхности жидкости через борт камеры в желоб 2, оттуда она поступает на сгущение (разрушение пены) и фильтрование. Отделенные твердые частицы минерала сушатся и в виде так называемого концентрата поступают потребителю или на дальнейшую переработку. Частицы, осевшие на дно камеры, выводятся в виде флотационных хвостов.
Природные минералы в большинстве хорошо смачиваются водой, и для их разделения флотацией в суспензию вводят специальные реагенты – собиратели или коллекторы, понижающие их смачиваемость. К ним относятся олеиновая кислота, нефтиновые кислоты и др. Собиратели покрывают поверхность частиц гидрофильных минералов гидрофобной пленкой, чем и объясняется всплывание частиц отдельных минералов. В суспензию вводят подавители, или депрессоры (щелочи, соли щелочных металлов и др.). Подавители повышают гидрофильность поверхности частиц минералов и затрудняют их всплывание. Кроме того, применяются реагенты, усиливающие или ослабляющие действие собирателей или подавителей. К ним относятся активаторы, регуляторы и др.
Следовательно, вводя в суспензию различные флотореагенты, можно обеспечить коллективную флотацию, т.е. разделить руду на концентрат, содержащий несколько полезных элементов, и хвосты, не содержащие ценных элементов, или создать такие условия процесса флотации, когда в концентрат будет переходить только какой-либо один определенный минерал, в хвосты – пустая порода и другие минералы. Такая флотация называется избирательной или селективной.
Флотация – один из широко применяемых промышленных методов обогащения сырья в крупных масштабах. Это объясняется тем, что при применении флотореагентов, имеющих различные свойства, можно обогащать и разделять на фракции самые разнообразные породы при незначительном расходе флотационных реагентов (100 г на 1 т породы). Кроме рассмотренных методов обогащения твердых минералов, применяются методы, основанные на различии электропроводности составляющих руды, – электростатистическое обогащение; на различии плавкости материалов, входящих в смесь, – термическое обогащение; на различии растворимости, разложении химическими реагентами, обжиге материалов, входящих в смесь, – химическое обогащение и др.
2.3. Качество сырья и современные технологические процессы
Качество сырья – это совокупность его технологических, физических и химических свойств, обеспечивающих высокий уровень технологического процесса и качества выпускаемой продукции.
Основными технико-экономическими показателями сырья является его химический состав и наличие его в природе, доступность его добычи и технологичность переработки.
Основными характеристиками компонентов материального потока является его состав, он определяет принципиальную схему процесса, его аппаратурное исполнение, затраты сырья, энергии и вспомогательных материалов, количество отходов, уровень безопасности процессов и влияние на окружающую среду.
Контроль состава сырья, промежуточных веществ и продуктов является важнейшим источником информации, необходимой для регламентации и оптимизации технологического процесса.
Состав вещества определяется с помощью различных физико-химических методов в зависимости от глубины и способа переработки сырья, требований к продукту, специфики управления процессами.
Определяющими компонентами сырья могут быть атомы (элементарный состав), молекулы (молекулярный состав), изотопы (изотопный), минералы (минеральный), распределение по размеру частиц, ситовый состав и др. Для твердых и жидких веществ (смесей, растворов, сплавов) определяют концентрацию следующими соотношениями.
Массовая доля компонентов
mk
W = ------- x 100%,
mb
где mk – масса компонента, г, кг; mb – масса вещества, г, кг;
Объемная доля компонентов
Vk
d = -------- х 100%,
Vb
где Vk – объем компонента, см3, м3; Vb – объем вещества, см3, м3.
Если необходимо определить очень малые концентрации, используют тысячные доли или десятую долю процента. Такая единица величины называется промилем (о/оо). Концентрацию компонента в сложном веществе выражают массой компонента, которая содержится в 100г вещества, в одном килограмме, в одном литре или 1м3.
Количественный состав благородных металлов определяют количеством граммов благородного металла в 1000 граммах сплава, его называют пробой. Чистому благородному металлу соответствует тысячная проба. Тысячная проба равна, примерно, 24 карата (США, Великобритания, Швейцария и др.), один карат весит 0,2г.
Состав минералов, силикатов, гидратов определяют соотношением молекул, из которых состоит вещество (Аl2O3; SiO2; P2O5и др.).
Использование количественного соотношения компонентов вещества дает возможность выбирать рациональное сырье, определять теоретические его затраты, выход продукции, затраты энергоресурсов, количество отходов и др.). Количество примесей в веществе является показателем качества и регламентируется техническими уровнями и государственными стандартами (ГОСТ). В расчетах необходимо учитывать, что количественное соотношение компонентов во многих веществах может изменяться под действием внешних факторов ( при хранении увеличивается влажность сахара и т.д.). Количественные расчеты в таких случае производят по компонентам, масса которых является постоянной величиной или изменяется очень мало.
Расчеты энергетических эффектов в химико-технологических процессах выполняют по стехеометрическим уравнениям химических реакций, например, при определении количества тепла, выделяемого при сгорании 1000г серы. S+O2= SO2+297 кДж. Молярная масса серы Ms=32
32г(S) - 297 кДж
1000г(S) - Х
297 х 1000
Откуда, Х = ----------------- = 9280 кДж
Оценка качества угля включает 19 нормируемых показателей. К основным из них относятся: рабочая влажность угля, зольность, содержание серы, низшая теплота сгорания, спекаемость и коксуемость. В бурых углях количество влаги составляет 15-60%, в каменных -5-15%. Зольность определяется содержанием в угле минеральных примесей. Она колеблется в широких пределах -от 10 до 60%. Зольность углей Донецкого бассейна равна 10-15%.
Очень вредной примесью в углях является сера, сгорая, она образует сернистый газ (SO2), отравляющий окружающую среду. Содержание серы в углях колеблется в пределах 1-6%.
Низшая теплота сгорания бурых углей 6-15 МДж/кг, каменных 10-30 МДж/кг.
Спекаемость и коксуемость – свойство угля при нагревании без доступа воздуха расплавляться, а также образовывать пористый остаток – кокс, являющийся основным топливом для доменных печей при выплавке чугуна.
Вид и качество сырья предопределяют режим работы и производительность оборудования, характер технологии, влияют на качество и себестоимость продукции. Так, при выплавке чугуна на металлургическом заводе используются руды с различным содержанием железа. Повышенное содержание пустой породы и вредных примесей в рудах обусловливает уменьшение производительности доменного цеха, увеличение расхода топлива, флюсов и снижение качества чугуна.
2.4. Виды и основные характеристики топлива
Топливо– вещество, при сжигании которого выделяется значительное количество теплоты, используемое как источник получения тепловой энергии и как сырье в химической, металлургической и других отраслях промышленности.
Топливо, содержащее органические вещества, называют углеводородным.
Различают естественное и искусственное топливо. К естественным относятся ископаемые и растительные виды топлива, а к искусственным – продукты переработки естественных видов топлива. Все топлива по агрегатному состоянию подразделяются на твердые (ископаемые угли и сланцы, торф, древесина), жидкие (нефть, нефтепродукты) и газообразные (природный и попутный газы и др.).
Основной характеристикой топлива является его теплота сгорания, т.е. количество теплоты, выделяющееся при полном его сгорании. Различают теплоту сгорания удельную (МДж/кг) и объемную (МДж/м3).
По удельной теплоте сгорания (МДж/кг) виды топлива характеризуются следующим образом:
Топливо Уд. теплота сгорания
МДж/кг
Дрова 8,3-15,5
Горючий сланец 8,4 – 20
Торф 8,4 – 21
Бурый уголь 10,5 – 21
Каменный уголь ок. 29,4
Антрацит 32,8- 32,6
Природный горючий газ на 1 куб.м 25,2-46,2
Нефть 42
По энергетической ценности виды топлива характеризуются следующим образом:
Топливо Энергетическая ценность
КВт ч /кг
Дрова 2,33-4,32
Горючий сланец 2,33 – 5,82
Торф 2,33 – 4,66
Бурый уголь 2,92 -5,82
Каменный уголь ок. 8,15
Антрацит 9,08 – 9,32
Природный горючий газ на 1 куб.м 6,98 – 12,82
Нефть 11,63
Различные виды топлива соизмеряются по их удельной теплоте сгорания, т.е. по количеству энергии, виделяющейся при сжигании кило-грамма топлива.
Для исчисления общих запасов топлива различные его виды мысленно заменяют так называемым условным топливом с удельной теплотой сгорания 29,4 МДж/кг. Обозначив удельную теплоту сгорания данного топлива через Q, а его количество ( в килограммах или тоннах) через Т, найдем эквивалентное ему количество Х условного топлива по одной из следующих формул:
Х=ТQ /29,4 или Х=ТQ/ 8,15,
в зависимости от того, в каких единицах (МДж/кг или кВт·ч/кг) задана Q.
Практически при соответствующих расчетах принимают:
1т каменного угля = 1 т условного топлива
1т бурого угля = 0,4 т условного топлива
1т нефти = 1,4 условного топлива
1000 м3природного газа = 1,3 т условного топлива
Несколько сложнее соизмерение топливных и нетопливных энергетических ресурсов. Мощность гидроэнергии, измеряемая в киловаттах, зависит от высоты (напора) воды и ее расхода, т.е. количество воды, протекающей в выбранном створе реки в единицу времени. Ее исчисляют следующим образом.
Вода, падая с высоты, производит работу, равную произведению ее веса на высоту падения. Масса воды пропорциональна ее объему. Обозначив через R ее расход, т.е. количество кубометров воды, падающей за секунду, а через Н – высоту падения, выраженную в метрах, можно вычислить мощность N водного потока в киловаттах по следующей формуле:
N=(1000/102) RH=9,8 RH.
В этой формуле 1000 – число килограммов в кубометре воды, а 102 – число килограммометров в секунду, равное одному киловатту мощности.
Принимая средний коэффициент полезного действия гидроустановки равным 0,80-0,85, получаем практическое выражение для потенциальной (теоретической) мощности водного потока:
N= 8RH, кВт.
Понятие условного топлива применяют не только для исчисления общих отходов топлива, но и для исчисления энергетических ресурсов любого вида. Исходной величиной при этом служит среднее количество весовых единиц условного топлива, фактически расходуемых на тепловых электростанциях для получения одного киловатт-часа электроэнергии при данном уровне энергетической техники ( в настоящее время -около 0,35 кг). При помощи этой величины определяют какому количеству условного топлива эквивалентны ресурсы нетопливных источников энергии (количество киловатт-часов электроэнергии, которые можно получить от них за год).
Запасы гидроэнергии на определенной территории представляют сумму потенциальной мощности всех водотоков, умноженную на число часов возможного ее использования за год. Это потенциальные (теоретические) гидроэнергоресурсы. Наряду с ними различают: технически возможные к использованию гидроэнергоресурсы – часть потенциальных, которая при данном уровне техники практически может быть использована; экономически эффективные гидроэнергоресурсы, использование которых при существующих условиях экономически выгодно.
При соизмерении невозобновляющихся и возобновляющихся энергетических ресурсов необходимо учитывать скорость возобновления (прирост древесины, а иногда и торфа).
В состав всех видов топлива входит горючая масса (органическая масса и горючие неорганические вещества: сера, ее соединения и т.д.) и негорючая масса (зола, влага). Чем больше в топливе золы, влаги, тем ниже его теплота сгорания. Чем выше в органической массе содержание углерода и водорода и чем ниже содержание кислорода и азота, тем больше теплота сгорания топлива.
Одним из важнейших видов жидких топлив является нефть, которая содержит в органической части 83-87% углерода и 12-14% водорода. Удельная теплота сгорания нефти колеблется в пределах 35,8-44 МДж/кг.
Природный газ содержит до 98% метана и является наиболее эффективным видом топлива. В пределах Украины имеются практически все виды топлива, в том числе нефть и газ.
2.5. Основные источники и характеристики воды
Вода занимает важное место в жизни и деятельности человека. Распространение воды: 97,57% – в мировом океане, 2,14% – в высокогорных ледниках и полярных льдах, 0,29% – в реках и озерах, в водяных парах атмосферы – около 0,001%. Примерно 7% массы земной коры составляют подземные воды.
Для бытовых и промышленных нужд применяется только пресная вода (содержание солей до 1 г/л), составляющая 3% всех запасов воды.
Расход воды на душу населения в крупных городах США и Европы составляет 600-700л в сутки, в развивающихся странах – 50 л.
В воде содержатся почти все элементы системы Менделеева. Ее обшая масса 1,4х1018т, в ней содержится 2,8 млрд. т урана. Если извлечь из нее только 0,01% содержащегося урана, то его хватит на 100 лет для выработки электроэнергии для всего человечества.
Качество воды определяется ее химическими и физическими характеристиками, такими как жесткость, общее солесодержание, прозрачность, окисляемость и др. Для питьевых нужд большое значение имеет количество токсичных примесей (мышьяк, стронций, радий, радиактивный уран), содержание микробов, запах, цвет и вкус. Для технических нужд важны показатели жесткости, содержание солей, механических примесей.
Жесткость воды характеризуется содержанием в ней солей кальция и магния. Различают жесткость воды трех видов: временную, постоянную и общую.
Временная (устранимая) жесткость характеризуется содержанием в воде бикарбонатов кальция и магния, которые легко удаляются из воды простым кипячением. Бикарбонаты переходят в нерастворимые углекислые соли и выпадают в виде плотного осадка.
Постоянная жесткость воды связана с присутствием в ней хлоридов, сульфатов, нитратов кальция и магния. Эти соли не удаляются при кипячении воды. Временная и постоянная жесткость в сумме дают общую жесткость. Вода имеет жесткость, равную единице, если в литре ее содержится 1 мг-экв ионов кальция или магния. Жесткость вызывает агресивность по отношению к бетону. При содержании 250 млг/л сульфатных ионов наступает разрушение бетонного камня.
Общее солесодержание или сухой остаток – масса вещества, оставшегося после испарения воды и высушивания полученного остатка при 105...110°С до постоянной массы. Сухой остаток выражается в миллиграммах на 1 литр воды.
Прозрачность воды определяется толщиной слоя воды, через который можно различить крест или шрифт определенного размера (без или с помощью фотоэлемента). В открытых районах Черного моря она равна 24...28 м.
Окисляемость воды определяется массой (в миллиграммах) перманганата калия, взаимодействующего с 1 л воды при кипячении в течение 10 минут.
Кислотность или щелочность воды характеризуется концентрацией водородных ионов или величиной pH = – 1g [H+, моль/л].
При pH = 6,5 – 7,5 вода считается нейтральной, при pH < 6,5 воду называют кислотной, при pH > 7,5 – щелочной.
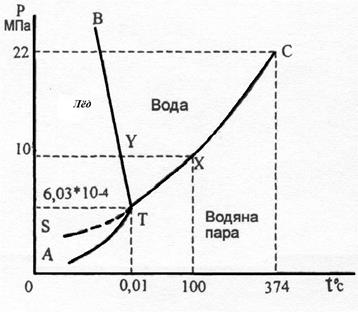
| |
Например, при определенных значениях темпера-туры и давления, которое соответствует точкам диаг-раммы в плоскости, огра-ниченной кривыми ВТ и СТ, вода существует только в жидком состоянии, в точках ниже кривых АТ и ТС – в виде пара.
Точки на кривых соответствуют условиям, при которых две смежные фазы находятся в равновесии.
Две точки на диаграмме вызывают особый интерес. Точка Т (0,01оС и 6,03·10-4МПа) называется тройной точкой, где в равновесии находятся одновременно три фазы: пар, вода и лед. Точка С (347оС и 22,0 МПа) называется критической. При температуре свыше 374оС пар воды нельзя преобразовать в жидкость при увеличении давления. Иными словами, при температуре и давлении свыше чем в точке С, пар и жидкость воды не различаются. Между ними не существует фазовой линии.
Диаграмма состояния воды играет исключительно важную роль при проектировании и эксплуатации паровых котлов, энергетических турбин энергосистем, автоклавов и т.д.
2.6. Классификация вод
Природные воды делятся на три вида, различающиеся по наличию примесей: атмосферные, поверхностные и подземные.
Атмосферная вода– это вода дождевых и снеговых осадков, она характеризуется сравнительно небольшим содержанием примесей, главным образом растворенных газов: кислорода, углекислого газа, сероводорода, оксидов азота, кислородных соединений серы, органических веществ, которые определяют атмосферу в промышленных районах. Атмосферная вода почти не содержит растворенных солей, в частности солей кальция и магния.
Поверхностные воды – речные, озерные, морские содержат, кроме примесей, имеющихся в атмосферной воде, разнообразные вещества. В ней есть двууглекислые соли кальция, магния, натрия и калия, а также сернокислые и хлорные соли. При содержании солей менее 1 грамма на литр воды она называется пресной, более одного грамма – соленой.
Подземные воды – артезианских скважин, колодцев, ключей, гейзеров – характеризуются разнообразным содержанием солей, состав которых зависит от вида и структуры почв и горных пород, через которые просачиваются атмосферные воды и воды поверхностных водоемов, образуя подземные водоемы. Фильтрующая способность почв и горных пород обусловливает высокую прозрачность подземных вод и отсутствие в них примесей органического происхождения. Уникальным сырьем для химической промышленности являются минеральные воды, насыщенные различными солями. Так, воды насыщенные хлористым натрием, служат сырьем для производства соды, едкого натра и хлора. Из подземных рассолов получают также йодистые, бромистые соединения и другие соли.
В зависимости от назначения вода условно подразделяется на промышленную и питьевую. Питьевая вода в первую очередь освобождается от бактерий; к ней предъявляются особые требования в отношении вкуса, цвета, запаха. Промышленные воды не должны содержать примесей больше допустимой нормы, которая устанавливается в зависимости от вида производства.
Вода для прямоточных паровых котлов не должна содержать окисей углерода и кислорода, вызывающих коррозийное разрушение труб, и может содержать сухой остаток не более 0,2...0,3 мг/л. Соли в паровых котлах отлагаются на внутренних поверхностях труб в виде накипи, снижают теплопроводность их стенок, приводят к перегреву труб и преждевременному их износу. Повышенные требования в отношении чистоты предъявляются к воде в производстве полупроводников, люминофоров и некоторых других материалов.
2.7 Очистка и обезвреживание воды
Очистка воды от примесей, т.е. подготовка, включает следующие операции: осветление, обесцвечивание, обеззараживание, смягчение, дегазацию.
Осветление и обесцвечивание природной воды производится с целью удаления из нее механических примесей. Это достигается отстаиванием ее в бетонированных резервуарах большой вместимости (отстойниках) с последующим пропусканием через песчаные фильтры с зернистым фильтрующим слоем. Для осаждения коллоидных примесей в отстойники вводят коагулянты – сульфаты железа или алюминия, в результате чего вода обесцвечивается. Осадки удаляются из воды при отстаивании и фильтровании.
Обеззараживание воды – обязательный процесс очистки воды, используемой для бытовых нужд. Уничтожение болезнетворных микробов и окисление органических примесей достигается хлорированием – введением газообразного хлора, хлорной извести, гипохлорида кальция, а также озонированием и кипячением. При обработке воды хлором вода приобретает его запах, при озонировании запах отсутствует, что является достоинством данного метода. Вода обеззараживается также обработкой ионами серебра и при воздействии ультрафиолетовых лучей и ультразвуковых колебаний.
Для того, чтобы после обработки в воде не оставался избыток хлора, ее дехлорируют. При этом избыток хлора либо химически связывается, либо удаляется при пропускании воды через угольные фильтры. Умягчение и обессоливание воды – основные процессы ее подготовки. Удаление из воды всех солей (всех катионов и анионов) называется обессоливанием, только солей кальция и магния – смягчением. Полное обессоливание воды (дистиллирование) применяется сравнительно редко. Способы умягчения воды подразделяются на физические, химические и физико-химические.
К физическим способам относятся – кипячение, дистилляция и вымораживание.
Дистиллированную (полностью обессоленную) воду получают перегонкой на специальных дистилляционных установках.
Сущность химических методов умягчения заключается в связывании ионов кальция и магния при помощи реагентов в нерастворимые и легкоудаляемые осадки. В зависимости от применяемых реагентов различают способы: а) известковый – обработка гашеной известью; б) содовый – воздействуют кальцинированной содой; г) натронный – обработка едким натром; д) фосфатный – воздействуют тринатрийфосфатом.
Сущность ионообменного (физико-химического) способа состоит в удалении из воды ионов кальция и магния при помощи ионитов (ионообменных солей), способных обменивать свои ионы на ионы, содержащиеся в воде.
Современным физико-химическим методом смягчения воды является электрохимический, в частности электрокоагуляция, которая производится в электролизерах с растворимыми электродами.
Дегазация воды– удаление из нее растворенных газов – осуществляется химическим и физическим способами.
Физические способы удаления газов заключаются в аэрации или нагревании воды в вакууме.
Производственные и бытовые сточные воды обычно содержат различные органические и неорганические примеси, которые при сливе в водоемы загрязняют их. Спуск промышленных сточных вод в водоемы производится в соответствии с санитарными правилами, которыми определено предельно допустимое содержание веществ в сточных водах.
Способы очистки и обезвреживания сточных водподразделяются на механические, физико-химические, химические и биологические.
Механические способы очистки сточных вод от примесей заключаются в их отстаивании и фильтровании, в частности, через полупроницаемые мембраны под давлением.
Физико-химические методы основаны на применении флотации, экстракции и адсорбции вредных примесей, отгонки их с водяным паром. Разновидностью физико-химических методов являются термические, например, испарение воды при нагревании и сжигании органической части сухого остатка.
Химические методы очистки сточных вод основаны на использовании окислительно-восстановительных, электрохимических процессов, реакций нейтрализации и перевода вредных веществ в неактивную безвредную форму. Биологический метод заключается в разложении и окислении вредных примесей с помощью микроорганизмов. Среди встречающихся в почве микроорганизмов наиболее многочисленными являются грибы, водоросли и бактерии. Они «атакуют» содержащиеся в сточных водах органические вещества, которые представляют собой прекрасную питательную среду для микробов, и разлагают углеводы, жиры и другие соединения на двуокись углерода, воду и минеральные соли. Различают процессы биологической очистки, протекающие в естественных и искусственно созданных условиях, проводимых на специальных очистных станциях.
2.8. Воздух в технологических процессах
Наряду с природной водой воздух широко используется в различных технологических процессах.
Прежде всего, воздух расходуется в энергетических агрегатах во время сжигания органических энергоносителей (угля, газа, мазута, бензина) – тепловых электростанциях и двигателях внутреннего сгорания. Большие объемы воздуха используют в металлургии: на производство 1т стали его расходуют около 15· 103 м3на 1т меди – примерно 60 · 103м3. Воздух широко используется для транспортирования материалов (пневмотранспорт), при теплопередаче и охлаждении технологических объектов, как рабочее тепло в пневматических системах. Некоторые физические характеристики атмосферного воздуха: плотность – 1,293 кг/м3; средняя молярная масса (условно) – 29; критическая температура – 140,7 0С, критическое давление 3,72 МПа
Существенную роль в промышленности играют отдельные составные воздуха, характеристики которых приведены в табл. 2.1.
Состав воздуха и его свойства
Таблица 2.1
| Складові | Вміст, % | Густина, кг/м³ | Температура кипіння, ºС | Молекулярна маса, а.о.м. |
| за об’ємом | за масою | |||
| Азот (N2) | 78,15 | 75,6 | 1,25 | –195 |











