Хронический панкреатит
Актуальность проблемы и распространенность заболевания
Панкреатит представляет собой тяжелое заболевание поджелудочной железы (ПЖ), в основе которого лежит внутриорганная активация продуцируемых железой пищеварительных ферментов и выраженное в различной степени ферментативное повреждение ткани (панкреонекроз), с последующим развитием фиброза, нередко распространяющееся на окружающие ткани (парапанкреофиброз), а также осложняемое вторичной инфекцией. Клинически панкреатит может протекать в острой и хронической формах, нередко тесно связанных между собой.
Хронический панкреатит (ХП) – это хроническое заболевание ПЖ, характеризующееся почти постоянно существующей симптоматикой вследствие воспаления и фиброза ПЖ, нередко сопровождающееся процессами кальцификации в железе. ХП приводит к развитию мальабсорбции и нарушению углеводного обмена.
На протяжении последних десятилетий распространенность ХП существенно возросла, и он приобрел важное медико‑социальное значение.
Этиология и патогенез
Известно более 140 факторов, способных вызвать панкреатит или способствовать его возникновению. Однако у подавляющего числа хирургических больных панкреатит бывает связан с тремя основными факторами, каждый из которых может играть этиологическую роль как при острой, так и при хронической формах заболевания. Факторы эти следующие (в порядке значимости):
1. Длительное и неумеренное употребление алкоголя (алкоголизм).
2. Заболевания соседних с ПЖ органов, в первую очередь, желчных путей (холелитиаз), реже двенадцатиперстной кишки и других.
3. Так называемая случайная, а также операционная травма.
Считается, что с алкоголизмом связано более половины случаев острого, примерно 3/4 случаев ХП, причем быстрый рост распространенности алкоголизма, особенно в нашей стране, определяет резкое увеличение заболеваемости панкреатитом за последние десятилетия, в частности, у мужчин молодого и среднего возраста.
Желчно‑каменная болезнь является второй по значению причиной панкреатита, которая играет преимущественную роль у женщин среднего и пожилого возраста. Хорошо известно, что на протяжении длительного времени в развитых странах наблюдался выраженный рост числа больных холелитиазом, что также в значительной мере определяет увеличение частоты связанного с ним панкреатита.
По сравнению с первыми двумя причинами, травма, как «случайная», в том числе криминальная, так и операционная, имеет меньшее значение и первично вызывает, как правило, острый панкреатит, который в дальнейшем может трансформироваться в хронические формы. В качестве этиологического фактора травма может оказывать на железу как прямое, так и косвенное воздействие. При прямом воздействии происходит непосредственное повреждение ткани железы под влиянием механической силы (закрытая или проникающая травма живота, операции на самой железе или окружающих ее органах, в особенности на дуоденальном соске). Косвенное воздействие травмы обычно связано с микроциркуляторными ишемическими расстройствами в железе при травматическом шоке, а также с длительным или несовершенным искусственным кровообращением при кардиохирургических операциях. Число травматических панкреатитов также склонно к увеличению вследствие роста криминального травматизма, количества и сложности оперативных вмешательств на ПЖ, в частности, по поводу резко участившегося рака этого органа, а также все более широкого распространения эндоскопических манипуляций и оперативных вмешательств на большом дуоденальном сосочке (ретроградная холангиопанкреатикография (РХПГ), эндоскопическая папиллосфинктеротомия (ЭПСТ)).
Таким образом, воздействие на население всех трех главных причин панкреатита усилилось в чрезвычайно большой степени, что объясняет огромный рост распространенности заболевания на протяжении XX века. В начале столетия панкреатит считался редкой болезнью, а крупнейший в то время авторитет в области диагностики и хирургического лечения острых заболеваний живота французский хирург А. Мондор (1916) гордился, что ему за много лет практики удалось дважды прижизненно распознать острый панкреатит. В настоящее же время даже начинающий хирург, работающий в системе скорой помощи, может похвалиться таким же или даже большим достижением в течение одной недели, а то и одного дежурства.
Многочисленные прочие факторы, считающиеся причиной или же способствующие развитию панкреатита, имеют меньшее значение, редко вызывают поражения ПЖ, в особенности требующие внимания хирурга. К более известным из этих факторов относят: 1) эндокринные заболевания (первичный гиперпаратиреоз, болезнь Кушинга); 2) гиперлипидемии и гиперглицеридемии, в частности осложняющие беременность, а также иного генеза; 3) лекарственные препараты (пероральные контрацептивы, кортикостероиды, азатиоприн и другие иммуносупрессоры); 4) аллергические и аутоиммунные факторы; 5) наследственные болезни (кистозный фиброз поджелудочной железы как проявление муковисцидоза, генетически обусловленные болезни обмена и ферментопатии, в частности врожденный дефицит кальций‑стабилизирующего фактора, способствующий увеличению вязкости панкреатического секрета и образованию обызвествленных конкрементов в панкреатическом протоке, и др.);
6) ишемия ПЖ, в частности связанная с компрессионным стенозом чревного ствола и другими причинами; 7) паразитарные заболевания (аскаридоз и др.).
Как это ни парадоксально, общепринятое и клинически, несомненно, целесообразное подразделение панкреатита на острый и хронический не имеет под собой четкого патогенетического основания, по крайней мере, для подавляющего большинства случаев болезни. В самом деле, безусловно, острым, иначе говоря, возникающим под влиянием острого воздействия в здоровом до этого воздействия органе, можно считать уже упоминавшийся панкреатит, связанный с травмой ПЖ, в том числе операционной. К острому в патогенетическом смысле панкреатиту можно отнести еще и панкреатит, обусловленный, например, случайным заползанием в фатеров сосочек кишечных гельминтов (аскарид), наблюдающийся почти исключительно в тропических странах, в частности, Юго‑Восточной Азии. В то же время при наиболее часто встречающихся формах панкреатита, связанных с алкоголизмом или холелитиазом, при которых причиной заболевания является фактор, постоянно действующий на протяжении многих лет, дело обстоит значительно сложнее.
Представляет интерес также и то обстоятельство, что у больных, погибших в ранние сроки от типичного острого панкреатита алкогольного или билиарного генеза, в ПЖ, наряду с острыми изменениями (массивный панкреонекроз, нагноение), нередко выявляются элементы хронического воспаления и фиброза, предшествовавшие острому фатально закончившемуся заболеванию. Во многих случаях у больных с клинически выраженным ХП возникает обострение, представляющее собой тяжелый панкреонекроз, дающий и клиническую картину, и осложнения, типичные для острого деструктивного панкреатита, который иногда заканчивается летальным исходом.
Патогенез панкреатита сложен и выяснен далеко не полностью. Рассмотрим кратко основные черты патогенеза панкреатита, не касаясь проблемы тяжелых системных полиорганных нарушений, свойственных, главным образом, острой форме заболевания.
Можно считать общепризнанным, что в основе патогенеза панкреатита у подавляющего большинства больных лежит повреждение ткани железы ею же продуцируемыми пищеварительными ферментами. В норме эти ферменты выделяются в неактивном состоянии (кроме амилазы и некоторых фракций липазы) и становятся активными лишь после попадания в двенадцатиперстную кишку. Большинство современных авторов выделяют три главных патогенетических фактора, способствующих аутоагрессии ферментов в секретирующем их органе: 1) затруднение оттока секрета железы в двенадцатиперстную кишку и внутрипротоковая гипертензия; 2) ненормально высокие объем и ферментативная активность сока ПЖ; 3) рефлюкс в протоковую систему железы содержимого двенадцатиперстной кишки и желчи.
Длительное время основным ферментом, виновным в повреждении ткани ПЖ при панкреатите, считался трипсин (после активации его предшественника трипсиногена цитокиназой поврежденных клеток или энтерокиназой двенадцатиперстной кишки). В последнее время значительно большее значение придается фосфолипазе А, активируемой из профермента желчными кислотами и другими факторами, в частности трипсином. Этот фермент способен разрушать живые ацинарные клетки, расщепляя их фосфолипидные мембраны. Липазы ответственны за возникновение основной массы панкреатического и парапанкреатического некроза (стеатонекроз). Трипсин же и другие активированные протеолитические ферменты (эластаза, коллагеназа, калликреин) расщепляют преимущественно внеклеточные элементы соединительной ткани, причем важным объектом их воздействия являются сосуды интерстиция ПЖ, с чем связывают геморрагический характер панкреонекроза у части больных.
Механизмы патологической внутриорганной активации ферментов и повреждения ткани железы различаются в зависимости от причины панкреатита. Так, известно, что алкоголь, особенно в больших дозах, рефлекторным и гуморальным путем резко повышает объем и активность панкреатического сока. К этому добавляется стимулирующее действие и алиментарного фактора. Кроме того, алкоголь способствует спазму сфинктера печеночно‑панкреатической ампулы (сфинктера Одди), вызывает повышение вязкости панкреатического секрета, образование в нем белковых преципитатов, в дальнейшем трансформирующихся в конкременты, характерные для хронической формы заболевания. Все это затрудняет отток секрета и ведет к внутрипротоковой гипертензии, которая при уровне, превышающем 35–40 см вод. ст. способна обусловить повреждение клеток эпителия протоков и ацинусов и освобождение цитокиназ, запускающих механизм активации ферментов. Спазм сфинктера Одди ведет к желчно‑панкреатическому рефлюксу и внутрипротоковой активации ферментов за счет желчных кислот. Не исключается также и прямое повреждающее действие высоких концентраций алкоголя в крови на железистые клетки.
При панкреатите, связанном с заболеваниями желчных путей, главным патогенетическим фактором является нарушение оттока панкреатического сока в двенадцатиперстную кишку, что связано, прежде всего, с наличием уже упоминавшегося «общего канала», через который отходят желчные конкременты и куда обычно впадает главный панкреатический проток. Из литературы известно, что при раздельном впадении желчного и панкреатических протоков, а также при отдельном впадении в двенадцатиперстную кишку добавочного (санториниева) протока, сообщающегося с главным протоком ПЖ, билиарный панкреатит не развивается.
Проходя через фатерову ампулу, желчные конкременты временно задерживаются в ней, вызывая спазм сфинктера Одди и преходящую протоковую гипертензию, обусловливающую ферментативное повреждение ткани железы и, возможно, приступ острого панкреатита, в ряде случаев протекающий малосимптомно или же маскирующийся приступом желчной колики. Повторное «проталкивание» желчных камней через ампулу за счет высокого панкреатического и билиарного давления может привести к травме слизистой дуоденального сосочка и стенозирующему папиллиту, все более затрудняющему пассаж желчи и панкреатического сока, а также и повторное отхождение камней. Иногда наступает стойкое ущемление желчного конкремента в ампуле, ведущее к обтурационной желтухе и тяжелому панкреонекрозу.
Определенную роль при рассматриваемой форме панкреатита может играть и рефлюкс желчи в панкреатический проток, причем при наличии холангита микробные энзимы, по‑видимому, также способствуют активации панкреатических ферментов.
Самостоятельную роль в патогенезе панкреатита могут играть также заболевания двенадцатиперстной кишки, связанные с дуоденостазом и гипертензией в ее просвете и способствующие рефлюксу дуоденального содержимого в панкреатический проток (в том числе «синдром приводящей петли» после резекции желудка по типу Бильрот II). Некоторые авторы указывают и на значение дивертикулов двенадцатиперстной кишки, в особенности перипапиллярных, которые могут обусловливать как спазм, так и (редко) атонию сфинктера Одди.
Как уже упоминалось, травматический панкреатит может быть связан как с прямым, так и с опосредованным воздействием на ПЖ. При прямой травме к внутриорганной активации ферментов ведет механическое повреждение железы с выделением из омертвевающих клеток уже упоминавшихся активаторов (цитокиназ) и последующим развитием в дополнение к травматическому еще и ферментативного панкреонекроза. При эндоскопических вмешательствах на большом дуоденальном сосочке часто травмируется слизистая оболочка фатеровой ампулы и терминального отдела главного панкреатического протока. В результате травмы, кровоизлияний и реактивного отека может затрудняться отток панкреатического секрета и развиваться протоковая гипертензия, роль которой в патогенезе панкреатита уже рассматривалась. Стенки протока могут повреждаться и от избыточного давления при введении контрастного вещества при РХПГ.
При опосредованном воздействии случайных и операционных травм на ПЖ (травматический шок, кровопотеря, кардиохирургические вмешательства с длительной перфузией) повреждение железистой ткани с высвобождением активирующих клеточных факторов связано в основном с микроциркуляторными расстройствами и соответствующей гипоксией.
Следует обратить внимание на еще один важный аспект патогенеза ХП, недостаточно освещаемый в литературе. По представлениям большинства клиницистов, панкреонекроз считается определяющей особенностью наиболее тяжелых форм острого деструктивного панкреатита. Однако повреждение и гибель (омертвение, некроз) ткани ПЖ под воздействием внутриорганной активации и аутоагрессии пищеварительных ферментов определяет возникновение и течение любых, в том числе и хронических, форм рассматриваемого заболевания. Так, хорошо известно, что при наиболее часто встречающейся так называемой отечной форме острого панкреатита, обычно противопоставляемой формам деструктивным, в железе, наряду с отеком, имеется множество мелких и мельчайших очагов омертвения, то есть мелкоочаговый панкреонекроз.
При ХП, не являющемся следствием острого, также имеет место ферментативное повреждение, некробиоз, некроз и аутолиз панкреатоцитов, происходящее как постепенно, под влиянием длительно действующего фактора, так и остро скачкообразно в период обострений хронического процесса.
В соответствии с законами общей патологии, судьба омертвевшей ткани в организме может быть троякой. Некротизированный участок может подвергнуться: а) рассасыванию (резорбции) с организацией омертвевшего субстрата новообразованной соединительной тканью;
б) инкапсуляции с образованием вокруг некротического очага фиброзной капсулы, отграничивающей его от жизнеспособной ткани;
в) отторжению с удалением (или тенденцией к удалению) омертвевшей ткани из организма больного. Исключением из этого правила является некроз тканей, сообщающихся с внешней средой (кожа, стенки желудочно‑кишечного тракта), когда рассасывание с организацией или инкапсуляция исключаются и возможно только отторжение. Важно хорошо понимать, что именно судьба (исход) панкреонекроза, как правило, определяет форму панкреатита и особенности его течения.
Существует хорошо выраженная закономерность, в соответствии с которой судьба омертвевшей ткани находится в четкой зависимости от объема некротического субстрата. Так, мелкие очаги склонны к резорбции или стойкой инкапсуляции, крупные – к нестойкой инкапсуляции и отторжению, причем в последнем играет роль вторичная инфекция.
Рассасывание мелких диссеминированных очагов панкреонекроза с организацией их рубцовой тканью ведет к склерозированию железы, сдавлению ацинусов, деформации и рубцовым стриктурам выводных протоков, что играет важную роль в нарушении оттока секрета и патогенезе ХП вообще. Прогрессирование рубцового процесса в железе может привести к значительному снижению как внешне‑, так и внутрисекреторной деятельности ее функции (расстройства пищеварения, диабет), а также к сдавлению проходящего через толщу головки ПЖ общего желчного протока (обтурационная желтуха), воротной вены или ДПК.
В случае инкапсуляции мелких очагов некроза часто возникает их вторичное обызвествление, особенно характерное для алкогольного ХП, а также для панкреатитов, связанных с нарушениями кальциевого обмена (гиперпаратиреоз, дефицит кальций‑стабилизирующего фактора). Обызвествление паренхимы ПЖ при ХП является косвенным доказательством перенесенного в прошлом мелкоочагового панкреонекроза, поскольку соли кальция обычно откладываются в девитализированную, омертвевшую ткань, например, в лимфоузлы при туберкулезном бронхоадените. Инкапсуляция, как и резорбция очагов панкреонекроза, связана со склерозированием ткани железы и его последствиями, о которых писалось выше.
Более крупные очаги панкреонекроза при его исходе в инкапсуляцию в ряде случаев могут протекать асептично и трансформироваться в ложную панкреатическую, парапанкреатическую или комбинированную кисту с фиброзными стенками, выполненную вначале некротизированной тканью, а после ее постепенной деградации и растворения – мутной, постепенно просветляющейся жидкостью, часто содержащей ферменты панкреатического секрета. Присоединение, как правило, маловирулентной инфекции обусловливает возникновение вялотекущего панкреатического или парапанкреатического абсцесса, обычно содержащего гной и элементы панкреонекроза, находящегося на различных стадиях деградации. Впрочем, присоединение инфекционного воспаления в принципе означает изменение судьбы некротизированной ткани и переход от нестойкой инкапсуляции к отторжению. Вместе с тем, особенности топографической анатомии ПЖ (глубина расположения), а также труднообъяснимая замедленность расплавления панкреонекроза, находящегося под сочетанным воздействием пищеварительных и микробных протеаз, делают самопроизвольное отторжение некротического субстрата практически невозможным, тогда как затруднения в процессе отторжения и его незавершенность являются важнейшими факторами рецидивирующего течения ХП и возникновения тяжелых осложнений.
Классификация хронического панкреатита
Предложено множество классификаций ХП. С нашей точки зрения, более удобен вариант классификации ХП, предложенный профессорами Н.Н. Артемьевой и Н.В. Путовым, так как эта классификация не только отражает этиологию и патогенез заболевания, но и учитывает факторы, важные с клинической точки зрения.
В зависимости от причины заболевания ХП может быть: 1) алкогольным, 2) холангиогенным (связанным с заболеваниями желчных путей), 3) травматическим, 4) обусловленным прочими факторами.
По характеру морфологических изменений в паренхиме железы следует выделять: 1) диффузно‑склерозирующий ХП и 2) ХП с наличием полостных образований (инкапсулированные очаги панкреонекроза, ложные кисты, вялотекущие абсцессы). Оба эти основные типа могут протекать: а) без кальцификации, б) с кальцификацией паренхимы железы.
По состоянию протоковой системы следует выделять: 1) ХП без признаков протоковой гипертензии, 2) ХП с признаками протоковой гипертензии, в том числе: а) без наличия внутрипротоковых конкрементов, б) с наличием внутрипротоковых конкрементов.
По распространенности бывают: 1) регионарные ХП с преимущественной локализацией изменений: а) в головке ПЖ, б) в теле ПЖ, в) в хвосте ПЖ (возможны сочетания); 2) субтотальные ХП;
з) тотальные ХП. Кроме того, выделяют также ХП: а) без выраженного поражения парапанкреатической клетчатки (парапанкреатита) и б) ХП с выраженным поражением парапанкреатической клетчатки.
В клиническом аспекте можно выделить: 1) первично хронический панкреатит, 2) резидуальный (остаточный) ХП, являющийся продолжением острого панкреатита.
Течение ХП может быть: 1) монотонным, 2) периодически обостряющимся с фазами: а) обострения, б) ремиссии, 3) латентным (в т. ч. при многолетней ремиссии).
Можно различать ХП в зависимости от наличия осложнений и их характера: 1) ХП без осложнений, 2) ХП, осложненный: а) острым массивным панкреонекрозом, б) панкреатическим свищом, в) обтурационной желтухой и/или холангитом, г) нарушением проходимости двенадцатиперстной кишки, д) портальной гипертензией, е) кровотечением, ж) алиментарным истощением, з) сахарным диабетом, и) прочими осложнениями.
Клиническая картина и данные объективного исследования
Наиболее частым и относительно ранним проявлением ХП является болевой синдром. Боль, как правило, значительной или резко выраженной интенсивности бывает связана с нарушением оттока панкреатических соков и протоковой гипертензией, хроническим воспалительным процессом в железе асептического или инфекционного происхождения, а также с вовлечением в рубцововоспалительные изменения забрюшинных нервных сплетений и сосудов, обеспечивающих кровообращение в ПЖ (ишемия). Боль обычно локализуется в эпигастральной области, иногда ближе к левому или правому подреберью, нередко иррадиирует в поясницу или имеет опоясывающий характер. Локализация болевых ощущений может зависеть от расположения зоны наибольшего или преимущественного поражения железы (головка, тело, хвост). Иногда боль бывает монотонной, но у большинства больных связана с приемом пищи и начинается или усиливается через час и более после еды. В ряде случаев отмечаются преимущественно ночные боли. При рецидивирующем панкреатите боли могут появляться только в период обострений или же усиливаться в эти периоды.
Характерным для болей при ХП считается то, что они склонны усиливаться в положении больного на спине и ослабевать при перемене положения тела. Прием алкоголя иногда временно ослабляет болевой синдром, однако у большинства больных способствует его усилению. При ХП, связанном с холелитиазом, панкреатогенные боли могут сочетаться с болями в правом подреберье, характерными для холецистита.
У больных с так называемым безболевым ХП или латентным его течением (чаще при алкогольном ХП) боли могут быть незначительными или же длительное время отсутствовать вовсе, что, по всей вероятности, может быть связано с отсутствием выраженной протоковой гипертензии. Клинические проявления у этой группы больных нередко связаны преимущественно со снижением внешней или же внутренней секреции ПЖ.
Группа часто встречающихся симптомов ХП зависит от ферментативной недостаточности железы и соответствующих расстройств пищеварения. Так, почти одновременно с болями у большинства пациентов возникают жалобы на вздутие и распирание живота, а иногда слюнотечение после приема пищи. Эти симптомы усиливаются при нарушениях диеты и после приема алкоголя. Характерным является также расстройство стула. В типичных случаях в начале возникают запоры, которые затем сменяются неустойчивым стулом с чередованием запоров и поносов. При нередко наблюдаемой стеаторее каловые массы приобретают сероватую окраску, характерный жирный блеск и могут содержать частицы непереваренной пищи. В тяжелых случаях может возникнуть упорный обильный понос с жидким водянистым стулом, содержащим жировые капли. Аппетит при этом бывает сохранен, а у некоторых больных даже повышен.
Расстройства пищеварения, состоящие в нарушениях переваривания и утилизации пищевых веществ и витаминов, ведут к снижению массы тела и алиментарному истощению больных, сопровождающемуся гиповитаминозом.
При возникновении в зоне железы вторичного инфекционного процесса (обычно при панкреатите, связанном с формированием патологических полостей – нагноившихся ложных кист) возникает лихорадка, иногда сопровождаемая познабливанием и потами, и связанное с этим общее недомогание, а также усиление болевых ощущений в области патологического очага. В случае вторичного нарушения пассажа желчи из‑за сдавления терминального отдела холедоха увеличенной и уплотненной головкой железы или кистой появляется желтуха, а при холангите – лихорадка, тяжесть и болезненность в правом подреберье. При сдавлении двенадцатиперстной кишки может отмечаться ускоренное чувство насыщения, тошнота и рвота после приема пищи. При крупных панкреатических и парапанкреатических кистах больные иногда жалуются на асимметрию живота, болезненное выбухание в его верхнем отделе (см. ниже).
Осложнение псевдокисты или хронического абсцесса железы кровотечением проявляется хорошо известными общими симптомами кровопотери, а при наличии сообщения между полостью и просветом желудочно‑кишечного тракта (чаще всего псевдоцисто‑дуоденальный свищ) появляется обильный дегтеобразный стул. Боли иногда усиливаются, причем в области кисты начинает пальпироваться или увеличиваться образование.
Жалобы, связанные с эндокринной недостаточностью ПЖ, возникают обычно поздно, и не всегда привлекают внимание больного. Причиной этого может быть снижение потребности в инсулине из‑за нарушения всасывания углеводов, а также и с тем, что в островковом аппарате одновременно с инсулином по тем же причинам уменьшается и секреция его антагониста – глюкагона, а это способствует стабилизации содержания глюкозы в крови и «мягкому» течению диабета у ряда больных ХП.
Анамнез больных ХП чаще всего достаточно характерен. У большинства из них в течение нескольких лет до появления расстройств, связанных с патологией ПЖ, отмечается неумеренное потребление алкоголя вследствие выраженной алкогольной зависимости (алкоголизм) или же так называемого бытового пьянства. Хотя во многих случаях больные стремятся скрыть от врача истинное количество потребляемого ими алкоголя, нельзя все же исключить, что иногда алкогольный ХП может быть и от приема умеренных доз крепких напитков, и явиться следствием индивидуально повышенной чувствительности к ним поджелудочной железы.
У количественно меньшей группы больных, в которой преобладают женщины среднего и пожилого возраста, в анамнезе отмечаются проявления желчно‑каменной болезни, в том числе осложнявшейся эпизодами обтурационной желтухи и/или холангита, наличие так называемого постхолецистэктомического синдрома, часто связанного с резидуальным холедохолитиазом. Иногда, впрочем, желчно‑каменная болезнь, осложнившаяся ХП, может протекать без классических симптомов, и холецисто– или даже холедохолитиаз диагностируются у больного ХП лишь при специальном исследовании.
Еще реже в анамнезе отмечается закрытая или открытая травма ПЖ, операции на железе или соседних с ней органах, эндоскопические вмешательства на большом дуоденальном сосочке и т. д.
У еще меньшего числа больных в анамнезе устанавливаются другие эндогенные или экзогенные факторы, могущие быть причиной или же способствовать возникновению ХП (гиперпаратиреоз, муковисцидоз, наследственные нарушения обмена веществ, систематический прием некоторых упоминавшихся выше медикаментов и др.).
При объективном клиническом исследовании больного неосложненным ХП относительно редко удается выявить специфичные для этого заболевания признаки. При осмотре у значительной части больных отмечается пониженное питание, бледный, иногда с желтушным или землистым оттенком цвет кожи лица, язык с беловатым налетом.
При перкуссии и аускультации груди в редких случаях выявляется выпот, локализующийся чаще в левой плевральной полости и связанный либо с панкреатико‑плевральным свищом, либо с нагноением панкреатической или парапанкреатической псевдокисты, расположенной под левым куполом диафрагмы. Плевральный выпот в последнем случае называют реактивным.
Асимметричное увеличение объема живота в верхнем отделе можно наблюдать при наличии крупной панкреатической или парапанкреатической псевдокисты (см. ниже).
Наличие асцита, обусловливающего общее увеличение размеров живота и перемещающуюся при перемене положения перкуторную тупость в отлогих его отделах, бывает связано с вторичной портальной гипертензией, которая развивается в результате вовлечения в рубцово‑воспалительный процесс и/или тромбоза воротной вены и ее главных притоков (верхняя брыжеечная и селезеночная вены), проходящих в непосредственной близости от поджелудочной железы (подпеченочный портальный блок). В этом случае асциту обычно предшествует и сопутствует спленомегалия, определяемая пальпаторно или перкуторно.
Пальпировать саму патологически измененную ПЖ удается, главным образом, у истощенных больных в виде поперечно расположенного в эпигастрии болезненного валика, а также при наличии в ней значительных по размеру полостных образований (псевдокисты, вялотекущие абсцессы), в том числе являющихся субстратом так называемой опухолевидной формы ХП. Иногда обращает на себя внимание несоответствие между интенсивным болевым синдромом и незначительной болезненностью, провоцируемой пальпацией.
В случае обтурационной желтухи, связанной с увеличением и уплотнением головки ПЖ, окружающей терминальный отдел общего желчного протока, иногда удается пальпировать увеличенный и безболезненный желчный пузырь (вариант симптома Курвуазье), а при нарушении проходимости двенадцатиперстной кишки – растянутый желудок с провоцируемым феноменом шума плеска.
Иногда в области мечевидного отростка выслушивается систолический шум, свидетельствующий о компрессионном стенозе чревного ствола, могущем обусловить ишемию ПЖ (и других органов верхнего отдела живота) и, как уже упоминалось, иметь отношение к патогенезу ХП. При этом компрессия сосуда бывает врожденной (на уровне пищеводного отверстия диафрагмы) или же вторичной, связанной с рубцовыми изменениями в парапанкреатической клетчатке, вокруг чревного ствола.
Лабораторная и инструментальная диагностика
При исследовании больных с подозрением на ХП лабораторные данные имеют вспомогательное диагностическое значение. В общем анализе крови может выявляться та или иная степень анемии, а также фазовые изменения, характерные для обострения инфекционновоспалительного процесса (лейкоцитоз, сдвиг нейтрофильной формулы влево, увеличение СОЭ). При биохимическом анализе у истощенных больных обнаруживается гипопротеинемия, а при вторичном диабете – гипергликемия. При монотонно текущем ХП повышения ферментов в крови, в частности гиперамилаземии, может не наблюдаться, а при обострениях уровень ферментов, как правило, повышается, причем иногда до высоких цифр. Соответствующее этому повышение уровня ферментов наблюдается и в моче.
В кале при стеаторее обнаруживают нейтральный жир и мыла, причем содержание желчных кислот оценивается нормальным (разумеется, при нормальной проходимости желчных путей). При креаторее, связанной с недостаточным ферментативным расщеплением белков, в кале содержатся малоизмененные мышечные волокна. Современным методом оценки внешнесекреторной функции ПЖ является эластазный тест (фермент продуцируется ацинарными клетками железы, в процессе пассажа по кишечнику не разрушается, поэтому определение его концентрации в кале является объективным критерием оценки состояния экзокринной функции железы.) Некоторое диагностическое значение имеет исследование ферментов (преимущественно амилазы) в пунктатах содержимого ложных кист, а также в плевральном экссудате, иногда осложняющем течение ХП.
Обзорная рентгенография верхнего отдела брюшной полости имеет больше академическое значение в диагностике ХП, однако, характерные изменения удается выявить лишь у больных с выраженным обызвествлением паренхимы железы и/или достаточно крупными обызвествленными конкрементами в панкреатическом протоке (рис. 131).
Ретроградная холангиопанкреатикография (РХПГ), позволяющая контрастировать вирсунгов проток, выполняется в ходе эндоскопического исследования (подробнее см. ниже) (рис. 132).
Контрастное исследование желчных путей (холангиография) необходимо, в первую очередь, больным с билиарным ХП или подозрением на таковой. Она осуществляется либо непрямым методом с пероральным или внутривенным введением контрастного вещества, который, к сожалению, не обеспечивает достаточное качество снимков и вообще неприменим у больных с обтурацией желчных путей, либо методом прямого контрастирования. Последнее достигается при уже упоминавшейся РХПГ, а также с помощью чрескожной чреспеченочной пункции желчного пузыря, в том числе под контролем УЗИ, КТ или лапароскопа (рис. 133).
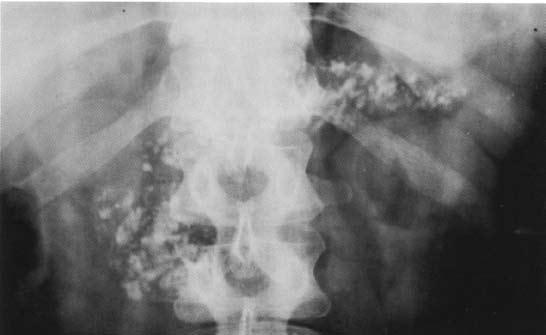
Рис. 131. Обзорная рентгенограмма органов брюшной полости (поджелудочной железы) при хроническом кальцифицирующем панкреатите. На снимке видны крупные кальцинаты в проекции поджелудочной железы на всем протяжении (во всех отделах поджелудочной железы) 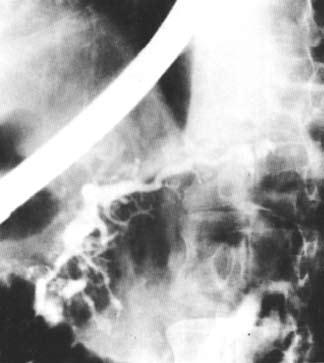
Рис. 132. Ретроградная панкреатикография при хроническом панкреатите. На снимке виден резко расширенный главный панкреатический проток
При блокированном камнями или отсутствующем (после холецистэктомии) пузыре возможно введение контрастного вещества путем пункции внутрипеченочных желчных протоков. В случае наличия желчного свища контрастирование достигается в результате фистулографии. 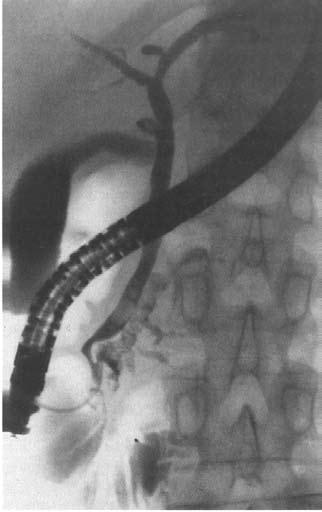
Рис. 133. Ретроградная холангиопанкреа‑тография. Контрастированы желчные протоки и желчный пузырь и главный панкреатический проток. Имеется продленное сужение (симптом «мышиного хвостика») терминального отдела общего желчного протока (панкреатическая часть) и резкое расширение главного панкреатического протока с нечеткостью его контуров
На основании холангиографии можно судить о наличии желчных конкрементов, расширении, деформации или стенозировании желчных путей, наличии препятствий для оттока желчи в двенадцатиперстную кишку. Существенное диагностическое значение имеет рентгенологическое исследование желудка и особенно двенадцатиперстной кишки.
При рентгенографии желудка исключаются его органические поражения, могущие иметь отношение к патогенезу панкреатита, и иногда выявляются деформации, связанные с изменениями в ПЖ, например, вдавления при наличии псевдокист, опухолевидной формы ХП и т. д. (рис. 134).
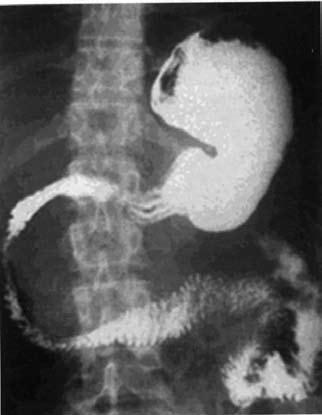
Рис. 134. Деформация контура выходного отдела желудка и разворот двенадцатиперстной кишки при кисте головки ПЖ
Дуоденография дает возможность судить о свободном пассаже бария через двенадцатиперстную кишку или же о наличии дуоденостаза, как уже упоминалось, имеющего значение в патогенезе ХП. Информативным методом является рентгенологическое исследование двенадцатиперстной кишки в условиях медикаментозной (искусственной) гипотонии, достигаемой предварительным введением спазмолитиков, например, атропина. Характерными признаками ХП, выявлению которых способствует гипотония, является расширение подковы двенадцатиперстной кишки вследствие увеличения размеров головки поджелудочной железы, наличие на медиальной стенке нисходящего отдела кишки широкого дефекта наполнения, иногда стенозирующего просвет и затрудняющего пассаж бария (рис. 135). 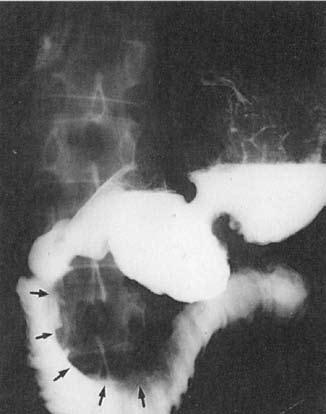
Рис. 135. Дуоденография с гипотонией. На снимке видно расширение подковы двенадцатиперстной кишки и сдавление кишки на уровне нисходящей и нижней горизонтальной ее ветвей увеличенной головкой поджелудочной железы
Фиброгастродуоденоскопия (ФГДС) и ретроградная холангио‑панкреатикография (РХПГ) позволяют визуально выявить изменения в двенадцатиперстной кишке, большом дуоденальном сосочке, а также контрастировать панкреатический и желчные протоки. Для выполн
Дата добавления: 2016-12-16; просмотров: 2037;











