Фуллерены и их производные
Одним из самых изучаемых объектов в химии за последние 20 лет стали фуллерены. Так называют аллотропную модификацию углерода состава Cn (n >20), молекулы которой имеют форму сферических много-гранников. Самой устойчивой из них является молекула, содержащая 60 атомов углерода, C60, которую и называют собственно фуллереном. Фуллерен обладает многими необычными физическими и химическими свойствами, которые делают его очень перспективным объектом как для научных исследований, так и для создания нанотехнологий.
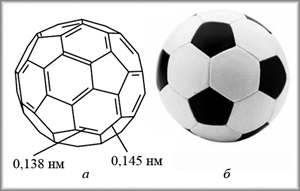
Свойства веществ определяются их строением. Рассмотрим сначала строение молекулы фуллерена. Ее называют «самой круглой молекулой, найденной в природе» (рис. 4,а). Радиус сферы составляет 0,357 нм. По форме и расположению пентагонов и гексагонов молекула совершенно аналогична футбольному мячу (рис. 4, б).
|
| Рис. 4. Молекула фуллерена C60 (а) и футбольный мяч (б) |
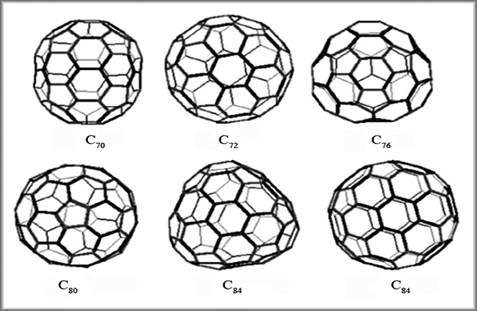
Молекулы других фуллеренов имеют далеко не столь симметричную форму (рис. 5) и термодинамически менее устойчивы, чем C60. Это обстоятельство имеет важное значение для получения последнего.
|
| Рис. 5. Некоторые высшие представители семейства фуллеренов |
Все атомы углерода в C60 находятся в sp2-гибридном состоянии. Каждый атом соединен с тремя соседями одинарными 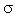 -связями. Четвертый электрон участвует в образовании общей p-электронной системы молекулы. В фуллерене можно выделить двойные и одинарные связи (см. рис. 4, а), их длины составляют 0,138 и 0,145 нм соответственно. Поэтому, а также в силу неплоской структуры, фуллерен не считают ароматической молекулой. Напротив, его рассматривают как сферический полиалкен, т.к. он содержит 30 двойных связей, слабо сопряженных между собой. Все они сосредоточены исключительно в шестичленных циклах.
-связями. Четвертый электрон участвует в образовании общей p-электронной системы молекулы. В фуллерене можно выделить двойные и одинарные связи (см. рис. 4, а), их длины составляют 0,138 и 0,145 нм соответственно. Поэтому, а также в силу неплоской структуры, фуллерен не считают ароматической молекулой. Напротив, его рассматривают как сферический полиалкен, т.к. он содержит 30 двойных связей, слабо сопряженных между собой. Все они сосредоточены исключительно в шестичленных циклах.
Возможность существования сферической формы углерода была теоретически доказана еще в 1970-х гг. А обнаружены молекулы C60 были в 1985 г. английским ученым Г. Крото с коллегами в плазме, образовав-шейся при лазерном испарении графита. В их экспериментах лазерный луч направляли на графитовую мишень в форме диска, находящуюся в печи при температуре 1200 °С. Образующиеся пары углерода уносились потоком гелия и осаждались на стенках камеры. Анализ продуктов осаждения, проведенный с помощью масс-спектрометрии, показал, что в них содержатся вещества с молекулярной массой 720 и 840. Это и были первые фуллерены – C60 и C70.
Электродуговой метод в различных модификациях и поныне остается основным способом лабораторного и промышленного получения фуллеренов, причем достичь их выхода выше 12 % в промышленных масштабах не удается. Коммерческая цена чистого (99,5 %) фуллерена C60 составляет около 500 рублей, а неочищенного, в смеси с C70, – 300 рублей за один грамм.
В природе фуллерены пока не найдены. В начале 1990-х гг. появи-лись сообщения о том, что они содержатся в минерале шунгите (назван в честь поселка Шуньга в Карелии). Этот минерал добывается только в Карелии и представляет собой природный аморфный углерод. Его используют для создания облицовочных материалов, которым реклама приписывает особые биоэнергетические свойства – «положительную энергетику» и «оздоровляющее действие». Отчасти эти свойства связыва-ли с фуллеренами, однако более тщательные исследования не подтвердили наличия фуллеренов в шунгите.
Твёрдый фуллерен имеет молекулярную кристаллическую решетку, в узлах которой находятся молекулы C60. Они неполярны, поэтому вандер-ваальсовы связи между ними обусловлены дисперсионным взаимодейст-вием (притяжение наведенных дипольных моментов). Элементарная ячейка имеет форму куба: молекулы расположены в вершинах куба и в серединах его граней – такую ячейку называют кубической гранецентри-рованной (ГЦК). Между молекулами в решетке имеются довольно объем-ные пустоты, в которые могут встраиваться атомы щелочных металлов, образуя с фуллереном соединения состава M3C60, где M = K, Rb, Cs. Эти соединения называют фуллеридами. В отличие от самого фуллерена, фуллериды имеют ионную кристаллическую решетку.
При нагревании в инертной атмосфере фуллерен возгоняется, не плавясь, а при охлаждении до 260 К происходит изменение кристалличес-кой структуры: образуется твердая фаза с примитивной кубической решеткой. Плотность фуллерена составляет 1,7 г/см3, что значительно меньше, чем у алмаза и графита. Это неудивительно – ведь в фуллерене много пустот как внутри молекул C60, так и между ними. Будучи непо-лярным, фуллерен очень плохо растворим в воде и гораздо лучше (нес-колько граммов на литр) – в неполярных органических растворителях. Это единственная аллотропная форма углерода, которая хоть в чем-то растворима!
Чистый фуллерен не проводит электрического тока. Это связано с тем, что между молекулами в кристаллической решетке невозможен пе-ренос электронов. Однако при облучении светом электрическое сопротив-ление кристаллов уменьшается – это означает, что фуллерен обладает фо-топроводимостью. Увеличить проводимость можно и другим способом – добавляя к фуллерену атомы щелочных металлов. Так, фуллериды состава M3C60 при низких температурах становятся сверхпроводниками. Самая высокая температура перехода в сверхпроводящее состояние (38 К) зафиксирована для фуллерида цезия, Cs3C60. Механизм сверхпроводимос-ти в такого рода соединениях пока не выяснен.
Строго говоря, фуллерен в макроскопических количествах, в виде порошка не является наноматериалом, хотя его частицы и состоят из молекул почти нанометрового размера. У такого вещества наноуровень не проявляется – для этого надо создать нанокластеры из молекул фуллерена или перевести его в коллоидный раствор, где частицы дисперсной фазы будут иметь размер десятков и сотен нанометров.
Рассмотрим химические свойства фуллерена. Имея в составе молекулы 30 двойных связей, фуллерен С60 обладает довольно высокой реакционной способностью. С момента открытия фуллерена уже получены десятки тысяч соединений на его основе, поэтому можно считать, что фуллерен стал одним из основных строительных блоков органической химии. Его роль в современной химии сравнивают с ролью бензола как родоначальника огромного класса ароматических соединений.
Все производные фуллерена подразделяют на два класса: «эндо» (внутри) и «экзо» (снаружи). Эндоэдральными называют соединения включения, в которых атомы или небольшие молекулы заключены внутри фуллереновой сферы (обозначаются M@C60). Поместить частицы внутрь уже сформированной фуллереновой сферы путем разрыва связей С–С и сшивания пока не удалось, поэтому эндоэдральные производные готовят «в момент образования» фуллеренов. Если в состав электродов, используемых в электродуговом синтезе фуллерена, входят примеси металлов, то небольшая часть из них может попасть внутрь формирующейся в газовой фазе фуллереновой сферы. Первым было обнаружено эндоэдральное соединение лантана, LaC60. Металл в нем не может выйти из углеродной клетки, но сохраняет присущие ему маг-нитные свойства и влияет на электронное состояние и реакционную способность углеродного каркаса. Эндоэдральные соединения находят применение в медицине, например соединение с забавным названием «гадофуллерен» GdC82 используется как метка в магнитно-резонансной томографии.
«Экзо»-соединения образуются в результате реакций присоединения к двойным связям фуллерена. В принципе молекула C60 может присое-динить до 60 одновалентных атомов или групп атомов, однако полного присоединения практически не наблюдается, т.к. при этом очень сильно искажается углеродный скелет и продукт присоединения становится неустойчивым. Из простых веществ фуллерен в различных условиях присоединяет водород и галогены. Наиболее насыщенные водородом и фтором соединения имеют состав C60H36 и C60F48 соответственно.
Реакции присоединения сложных веществ позволяют, во-первых, вводить различные функциональные группы в фуллереновое ядро и тем самым менять его химическую природу, например, получать хорошо растворимые в воде биологически активные производные фуллерена. Во-вторых, с помощью подобных реакций фуллерен можно включать в сложные супрамолекулярные комплексы различной архитектуры.
Фуллерен легко вступает в реакции нуклеофильного, радикального и циклоприсоединения. Последние особенно важны для синтеза практи-чески важных производных фуллерена. Так, в реакциях диенового синтеза ([2+4]-циклоприсоединение) фуллерен выступает в роли диенофила и присоединяет диены с образованием шестичленных циклов:
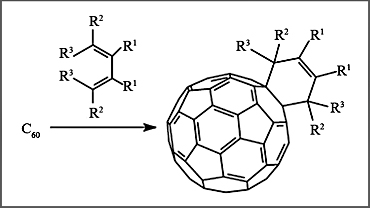
Реакции [2+1]-циклоприсоединения приводят к образованию трехчленных циклов на фуллереновом каркасе. В реакции Бингеля между фуллереном и 2-броммалоновым эфиром из двойной связи фуллерена образуется циклопропановое кольцо:
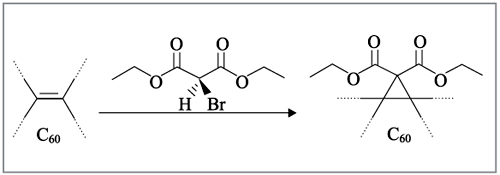
Эта реакция служит основой для построения на основе фуллерено-вого фрагмента разнообразных органических наноструктур.
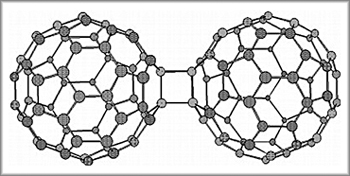
Реакции присоединения молекул фуллерена друг к другу относятся к типу [2+2]-циклоприсоединения и протекают при УФ-облучении фуллерена или под действием высокого давления. В зависимости от условий могут образовываться димер (рис. 8), тример, линейный полимер или двумерная сеть связанных между собой фуллереновых сфер.
|
| Рис. 8. Димер фуллерена C120 |
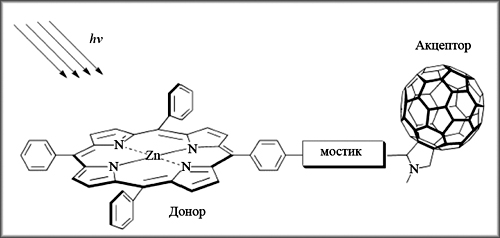
Очень важны для приложений электронные свойства фуллерена. Будучи электронодефицитным соединением, фуллерен служит хорошим акцептором электронов. Он способен принимать от одного до шести электронов. В качестве доноров могут выступать активные металлы, комплексные соединения переходных металлов или органические молекулы. Многие органические молекулы проявляют донорные свойства, находясь в возбужденном электронном состоянии, в которое они переходят, поглотив свет. Объединив в одном комплексе такие молекулы с акцепторами электронов типа фуллерена, получают устройства для преобразования световой энергии в электрическую (рис. 9,см. с. 22). В октябре 2008 г. появилось сообщение о том, что американская фирма «Konarka» начала производство солнечных батарей, в которых донором электронов служит органический полимер, а акцептором – наноструктуры на основе фуллеренов.
|
| Рис. 9. Перенос электрона от органического донора к фуллерену под действием света |
Области применения фуллерена очень разнообразны. Уникальное сочетание электронных свойств, симметричной объемной структуры и высокой реакционной способности делает фуллерен идеальным компонентом для создания супрамолекулярных наноматериалов и электронных устройств. На его основе созданы электрохимические сенсоры для обнаружения ионов, твердые ион-селективные электроды, монослои, генерирующие ток при облучении, катализаторы для реакций окисления органических веществ. Супрамолекулярные нанокомплексы фуллеренов и порфиринов, в которых происходит обратимый перенос электрона от порфиринов к фуллерену, – основа будущих устройств для искусственного фотосинтеза.
Производные фуллерена легко проникают через биологические мембраны, поэтому используются в качестве меток и индикаторов в медико-биологических исследованиях. Фуллерен легко присоединяет свободные радикалы и может выполнять в организме роль антиоксиданта. Эндоэдральные соединения, в которых внутри фуллерена заключен радионуклид, можно использовать при создании противораковых препаратов. Для этого фуллерен модифицируют такими функциональ-ными группами, которые обеспечивают его накопление в клетках опухоли, после чего радиоактивное излучение от находящегося внутри нуклида будет уничтожать эти клетки.
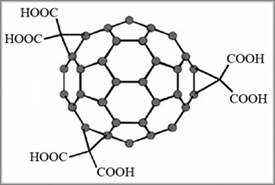
Главный барьер на пути использования фуллерена в медицине – его плохая растворимость – снимается путем химической модификации поверхности сферы и присоединения к ней гидрофильных групп. Так, шестиосновная кислота, полученная из фуллерена, обладает раство-римостью до 70 г/л (рис. 11). Другой способ повышения растворимости фуллерена в воде – использование поверхностно-активных веществ.
|
| Рис. 11. Водорастворимое производное фуллерена |
Интересное применение нашел фуллерен в водородной энергетике. Российские ученые создали новый композитный материал на основе фуллеренсодержащей сажи и гидрида магния, который способен обратимо поглощать рекордные количества водорода и может служить хранилищем этого газа в энергетических установках. В порошок сажи, обработанный глицерином, ученые добавили порошок гидрида магния и приготовили сорбент, который способен поглощать до 65 г/л водорода.
В следующей лекции будем говорить о нанотрубках.
Дата добавления: 2016-10-26; просмотров: 5969;











