Выведение (экскреция)
Большинство лекарственных веществ выводится из организма через почки в неизмененном виде или в виде продуктов биотрансформации. В почечные канальцы вещества могут поступать при фильтрации плазмы крови в почечных клубочках. Многие вещества секретируются в просвет проксимальных канальцев. Транспортные системы, которые обеспечивают эту секрецию, малоспецифичны, поэтому разные вещества могут конкурировать за связывание с транспортными системами. При этом одно вещество может задерживать секрецию другого вещества и таким образом задерживать его выведение из организма. Например, хинидин замедляет секрецию дигоксина, концентрация дигоксина в плазме крови повышается, возможно проявление токсического действия дигоксина (аритмии и др.).
Липофильные неполярные вещества в канальцах подвергаются обратному всасыванию (реабсорбции) путем пассивной диффузии. Гидрофильные полярные соединения мало реабсорбируются и выводятся почками.
Выведение (экскреция) слабых электролитов прямо пропорционально степени их ионизации (ионизированные соединения мало реабсорбируются). Поэтому для ускоренного выведения кислых соединений (например, производных барбитуровой кислоты, салицилатов) реакцию мочи следует изменять в щелочную сторону, а для выведения оснований — в кислую.
Кроме того, лекарственные вещества могут выделяться через желудочно-кишечный тракт (выделение с желчью), с секретами потовых, слюнных, бронхиальных и других желез. Летучие лекарственные вещества выделяются из организма через легкие с выдыхаемым воздухом.
У женщин в период кормления грудью лекарственные вещества могут выделяться молочными железами и с молоком попадать в организм ребенка. Поэтому кормящим матерям не следует назначать лекарства, которые могут неблагоприятно воздействовать на ребенка.
Биотрансформация и экскреция лекарственных веществ объединяются термином «элиминация». Для характеристики элиминации используют константу элиминации — ке1 (ке) и период полуэлиминации - t1/2.
Константа элиминации показывает, какая часть вещества элиминируется в единицу времени. Например, внутривенно введено вещество А в дозе 10 мг; ке1 = 0,1/ч. Через 1 ч в плазме крови останется 9 мг, через 2 ч - 8,1 мг.
Период полуэлиминации — t1/2 — время, за которое концентрация вещества в плазме крови снижается наполовину. В основное время элиминации t1/2 не зависит от дозы вещества и одинаков в разное

Общий (total) клиренс определяется по формуле Clt = Vd * ke[.
Другими словами, Clt показывает, какая часть объема распределения освобождается от вещества в единицу времени.
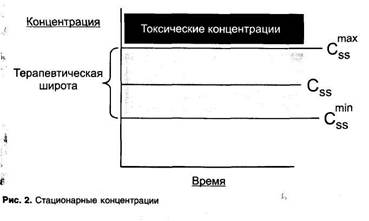
Для оптимального терапевтического эффекта и для предупреждения токсического действия необходимо поддерживать в плазме крови постоянную (стационарную) терапевтическую концентрацию лекарственного вещества. Стационарную концентрацию обозначают как Css (steady-state concentration). В справочниках и руководствах по фармакологии приводят значения средних терапевтических концентраций для наиболее употребительных лекарственных веществ.
Определяют также минимальную терапевтическую концентрацию (минимальную эффективную концентрацию) — Cssmin и максимальную терапевтическую концентрацию (максимальную безопасную концентрацию) - Cssmax, выше которой концентрации становятся токсическими. Интервал между Cssmin и Cssmax соответствует терапевтической широте (рис. 2). Чем больше терапевтическая широта лекарственного средства, тем легче его использовать в практической медицине. Наоборот, при малой терапевтической широте увеличивается вероятность попадания в зону токсических концентраций.
Для поддержания средней терапевтической концентрации лекарственного вещества можно вводить раствор этого вещества внутривенно капельно. При этом концентрация вещества в плазме крови сначала повышается быстро, затем медленнее и, наконец, устанавливается стационарная концентрация, при которой скорость введения вещества равна скорости его элиминации (биотрансформация + экскреция). Скорость введения определяют по формуле

Однако значительно чаще лекарственные вещества назначают внутрь или в виде отдельных инъекций. В этих случаях целесообразно сначала вводить нагрузочную дозу для быстрого достижения терапевтической концентрации, а затем назначать малые дозы, которые поддерживают терапевтическую концентрацию, — поддерживающие дозы.
Б. Фармакодинамика
Фармакодинамика - фармакологические эффекты, механизмы действия, локализация действия, виды действия лекарственных веществ.
Фармакологические эффекты лекарственного вещества — изменения в деятельности органов, систем организма, которые вызывает данное вещество (например, усиление сокращений сердца, снижение артериального давления, стимуляция умственной деятельности, устранение страха и напряженности и т.п.). Как правило, каждое вещество вызывает ряд характерных для него фармакологических эффектов. В каждом конкретном случае используют лишь определенные эффекты лекарственного средства, которые определяют как основные эффекты. Остальные (не используемые, нежелательные) фармакологические эффекты называют побочными эффектами.
Механизмы действия лекарственных веществ — способы, которыми вещества вызывают фармакологические эффекты. К основным вариантам механизмов действия относятся действие на: 1) специфические рецепторы, 2) ферменты, 3) ионные каналы, 4) транспортные системы.
Большинство лекарственных веществ действует на специфические рецепторы. Эти рецепторы представлены чаще всего функционально активными белковыми молекулами; взаимодействие с ними дает начало биохимическим реакциям, которые ведут к возникновению фармакологических эффектов.
Различают специфические рецепторы, связанные с клеточными мембранами (мембранные рецепторы), и внутриклеточные рецепторы.
Мембранные рецепторы делят на: 1) рецепторы, сопряженные с ионными каналами, 2) рецепторы, сопряженные с ферментами, 3) рецепторы, взаимодействующие с G-белками.
К рецепторам, сопряженным с ионными каналами, относятся, в частности, N-холинорецепторы и ГАМКА -рецепторы.
При стимуляции N-холинорецепторов (никотиночувствительные холинорецепторы) открываются сопряженные с ними натриевые каналы. Вход ионов Na+ в клетку обусловливает деполяризацию клеточной мембраны и возбудительный эффект.
ГАМКА -рецепторы непосредственно сопряжены с хлорными каналами. Стимуляция ГАМКА-рецепторов ведет к открытию Сl--каналов, входу ионов Сl-, гиперполяризации клеточной мембраны и тормозному эффекту.
К рецепторам, которые сопряжены с ферментами, относятся, в частности, рецепторы инсулина, сопряженные с тирозинкиназой.
Рецепторы, взаимодействующие с G-белками, — М-холинорецепторы (мускариночувствительные холинорецепторы), адренорецепторы, дофаминовые рецепторы, опиоидные рецепторы и др.
G-белки, т.е. ГТФ-связывающие белки, локализованы в клеточной мембране и состоят из α-β-γ-,субъединиц. При взаимодействии лекарственного вещества с рецептором α -субъединица G-белка соединяется с ГТФ (GTP) и воздействует на ферменты или ионные . каналы. Один рецептор взаимодействует с несколькими G-белками, а каждый комплекс а-субъединицы G-белка с ГТФ действует ;на несколько молекул фермента или на несколько ионных каналов. Таким образом осуществляется механизм амплифайера (усилителя): при активации одного рецептора изменяется активность многих молекул фермента или многих ионных каналов.
Одними из первых были обнаружены G-белки, связанные с β 1-адренорецепторами сердца. При активации симпатической иннервации сердца возбуждаются β 1-адренорецепторы; через посредство G-белков активируется аденилатциклаза; из АТФ образуется цАМФ, активируется протеинкиназа, при действии которой фосфорилиру-ются и открываются кальциевые каналы.
Увеличение входа ионов Са2+ в клетки синоатриального узла ускоряет 4-ю фазу потенциала действия — сокращения сердца учащаются. Открытие Са2+-каналов в волокнах рабочего миокарда ведет к увеличению концентрации Са2+ в цитоплазме (вход Са2+ способствует высвобождению Са2+ из саркоплазматического ретикулума). Ионы Са2+ связываются с тропонином С (составная часть тропонин-тро-помиозина); таким образом уменьшается тормозное влияние тропонин-тропомиозина на взаимодействие актина и миозина - сокращения сердца усиливаются (рис. 3).
При активации парасимпатической иннервации сердца (блуждающие нервы) возбуждаются М2-холинорецепторы и через посредство G-белков аденилатциклаза угнетается — сокращения сердца урежаются и ослабляются (в основном ослабляются сокращения предсердий, так как парасимпатическая иннервация желудочков относительно бедна).
Таким образом, G-белки могут оказывать на аденилатциклазу как стимулирующее, так и угнетающее влияние. Стимулирующие G-белки обозначили как Gs -белки (stimulate), а угнетающие — Gi-белки (inhibit) (рис. 4).
При возбуждении М1-холинорецепторов, М3-холинорецепторов, α1-адренорецепторов через Gq белки активируется фосфолипаза С, которая способствует тому, что из фосфатидилинозитол-4,5-дифос-фата образуются инозитол-1,4,5-трифосфат и диацилглицерол. Ино-зитол-1,4,5-трифосфат стимулирует высвобождение ионов Са2+ из саркоплазматического ретикулума (рис. 5, 6).
К внутриклеточным рецепторам относятся рецепторы кортико-стероидов и половых гормонов. В частности, рецепторы глюкокор-тикоидов локализованы в цитоплазме клеток. После соединения глюкокортикоида с цитоплазматическими рецепторами комплекс глюкокортикоид-рецептор проникает в ядро и оказывает влияние на экспрессию различных генов.
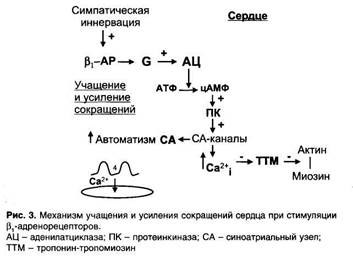

Рис. 5. Влияние фосфолипазы С на уровень цитоппазматического Са2+.
• • •
Способность веществ связываться с рецепторами (тенденция веществ к связыванию с рецепторами) обозначают термином «аффинитет». По отношению к одним и тем же рецепторам аффинитет разных веществ может быть различным. Для характеристики аффинитета используют показатель pKD - отрицательный логарифм константы диссоциации, т.е. концентрации вещества, при которой занято 50% рецепторов.
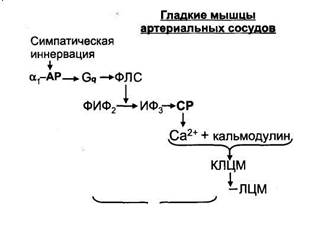
Рис. 6. Механизм сокращения гладких мышц артериальных сосудов при стимуляции
симпатической иннервации.
ФПС - фосфолипаза С; ФИФ2 - фосфатидилинозитол -4,5- дифосфат; ИФ3 - инозитоп -
1,4,5- трифосфат; СР - саркоплазматический ретикулум; КЛЦМ - киназа легких цепей
миозина.
Внутренняя активность - способность веществ стимулировать рецепторы; определяется по величине фармакологического эффекта, связанного с активацией рецептора. В обычных условиях нет прямой корреляции между аффинитетом и внутренней активностью: вещество может занимать все рецепторы и вызывать слабый эффект, и, наоборот, вещество может занимать 1% рецепторов и вызывать максимальный для данной системы эффект.
Агонисты — вещества, обладающие аффинитетом и внутренней активностью.
Полные агонисты обладают аффинитетом и максимальной внутренней активностью. Частичные (парциальные) агонисты обладают аффинитетом и менее, чем максимальной внутренней активностью.
Антагонисты обладают аффинитетом, не обладают внутренней активностью и препятствуют действию полных или частичных агонистов (вытесняют агонисты из связи с рецепторами). Если действие антагониста устраняется при повышении дозы агониста, такой антагонизм называют конкурентным.
Частичные агонисты могут быть антагонистами полных агонистов. В отсутствие полного агониста частичный агонист стимулирует рецепторы и вызывает слабый эффект. При взаимодействии с полным агонистом частичный агонист занимает рецепторы и препятствует действию полного агониста. Например, окспренолол — частичный агонист β -адренорецепторов в отсутствие влияний симпатической иннервации на сердце вызывает слабую тахикардию. Но при повышении тонуса симпатической иннервации окспренолол действует, как настоящий β -адреноблокатор, и вызывает брадикардию. Это объясняется тем, что частичный агонист окспренолол устраняет действие медиатора норадреналина, который по отношению к β 1 -адренорецепторам сердца является полным агонистом.
Агонисты-антагонисты — вещества, которые по-разному действуют на подтипы одних и тех же рецепторов: одни подтипы рецепторов они стимулируют, а другие - блокируют. Например, наркотический анальгетик налбуфин по-разному действует на подтипы опиоидных рецепторов. Каппа-рецепторы налбуфин стимулирует (и поэтому снижает болевую чувствительность), а мю-рецепторы блокирует (и поэтому менее опасен в плане лекарственной зависимости).
Примером влияния веществ на ферменты может быть действие антихолинэстеразных средств которые блокируют ацетилхолинэстеразу (фермент, расщепляющий ацетилхолин) и таким образом усиливают и удлиняют действие ацетилхолина.
Известны лекарственные вещества, которые стимулируют или блокируют ионные каналы клеточных мембран, т.е. каналы, которые избирательно проводят ионы Na+, K+, Са2+ (натриевые, калиевые, кальциевые каналы) и др. Например, местноанестезирующие и некоторые противоаритмические вещества (прокаин, хинидин) блокируют натриевые каналы. В медицинской практике применяют блокаторы кальциевых каналов, активаторы калиевых каналов.
Примером влияния веществ на транспортные системы может быть действие трициклических антидепрессантов, которые блокируют обратный транспорт норадреналина и серотонина через пре-синаптическую мембрану.
Возможны и другие механизмы действия. Например, диуретик маннитол увеличивает диурез за счет повышения осмотического давления в почечных канальцах.
Механизмы действия разных лекарственных веществ изучены в разной степени. В процессе их изучения представления о механизмах действия могут не только усложняться, но и существенно меняться.
Понятие «локализация действия» означает преимущественное место (места) действия тех или иных лекарственных веществ. Например, сердечные гликозиды действуют в основном на сердце.
К понятию «виды действия» относятся местное и общее (резор-бтивное) действие, рефлекторное действие, основное и побочное действие, прямое и косвенное действие.
Примером местного действия может быть действие местноанес-тезирующих средств (с. 38).
Большинство лекарств оказывают общее (резорбтивное) действие, которое обычно развивается после всасывания (резорбции) вещества в кровь и его распространения в организме.
Как при местном, так и при резорбтивном действии вещества могут возбуждать различные чувствительные рецепторы и вызывать рефлекторные реакции.
Основное действие лекарственного вещества — его эффекты, которые используются в каждом конкретном случае. Все остальные эффекты при этом оценивают как проявления побочного действия.
Лекарственные вещества могут оказывать на те или иные органы прямое действие. Кроме того, действие лекарственных веществ может быть косвенным. Например, сердечные гликозиды оказывают на сердце прямое действие, но, улучшая работу сердца, эти вещества повышают кровоснабжение и функции других органов (косвенное действие).
Дата добавления: 2016-09-26; просмотров: 2099;











