Понятия о фазах. Твердые растворы
В промышленности в качестве конструкционных материалов применяются в основном сплавы. Получают их сплавлением двух и более металлов (например, латунь – это сплав меди с цинком) или металла с неметаллом (сталь – это сплав железа с углеродом). Химические элементы из таблицы Менделеева, образующие сплав, называются компонентами.
Фаза – это однородная часть системы (сплава), которая имеет свою кристаллическую решетку, а, следовательно, и свои свойства, и от остальной части системы отделена поверхностью раздела.
Например, при кристаллизации чистого металла в равновесии находятся две фазы: твердый и жидкий металл.
Большинство компонентов в жидком состоянии полностью растворяются друг в друге, образуя одну фазу – жидкость. В твердом состоянии образуются следующие фазы: твердые растворы и химические соединения.
Твердый раствор – это фаза, в которой один компонент сохраняет свою кристаллическую решетку (растворитель), а второй не сохраняет (легирующий элемент). Твердые растворы всегда имеют решетку растворителя.
Существуют следующие виды твердых растворов: замещения, упорядоченные, внедрения.
Твердые растворы замещения (рис. 3.1). По этому механизму образуются легированные стали, где растворителем является железо (Fe). При этом следует иметь в виду, что атомные объемы у Fe и легирующего элемента (хрома, молибдена, никеля, вольфрама и др.) не одинаковы, то есть при замещении атомов железа легирующим элементом кристаллическая решетка железа деформируется, искажается. Поэтому легированные стали по сравнению с углеродистыми более твердые и прочные, но у них запас пластичности и вязкости ниже. Замещение происходит произвольно, статистически, то есть никакого упорядочения нет.
Эти растворы бывают ограниченные и неограниченные.
– растворитель; – легирующий элемент
Рис. 3.1. Схема строения твёрдых растворов замещения
Условия образования неограниченных твердых растворов:
1) однотипность кристаллических решеток;
2) различие в атомных объемах должно быть небольшим (не более 8…15%);
3) элементы должны быть в одной или смежных группах таблицы Менделеева.
При несоблюдении этих требований получим ограниченныетвердые растворы.
Упорядоченные твердые растворы. Замещение идет упорядоченно. На рис. 3.2: компонент 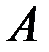 (Au), золото является растворителем; компонент
(Au), золото является растворителем; компонент 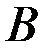 (Cu), медь – легирующий элемент, который замещает атомы Au в его кристаллической решетке упорядоченно, то есть только по граням куба, при этом образуется как бы химическое соединение Cu3Au.
(Cu), медь – легирующий элемент, который замещает атомы Au в его кристаллической решетке упорядоченно, то есть только по граням куба, при этом образуется как бы химическое соединение Cu3Au.
При упорядочении резко растет твердость, появляется хрупкость, падает ударная вязкость за счет образования ковалентной связи между атомами.
| Au |
| Cu |
Рис. 3.2. Схема строения упорядоченных
твердых растворов замещения
Твердые растворы внедрения. Эти растворы образуются между переходными металлами (Fe, Ni, Co, Mn …) и металлоидами (C, N, O, S, P …) с очень маленьким атомным объемом, чтобы они смогли поместиться в порах между атомами растворителя (рис. 3.3). Эти растворы всегда ограниченные (поры заполнены – больше не растворяются). По свойствам эти растворы так же, как и растворитель, мягкие и пластичные.
| растворитель |
| металлоид |
Рис. 3.3. Схема строения твердых растворов внедрения
Кроме твердых растворов существуют химические соединения. Они образуются между элементами, далеко находящимися друг от друга в таблице Менделеева, а, следовательно, атомы имеют большое различие в строении и свойствах. В отличие от твердых растворов химические соединения приобретают новую кристаллическую решетку, а, следовательно, новые физико-механические свойства: высокую твердость, хрупкость и не поддаются обработке резанием.
Виды химических соединений:
а) валентные. Например, Al2O3; Fe2O3; Cu2O. Формула этих соединений определяется правилом валентности;
б) фазы внедрения. Они так же, как и растворы внедрения, образуются между металлами и металлоидами путем внедрения по порам между атомами. Но в отличив от растворов внедрения приобретают новую кристаллическую решетку, а следовательно, и свойства (высокую твердость и хрупкость) и образуются при большом содержании металлоида;
Например, WC – карбид вольфрама, фаза внедрения, paстворяется в вольфраме по механизму внедрения: всего 0,001% С. Другие примеры: Fe3C – карбид железа; Fe2N – нитрид железа;
в) электронные соединения. Формула этих соединений определяется электронной концентрацией, то есть отношением суммы валентных электронов к общему числу атомов в соединении. Электронные соединения бывают с электронной концентрацией 3/2; 21/13; 7/4.
Итак, фазами являются:
1) жидкость (расплав);
2) чистый твердый металл;
3) твердые растворы;
4) химические соединения.
Дата добавления: 2016-05-31; просмотров: 2703;











