Примеры решения задач на определение затрат количества теплоты
Задача 1. Закрытый баллон емкостью V=10л с углекислым газом под давлением p=8МПа и температурой 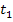 =7°C нагрели до
=7°C нагрели до  =17°С. Какое количество теплоты было затрачено на нагревание углекислого газа?
=17°С. Какое количество теплоты было затрачено на нагревание углекислого газа?
Дано: 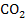 V=10л Р=8МПа V=10л Р=8МПа 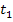 =7°C =7°C  =17°С =17°С |
СИ V=10 . 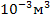 P=8 . P=8 . 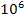 Па Па   |
Решение Первое начало термодинамики  +A, где +A, где 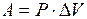 A=0, т.к. баллон был закрыт. A=0, т.к. баллон был закрыт.  , ,  Значит Значит  . Затраченное количество теплоты идет на увеличение внутренней энергии газа. ∆U= . Затраченное количество теплоты идет на увеличение внутренней энергии газа. ∆U= 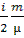 R∆T, где i=6 – число степеней свободы трехатомной молекулы углекислого газа СО2. Из уравнения Клапейрона-Менделеева R∆T, где i=6 – число степеней свободы трехатомной молекулы углекислого газа СО2. Из уравнения Клапейрона-Менделеева  выражаем выражаем 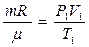 . . |
| Q - ? |
Теперь 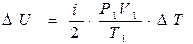 .
.
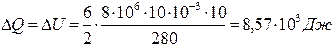
Ответ: На нагревание углекислого газа затрачено 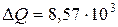 Дж теплоты.
Дж теплоты.
Задача 2. 2,5г хлороформа разлили при температуре кипения (61°С). Найти количество теплоты, затраченное на испарение хлороформа и изменение энтропии при испарении. Удельная теплота парообразования хлороформа r=2,57. 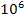 Дж/кг
Дж/кг
Дано: r=2,57. 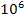 Дж/кг m=2,5г t=61°C Дж/кг m=2,5г t=61°C |
СИ m=2,5. 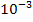 кг T=t+273=334 К кг T=t+273=334 К |
Решение В процессе испарения температура хлороформа не изменяется Т= const. Количество теплоты, необходимоедля испарения массы m жидкости ∆Q = rm; ∆Q =2,57. 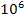 2,5. 2,5. 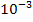 =6,43. =6,43.  Дж Изменение энтропии Дж Изменение энтропии  ; ; 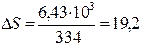 Дж/К Дж/К |
| ∆Q- ? ∆S - ? |
Ответ: На испарение хлороформа затрачено ∆Q=6,43.  Дж теплоты, изменение энтропии при испарении ∆S=19,2 Дж/К.
Дж теплоты, изменение энтропии при испарении ∆S=19,2 Дж/К.
Задачи
4.1. В автоклаве объемом V=8л находилось m=0,1кг воды, которая при температуре t=200°С превратилась в пар. Найти давление пара внутри автоклава.
4.2. Определить значения молярных теплоемкостей при V=const и при P=const, т.е. 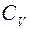 и
и  , а также отношение
, а также отношение 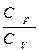 для углекислого газа СО2.
для углекислого газа СО2.
4.3.Насколько изменится внутренняя энергия водяного пара при нагревании его от 20°С до 100°С, если масса пара m=2г?
4.4. Какое количество  теплоты нужно сообщить m=15г кислорода, чтобы нагреть его на ∆t=100° при постоянном объеме.
теплоты нужно сообщить m=15г кислорода, чтобы нагреть его на ∆t=100° при постоянном объеме.
4.5. Один киломоль азота нагревают при постоянном давлении от 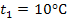 до
до 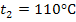 . Найти: 1) изменение внутренней энергии ∆U, 2) работу расширения A, 3) количество теплоты, сообщенного азоту
. Найти: 1) изменение внутренней энергии ∆U, 2) работу расширения A, 3) количество теплоты, сообщенного азоту  .
.
4.6. Азот массой m=28г нагревают от 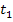 =20°C до
=20°C до  =120°C при постоянном давлении. Найти работу расширения азота.
=120°C при постоянном давлении. Найти работу расширения азота.
4.7. Для лечения мастита на вымя коровы накладывают парафин при 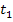 =70°С. Удельная теплоемкость парафина с=3,23 .
=70°С. Удельная теплоемкость парафина с=3,23 .  Дж/кг . К. Температура вымени
Дж/кг . К. Температура вымени  =38°С. Вычислить массу парафина, если надо передать ∆Q=185.
=38°С. Вычислить массу парафина, если надо передать ∆Q=185.  Дж тепла.
Дж тепла.
4.8. Какое количество теплоты  затратит человек на парообразование, если за сутки он выделяет m=0.5кг пота? Масса человека M=70кг. Удельная теплопродукция его q=1.6 Дж/кг.с. Удельная теплота парообразования r=2,45.
затратит человек на парообразование, если за сутки он выделяет m=0.5кг пота? Масса человека M=70кг. Удельная теплопродукция его q=1.6 Дж/кг.с. Удельная теплота парообразования r=2,45. 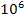 Дж/кг. Найти количество теплоты
Дж/кг. Найти количество теплоты  , выделяемое человеком за сутки.
, выделяемое человеком за сутки.
4.9. Удельная теплопродукция взрослого человека q=1,6 Дж/кг.с. Сколько теплотыв годвыделит человек при средней мышечной нагрузке? Масса человека m=75кг?
4.10. Какое количество эфира, находящегося при температуре кипения, должно испариться, чтобы энтропия увеличилась на ∆S=200 Дж/К? Температура кипения эфира t=34,8°С? Удельная теплота парообразования эфира  Дж/кг.
Дж/кг.
4.11. Определить увеличение энтропии, обусловленное выделением тепла лошадью за 1 час, если удельная теплопродукция лошади q=0,547 Дж/кг.с, масса лошади m=450кг, температура ее тела t=37°С.
4.12. Вычислить увеличение энтропии в результате потоотделения человека, если за 1 час человек в среднем выделяет m=20г пота. Температура тела t=37°С, удельная теплота парообразования  Дж/кг.
Дж/кг.
4.13. Одноатомный идеальный газ совершил при адиабатном расширении работу А=20кДж. Как при этом изменилась его внутренняя энергия ∆U?
Ответы 4. Основы термодинамики
4.1.27,3.105 Па.4.2.24,93 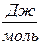 ; 33,24
; 33,24 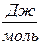 ; 1,33.4.3.222 Дж.
; 1,33.4.3.222 Дж.
4.4. 974 Дж.4.5.831Дж.4.6.2,1.106 Дж; 0,83.106 Дж; 2,93.106 Дж.
4.7.1,8 кг. 4.8.1,23 .106 Дж; 9,7 .106 Дж. 4.9.3,78.109 Дж.4.10.0,173 кг.
4.11.2,86.103  .4.12.158
.4.12.158  .4.13. -20 кДж.
.4.13. -20 кДж.
Дата добавления: 2020-11-18; просмотров: 1253;











