Лактатдегидрогеназа
Лактатдегидрогеназа (ЛДГ, L-лактат: NAD-оксидоредуктаза; К.Ф. 1.1.1.27) – цитоплазматический , Zn-содержащий гликолитический фермент, обратимо катализирующий восстановление пировиноградной кислоты в молочную кислоту:
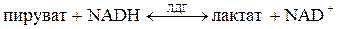
Фермент широко распространён в организме человека. По степени убыли активности ЛДГ органы и ткани можно расположить в следующей последовательности: почки, сердце, скелетные мышцы, поджелудочная железа, селезёнка, печень, лёгкие, сыворотка крови. ЛДГ содержится в значительном количестве в эритроцитах, поэтому исследуемая сыворотка не должна содержать следов гемолиза. ЛДГ имеет пять изоферментов, представляющих различные комбинации из четырёх субъединиц двух основных типов – Н (от англ. heart – сердце) и М (от англ. muscle – мышца):
ЛДГ1 – 4Н;
ЛДГ2 – 3Н1М;
ЛДГ3 – 2Н2М;
ЛДГ4 – 1Н3М;
ЛДГ5 – 4М.
Изоферменты ЛДГ нумеруются в соответствии с электрофоретической подвижностью по направлению к аноду (рис. 5.2.2). На рисунке показано распределение и относительное количество изоферментов ЛДГ в различных органах. Экстракты нанесены на линию, отмеченную надписью «Старт». При заданных условиях опыта (рН) 4 изофермента ЛДГ движутся к аноду, а один (ЛДГ5) к катоду.
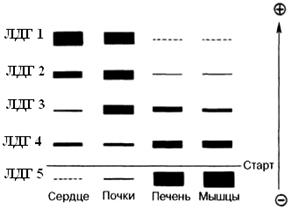
Рис. 5.2.2 Распределение и относительное количество изоферментов ЛДГ в различных органах
Протекание прямой реакции превращения пирувата в лактат обеспечивает М субъединица ЛДГ, протекание обратной реакции – Н субъединица (рис. 5.2.3).
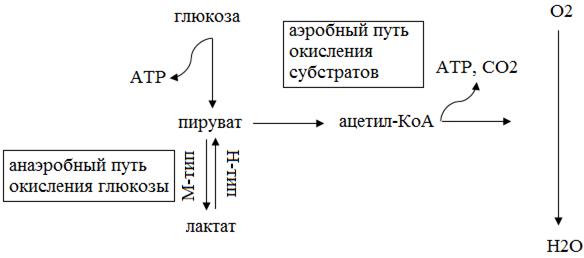
Рис. 5.2.3. Обратимая реакция превращения пирувата в лактат, катализируемая ЛДГ
Изоферментный спектр и тип обмена веществ в ткани коррелируют между собой. Так, в тканях с преимущественно аэробным обменом веществ (мозг, сердце, почки и др.) наибольшей активностью обладают ЛДГ1 и ЛДГ2, в тканях с выраженным анаэробным обменом веществ (печень, скелетная мускулатура и др.) преобладают ЛДГ4 и ЛДГ5. Наиболее высокое содержание ЛДГ3 отмечают в лимфоидной ткани, тромбоцитах и опухолях. Это распределение имеет большой биологический смысл. Изофермент ЛДГ1 in vitro активен при низкой концентрации пирувата и ингибируется его избытком, в то время как ЛДГ5 сохраняет активность при сравнительно высоких концентрациях пирувата. Поскольку восстановление пирувата в лактат, катализируемое ЛДГ1, сильно ингибируется уже небольшими концентрациями пирувата, то в ткани, богатой этим изоферментом, например в сердце, пируват подвергается преимущественно аэробному окислению. Кроме активной переработки собственного (эндогенного) лактата, сердечная мышца способна поглащать лактат из крови, затем превращать его в пировиноградную кислоту и подвергать дальнейшему окислению для пополнения запасов АТР. С другой стороны, в тканях, где преобладают изоферменты ЛДГ4 и ЛДГ5 (печень, скелетная мускулатура), АТР в значительной степени образуется за счёт гликолиза. Высокая активность ЛДГ5 в них обеспечивает быстрое превращение пирувата в лактат, который затем выбрасывается в кровь, поскольку в скелетной мускулатуре дальнейшее превращение лактата почти не осуществляется. Однако в некоторых тканях нет зависимости между типом обмена и изоферментным спектром. Так в эритроцитах, тромбоцитах, хрусталике глаза, где преобладает анаэробный обмен, фермент представлен в основном изоферментами ЛДГ1 ЛДГ2.
Молекулярная масса каждой изоформы ЛДГ составляет 135 кДа (по другим данным 140 кДа), а каждой субъединицы – 34 кДа (по другим данным – 33,5 кДа). Вместо лактата ЛДГ может окислять α-гидроксибутират до α-оксибутирата. Особенно высокую активность в отношении α-гидроксибутирата по сравнению с лактатом проявляет ЛДГ1. Вследствие этого ЛДГ1 обычно измеряют с использованием именно этого субстрата, а данный изофермент (ЛДГ1) имеет второе название – α-гидроксибутиратдегидрогеназа (α-ГБДГ).
Соотношение между изозимами ЛДГ, по данным разных авторов при электрофорезе на ацетатцеллюлозных плёнках составляет у взрослых:
| ЛДГ1 | 19-29% |
| ЛДГ2 | 23-27% |
| ЛДГ3 | 17-25% |
| ЛДГ4 | 8-17% |
| ЛДГ5 | 8-18% |
Это соотношение может изменяться как при адаптации к меняющимся условиям среды, так и в ходе онтогенеза. Эмбрионы всех млекопитающих проходят стадию развития, когда митохондрии ещё не готовы к окислению субстратов. В этих условиях особенно велика роль анаэробного гликолиза. Как показано для развивающихся мышей, на стадии эмбриона основной формой фермента является тетрамер типа М4. После рождения постепенно нарабатываются другие формы ЛДГ, и к периоду, соответствующему взрослому организму, устанавливается соотношение разных изоформ, типичное для каждой ткани.
Клиническое значение определения ЛДГ
Рост общей активности ЛДГ сыворотки крови не несёт достаточно специфической информации. Можно отметить, что общая активность ЛДГ резко повышена при миелобластных и пернициозных анемиях, обширных опухолевых процессах, вирусных гепатитах, шоке и гипоксии. Выраженное повышение наблюдается при циррозах печени, обтупационных желтухах, заболеваниях почек, опорно-мышечного аппарата, опухолях, при сердечной недостаточности. Активность фермента повышается при любых патологических процессах, связанных с цитолизом клеток органов и тканей (например, при инфарктах миокарда, лейкозах, гемолитических анемиях, гепатитах и др.). Определение отдельных изоферментов ЛДГ в сыворотке крови имеет большую диагностическую значимость, чем определение суммарной активности.
Активность ЛДГ1 и ЛДГ2 увеличивается при инфаркте миокарда, различных видах анемий, острых поражениях (некрозах) почечной ткани. Уровень ЛДГ1 повышается при опухолевых заболеваниях яичников. Повышение активности ЛДГ5 выявляется при повреждении скелетных мышц, любых воспалительных или дегенеративных заболеваниях скелетных мышц, многих заболеваниях печени (циррозе, всех типах гепатитов) и при раковых опухолях. Повышение активности изоферментов средней зоны, то есть ЛДГ2 и ЛДГ3 ЛДГ4 встречается при массивном разрушении тромбоцитов (эмболия лёгочной артерии, массивная гемотрансфузия) и вовлечении в патологический процесс лимфатической системы, например, при таких заболеваниях, как инфекционный мононуклеоз, лимфомы, лимфоцитарный лейкоз.
У здоровых новорожденных, в первые дни жизни содержание ЛДГ2 ниже, а содержание ЛДГ5 выше чем у взрослого человека. Максимальная активность фермента наблюдается на 2-4 день жизни. К 6-7 годам соотношение фракций ЛДГ примерно соответствуют таковому у взрослого человека.
Рекомендации по определению ЛДГ:
1. Сыворотка не должна быть гемолизирована, так как ЛДГ содержится в эритроцитах и результаты могут быть завышены;
2. Не рекомендуется использовать в качестве антикоагулянта оксалаты, так как соли щавелевой кислоты являются ингибиторами лактатдегидрогеназной реакции;
3. Рекомендуется использовать свежую сыворотку или плазму крови, лучше плазму, так как ЛДГ много в тромбоцитах и при их разрушении активность ЛДГ повышается.
ЛЕКЦИЯ 5.3
Дата добавления: 2020-10-01; просмотров: 709;











