Физические основы замораживания воды путем интенсивного испарения и свойства твердой углекислоты
В предыдущих разделах было отмечено, что количество теплоты, необходимое для испарения жидкости, настолько значительно, что горячая вода, кипящая без нагревания при пониженном давлении, поглощает собственную тепловую энергию и быстро охлаждается. Если продолжить этот опыт и обеспечить достаточно низкое давление, можно добиться замерзания кипящей воды. Для создания такого давления требуется высокоэффективный воздушный насос и непрерывное поглощение образующегося водяного пара с использованием концентрированной серной кислоты, что технически сложно реализовать в домашних условиях. Однако существует более практичный метод — использование жидкостей, испаряющихся легче воды, таких как сернистый углерод или диэтиловый эфир.
Сернистый углерод (CS₂) обладает высокой летучестью, однако его применение в жилых помещениях ограничено из-резкого неприятного запаха, который значительно интенсивнее ароматов, характерных для моторных экипажей. По этой причине для демонстрационных опытов предпочтительнее использовать диэтиловый эфир, несмотря на его специфический запах. Оптимальное время для проведения эксперимента — послеобеденные часы, когда члены семьи заняты делами вне дома. Методика выполнения опыта проиллюстрирована на рисунке 43 и заключается в создании условий для интенсивного испарения эфира, что приводит к локальному понижению температуры и замерзанию воды.
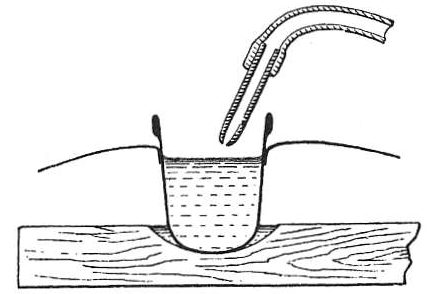
Рис. 43. Схема экспериментальной установки для замораживания воды с использованием испаряющегося эфира: деревянная основа с углублением, наперсток с эфиром, погруженный в воду, и устройство для подачи воздуха
В деревянной пластине необходимо выполнить небольшое углубление, куда наливают несколько капель воды, после чего в воду помещают наперсток, заполненный эфиром. Для проведения серии экспериментов достаточно небольшого количества эфира. Для интенсификации испарения используют резиновые меха от пульверизатора, соединяя их через резиновую трубку со стеклянным наконечником, имеющим узкое отверстие. При отсутствии мехов можно использовать силу легких, однако важно обеспечить направленную подачу воздуха, не допуская разбрызгивания эфира. Во избежание попадания эфира в воду рекомендуется расширить край наперстка, вставив его в тонкую пластину с круглым отверстием.
Диэтиловый эфир характеризуется высокой воспламеняемостью, поэтому в зоне проведения эксперимента категорически запрещается использование открытого огня или нагревательных приборов. Поток воздуха, направленный на поверхность эфира, ускоряет процесс испарения по тому же принципу, который используется при сушке белья в ветреную погоду: движущийся воздух удаляет насыщенный пар с поверхности жидкости, замещая его сухим воздухом, что увеличивает градиент концентрации и скорость парообразования. Поглощение теплоты при испарении эфира столь интенсивно, что до полного испарения жидкости температура в наперстке снижается настолько, что происходит замерзание воды, и наперсток примерзает к деревянной пластине. Хотя данный процесс не является кипением в строгом смысле слова, он представляет собой ускоренное парообразование, приводящее к аналогичным термическим эффектам.
Для замораживания воды путем кипения при пониженном давлении требуется сложное оборудование, однако существует другое вещество, легко переходящее в твердое состояние при частичном испарении — жидкая углекислота (диоксид углерода). В газообразной форме CO₂ хорошо известен по процессу выделения пузырьков при открывании бутылок с газированными напитками, пивом или игристым вином. Под давлением около 60 атмосфер диоксид углерода переходит в жидкое состояние при обычной температуре и хранится в стальных баллонах. При открывании вентиля такого баллона происходит резкое снижение давления, вследствие чего жидкая углекислота интенсивно переходит в газообразное состояние, образуя струю газа.
При горизонтальном расположении баллона (выходным отверстием вниз) жидкая фаза скапливается у выходного отверстия, и при открытии вентиля сжатый газ выталкивает жидкость наружу. Визуально струя жидкости не наблюдается — виден лишь белый туман, оседающий на поверхности в виде белого налета твердого вещества. Этот налет представляет собой твердую углекислоту, образующуюся в результате интенсивного охлаждения при испарении. Для сбора твердой фазы на горловину баллона закрепляют мешок из плотной фланели, в который направляют струю углекислоты. Мешок быстро заполняется снегообразной массой твердого CO₂.
Механизм этого явления основан на том, что при нормальной температуре жидкая углекислота существует только под высоким давлением. При снижении давления до атмосферного происходит быстрое испарение, причем необходимая для фазового перехода теплота отбирается от самой жидкости. В результате часть углекислоты, теряя теплоту, замерзает, образуя мелкие кристаллические частицы, которые агломерируются в мешке, тогда как газообразная фракция фильтруется через ткань. Температура твердой углекислоты составляет приблизительно -60 °C, поэтому обращение с ней требует осторожности во избежание криогенных ожогов, сходных по последствиям с термическими.
Твердая углекислота позволяет демонстрировать замерзание ртути, температура плавления которой составляет -39 °C. Для этого в массе снегообразной углекислоты формируют углубление, куда заливают ртуть из разбитого термометра. Через несколько минут ртуть полностью затвердевает, образуя ковкий металлический комок. Однако при комнатной температуре замерзшая ртуть быстро оттаивает, и при наклоне поверхности она растекается в виде шарообразных капель, которые трудно собрать. Важно помнить о высокой токсичности паров ртути, поэтому эксперименты следует проводить оперативно, не оставляя металл открытым. Для измерения температур ниже -39 °C применяют спиртовые термометры, поскольку ртутные термометры непригодны при таких условиях.
Наблюдая за снегообразной углекислотой, оставленной при атмосферном давлении, можно заметить уменьшение ее массы без образования жидкости. Это явление называется сублимацией — прямым переходом вещества из твердого состояния в газообразное, минуя жидкую фазу. Аналогичный процесс происходит со льдом в морозную погоду, когда масса ледяного тела на весах постепенно уменьшается вследствие испарения. Если на поверхности твердой углекислоты или соприкасающихся с ней предметах появляется жидкость, это не расплавленная углекислота, а вода, сконденсировавшаяся из атмосферного водяного пара при контакте с сильно охлажденными поверхностями.
Сведения об авторах и источниках:
Авторы: В. Гампсон, К. Шеффер
Источник: Парадоксы природы
Данные публикации будут полезны студентам физических и технических специальностей, изучающих механику и принципы работы простых механизмов, начинающим инженерам и конструкторам, интересующимся эргономикой и оптимизацией транспортных средств, а также всем, кто увлекается историей техники и неочевидными физическими явлениями в повседневной жизни.
Дата добавления: 2026-02-16; просмотров: 86;











