СТРОЕНИЕ ВЕЩЕСТВА. ВИДЫ СВЯЗИ
Все вещества состоят из атомов.
Атом представляет собой систему, состоящую из положительно заряженного ядра, вокруг которого вращаются отрицательно заряженные электроны. Электроны притягиваются к ядру и отталкиваются друг от друга. Расположенные ближе к ядру электроны подвержены большему притяжению, они ослабляют притяжение внешних электронов, которые находятся на большем расстоянии от ядра. Внешние электроны могут отрываться от одного атома и присоединяться к другому атому, изменяя число его внешних электронов. Такие электроны называются валентными. У разных веществ атомы содержат разное число валентных электронов.

| а | б |
Рис. 1.1. Ковалентная (атомная) связь в молекуле водорода:
а - изолированные атомы; б - молекула с ковалентной связью
Атом, потерявший один или несколько электронов, становится положительно заряженным. Атом, который присоединил к себе свободные электроны, становится отрицательно заряженным. Образовавшиеся таким образом положительные и отрицательные частицы называются ионами.
Из атомов строятся молекулы. Связи, благодаря которым происходит объединение атомов в молекулы, называются химическими.
Способность атомов вступать в соединения с атомами других веществ и образовывать молекулы определяет химические свойства вещества.
Молекула является наименьшей частицей вещества, которая сохраняет его химические свойства.
Химические связи между атомами вещества делят на ковалентные (атомные), ионные, металлические и молекулярные.
1) Ковалентная
Ковалентные связи возникают между атомами за счет образования устойчивых пар валентных электронов разных атомов (рис. 1.1).
Эти пары являются общими для атомов, которые входят в молекулу. Если двухатомная молекула состоит из атомов одного элемента (Н2, Сl2, N2), то электронная пара в одинаковой степени принадлежит обоим атомам. В таком случае молекулу и ковалентную связь называют неполярными и (или) нейтральными. В неполярных молекулах центры положительных и отрицательных зарядов совпадают.
Если двухатомная молекула состоит из атомов различных элементов, то электронная пара может быть смещена к одному из атомов. В этом случае ковалентную связь называют полярной, а молекулы с полярной связью, у которых центры положительных зарядов не совпадают, - полярными или дипольными. Дипольная молекула характеризуется электрическим дипольным моментом

где g - абсолютное значение заряда, Кл; l – расстояние между центрами положительного и отрицательного зарядов, м.
Если у многоатомных молекул заряды расположены симметрично, то они неполярны, при несимметричном расположении атомов молекулы полярны (рис. 1.2).
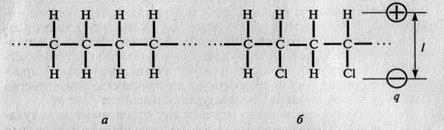
Рис. 1.2. Схемы неполярной молекулы полиэтилена (  ) (а) и полярной молекулы поливинилхлорида (б): q - абсолютное значение заряда; l - расстояние между центрами положительного и отрицательного зарядов
) (а) и полярной молекулы поливинилхлорида (б): q - абсолютное значение заряда; l - расстояние между центрами положительного и отрицательного зарядов
Атомная связь имеет направленный характер. Эта связь образуется в направлении наибольшей плотности объединенных электронов. Поэтому вещества с ковалентными связями обычно характеризуются твердостью, хрупкостью, тугоплавкостью и химической инертностью. К ним относятся кристаллы германия, кремния, алмаза, соединения элементов из средних групп таблицы Д.И.Менделеева - SiC, BN. Атомные связи характерны для таких газов, как Н2, О2, N2. Молекулы некоторых органических соединений: полиэтилена (С2Н4)n, политетрафторэтилена (C2F4)n -имеют ковалентную связь, при этом между отдельными молекулами в этих материалах образуются молекулярные связи.
Разновидностью ковалентной связи является донорно-акцепторная связь, которая возникает между атомом, способным отдать электрон (донор), и атомом, способным принять этот электрон (акцептор). Примером таких материалов являются соединения мышьяка -арсениды галлия GaAs и индия InAs.
2) Ионная
Ионные связи обусловлены силами электростатического притяжения между положительными и отрицательными ионами.
Молекулы вещества с полярной связью полярны. Не имеют направленности. Соединения с ионной связью обладают разными свойствами, которые характерны для типичных металлов и неметаллов. Такие связи наиболее характерны для неорганических диэлектриков, которые имеют в своем составе ионы противоположных знаков (большинство солей и некоторые оксиды, например, ZnO, CdO, NiO, CuO2).
Ионные связи менее прочны, чем ковалентные, поэтому соединения, образованные ионной связью, уступают веществам с ковалентной связью по механической прочности и химической стойкости.
3) Металлическая
Металлические связи образуются в металлах и обусловлены особенностями поведения внешних (валентных) электронов. Атомы металлов обладают способностью отдавать внешние (валентные) электроны, превращаясь в положительный ион, или присоединять их вновь, превращаясь снова в нейтральный атом.
Внешние электроны, которые покидают атомы, становясь свободными, называются коллективизированными.
В результате металл представляет собой систему, состоящую из положительных ионов, которые находятся в среде коллективизированных электронов.

Рис.1.3. Металл в представлении теории электронного газа
В этой системе одновременно имеют место притяжение между ионами и свободными электронами и ковалентная связь между нейтральными молекулами. Наличие этих связей определяет монолитность и прочность металлов.
Благодаря наличию свободных электронов металлы обладают высокой электро- и теплопроводностью. Металлическая связь в отличие от ковалентной не имеет направленного характера, что придает металлам высокую пластичность. Большинство металлов имеют высокие температуры плавления и кипения.
4) Молекулярная
Молекулярные связи образуются между отдельными молекулами в результате электростатического притяжения между зарядами противоположных знаков, которые имеются в молекулах. Такое электростатическое притяжение называют силами Ван-дер-Ваалъса. С помощью таких сил образуются молекулы в твердом водороде Н2, азоте N2, углекислом газе СО2 и других органических соединениях - полиэтилене, фторопласте и др.
Особым видом молекулярной связи является водородная связь, которая образуется через ион водорода (протон), расположенный между двумя ионами соседних молекул. Водородной связью соединяются молекулы воды и некоторых органических соединений.
В твердых веществах атомы и молекулы располагаются в строгом порядке и хаотично. Вещества с закономерным упорядоченным расположением атомов или молекул в пространстве называют кристаллическими, а вещества с беспорядочным расположением атомов или молекул - аморфными.
КРИСТАЛЛИЧЕСКИЕ ВЕЩЕСТВА
К кристаллическим веществам относятся все металлы и металлические сплавы.
Кристалл состоит из множества сопряженных друг с другом элементарных кристаллических ячеек. В элементарной кристаллической ячейке содержится наименьшее число атомов.
Простейшим типом элементарной кристаллической ячейки является простая кубическая решетка. Размеры кристаллической решетки характеризуются ее параметрами. Под параметром решетки понимают расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку. Эти расстояния очень малы и их измеряют в нанометрах или ангстремах (1А = 10-10 м). Параметр кубической решетки (рис. 1.5) обозначается буквой а и находится в пределах 0,28...0,6 нм. Параметр решетки хрома равен 2,9 А , алюминия - 4,04 А. Следовательно, в кристаллическом веществе на 1 мм размещаются десятки миллионов атомов.
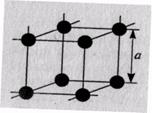
Рис. 1.4.Элементарная ячейка кубической решетки
Для описания структуры кристаллических тел пользуются понятием пространственной кристаллической решетки, которая представляет собой пространственную сетку, в узлах которой располагаются частицы, образующие твердое тело.
В узлах ковалентных (атомных) решеток находятся нейтральные атомы, которые связаны друг с другом ковалентной связью.
В узлах ионных решеток расположены чередуясь положительные и отрицательные ионы, которые связаны друг с другом ионной связью.
В узлах металлических решеток расположены положительные ионы, в промежутках между которыми находятся свободные электроны. Они образуют решетку с помощью металлических связей.
В узлах молекулярных решеток находятся молекулы. Такие решетки образуются за счет ковалентной и ионной связей.
Каждое вещество обычно образует кристаллы определенной формы. Порядок взаимного расположения атомов в кристалле может быть различным.
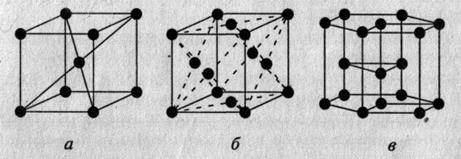
Рис. 1.5. Основные типы кристаллических решеток металлов:
а - кубическая объемно центрированная; б - кубическая гранецентрированная; в – гексагональная
Стремление атомов металлов к сближению и уплотнению приводит к образованию более сложных типов решеток. Наиболее распространенными типами кристаллических решеток являются:
кубическая объемно центрированная (см. рис. 1.5, а), ее имеют 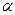 -железо, хром, вольфрам, ванадий;
-железо, хром, вольфрам, ванадий;
кубическая гранецентрированная (см. рис. 1.5, б), ее имеют 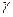 -железо, медь, алюминий;
-железо, медь, алюминий;
гексагональная (см. рис. 1.5, в), ее имеют бериллий, кадмий, магний и другие металлы.
Наиболее плотно и компактно размещены атомы гексагональной и кубической гранецентрированной решеток.
Упорядоченное расположение атомов в кристаллах приводит к различному расположению и плотности атомов в разных направлениях. Этим обусловлено различие свойств металлов в разных направлениях.
Изменение свойств кристаллов (металлов) в зависимости от направления называют анизотропией.
Степень анизотропности свойств металлов может быть значительной. Например, предел прочности на растяжение у меди изменяется от 120 до 360 МПа, а относительное удлинение при растяжении ( 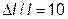 ) - до 55%.
) - до 55%.
Однако промышленные сплавы обычно состоят из большого числа кристаллов, кристаллические решетки которых по-разному ориентированы в пространстве, поэтому свойства сплавов не зависят от направления.
Все кристаллические вещества при нагревании сохраняют твердое состояние до определенной температуры. Атомы, находящиеся в узлах кристаллической решетки, совершают непрерывные колебательные движения. Чем выше температура вещества, тем больше амплитуда этих колебаний. При достижении определенной температуры амплитуда колебаний атомов настолько увеличивается, что происходит разрушение кристаллической решетки. Атомы переходят в хаотическое состояние, а вещество превращается из твердого в жидкое. Температура, при которой происходит фазовое превращение твердого вещества в жидкое, называется температурой плавления Тпл.
Обратный переход кристаллических веществ из жидкого состояния в твердое называется кристаллизацией. Температура, при которой происходит фазовое превращение жидких веществ в кристаллические, называется температурой кристаллизации Тк.
Дефекты кристалических решеток
Строение металлов, когда атомы образуют геометрически правильную кристаллическую структуру, может быть только в идеальном случае. В реальных условиях кристаллы имеют большое число дефектов, наличие которых оказывает существенное влияние на свойства металлов и сплавов.
Основными дефектами кристаллических решеток являются точечные, линейные, поверхностные и объемные (трехмерные) несовершенства.
1) Точечные
Точечные несовершенства появляются в результате образования вакансий (атомных дырок) или внедрения атомов в междуузлие (рис. 1.6).
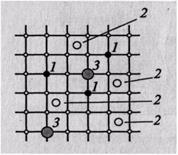
Рис1.6. Точечные несовершенства:
1 – вакансия; 2 – дислоцированный атом; 3 – примесный атом
Атомы металлов находятся в колебательном движении относительно положения равновесия. При нагревании амплитуда колебаний атомов возрастает. Большинство атомов в данной кристаллической решетке обладает одинаковой средней энергией, поэтому амплитуда их колебаний при данной температуре одинакова, но отдельные атомы имеют энергию, значительно превышающую среднюю, и амплитуда колебаний их также больше среднего значения. Такие атомы могут перемещаться из одного места в другое и выходить из узла в междуузлие. Атомы, вышедшие из узла решетки, называются дислоцированными, а места, где находились атомы, остаются в решетке незаполненными и называются вакансиями.
Причинами точечных несовершенств являются условия кристаллизации, наличие примесей в металлах и сплавах, неравномерное распределение энергии между атомами кристаллической решетки.
Точечные дефекты влияют на диффузионные процессы. Например, при изготовлении полупроводниковых интегральных схем нагревание до температуры плавления приводит к увеличению вакансий на 2%.
2) Линейные
Линейные несовершенства представляют собой изменения структуры, протяженность которых в одном измерении гораздо больше, чем в двух других. Такие несовершенства называют дислокациями. Появление дислокаций вызвано воздействиями на металл напряжений разного происхождения. При воздействии сосредоточенной нагрузки на некоторый участок происходит перераспределение напряжений в образце. Этот процесс сопровождается медленным сдвигом атомов. Граница между сдвинутыми участками и сохранившейся без изменения областью является дислокацией (рис. 1.7).
Дислокации бывают краевыми, винтовыми и смешанными.
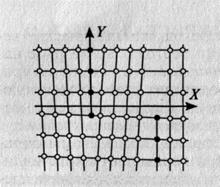
Рис. 1.7. Линейные дислокации
3) Поверхностные
Поверхностные несовершенства характеризуются значительными изменениями в двух измерениях. Примером поверхностного несовершенства является граница между кристаллами в реальных сплавах.
Кристалл состоит из блоков, которые по-разному ориентируются в пределах этого кристалла, образуя мозаичную структуру. На границах повернутых друг относительно друга блоков возникают напряжения, приводящие к искажению кристаллической решетки (рис. 1.8).

Рис. 1.8. Поверхностные несовершенста (мозаичная структура кристалла)
4) Объемные
Объемные несовершенства кристалла имеют существенные размеры во всех трех измерениях. К объемным дефектам относятся пустоты, включения отдельных кристаллических зерен или кристаллической модификации.
По структуре кристаллические материалы бывают монокристаллическими и поликристаллическими.
Монокристаллические материалы - это однородные анизотропные тела, у которых атомы расположены по всему объему в правильном порядке. При этом сами атомы состоят из периодически повторяющихся одинаковых кристаллических ячеек.
Поликристаллические материалы состоят из большого числа сросшихся между собой мелких кристаллических зерен (кристаллитов), которые хаотически ориентированы в разных направлениях. За счет усреднения свойств отдельных кристаллов свойства тела в целом не зависят от направления, и поликристаллические материалы обычно изотропны. Однако с помощью специальной обработки (холодная прокатка с последующим отжигом, намагничивание, поляризация и т.д.) материал становится анизотропным. Материалы с искусственно созданной анизотропией называют текстурами.
К поликристаллическим материалам относятся металлы и многие керамические материалы.
АМОРФНЫЕ ВЕЩЕСТВА
В аморфных веществах атомы и молекулы расположены беспорядочно. В отличие от кристаллических аморфные вещества не имеют строго определенной температуры перехода из твердого состояния в жидкое. Этот переход осуществляется в некотором диапазоне температур. При понижении температуры у аморфных материалов, находящихся в жидком состоянии, происходит быстрое повышение вязкости, которое затрудняет перемещение молекул, необходимое для формирования и роста кристаллов.
Свойства аморфных тел не зависят от выбранного направления, так как аморфные тела изотропны. Например, при охлаждении расплавленного кристалла кварца образуется так называемый плавленный кварц, свойства которого одинаковы по всем направлениям и при этом не отличаются от свойств кристаллического кварца.
Аморфные вещества делятся на две группы:
простые аморфные, к которым относятся низкомолекулярные жидкости, неорганические стекла, плавленный кварц и др.;
высокополимерные соединения, к которым относятся каучуки, резины, органические стекла, смолы.
АМОРФНО-КРИСТАЛЛИЧЕСКИЕ ВЕЩЕСТВА
Некоторые вещества могут находиться в кристаллическом и аморфном состояниях. Аморфное состояние вещества менее устойчиво, чем кристаллическое, поэтому возможен самопроизвольный переход вещества из аморфного состояния в кристаллическое. Примером такого превращения служит расстекловывание, в процессе которого происходит самопроизвольная кристаллизация стекла при повышенных температурах или давлении. В связи с образованием мелких кристалов стекло меняет свои оптические свойства и превращается в аморфно-кристаллический материал, называемый ситаллом.
Аморфно-кристаллическое состояние свойственно оксиду кремния, который встречается в природе в виде кристаллов кварца, а также в аморфном состоянии в виде минерала опал. В определенном интервале температур в термодинамически устойчивом состоянии, которое характерно для аморфно-кристаллических веществ, находятся жидкие кристаллы.
Дата добавления: 2020-07-18; просмотров: 511;











