Типы и классы биогеохимических провинций
(по А.И. Перельману)
| Типы провинций | Классы провинций | Типоморфные элементы и ионы | Примеры элементов, с которыми связаны биогеохимические эндемии (в скобках - предполагаемые) | |
| Дефицит- ные | Избыто- чные | |||
| S - с сильнокис- лыми водами | Si - с cернокис- лыми водами | Н+, SO42- | N, Р, К, Са | Н+-ион, S, Al, Mn, Fe, Co, Ni, Си, Zn, Cd, Mo, Pb, Hg, U, As |
| S2 - с соляно- кислыми водами | Н+, Сl- | H-H+ ион, Cl; Na, Al, Mn, Fe, B, F… | ||
| W - с кислыми и кислыми глеевыми водами | Wi - с водами, не обогащенными растворенным органическим веществом (РОВ) | Н+, H+-Fe2+ | В, N, F, Mg, Н, К, Са, Со, Сu, Zn, Se, Mo... | H-H+ ион, Al |
| W2 - с водами, богатыми РОВ | Н+, H+-Fe2+, Сорг. | О, N, P, К, Са, Mg, Сu, Se, Mo… | H-H+ ион, Al, Mn. Fe… | |
| V - с нейтральными и слабощелоч-ными водами | V1 - с пресными водами | Са (Са2+) | N,P,K… | |
| V2 - с солонова- тыми и солены- ми водами | Na(Na+), Cl (С12-), S (SO42-) | N,P,K... | Na Mg, S, Cl, Sr, Mo, В (U) | |
| F - с сильноще- лочными (содовыми) водами | F1 | Na (Na+), OH- | N, Mg, P, Ca, K... | (Na, Al, Сu, Zn, TR, Y, Sc...) |
Границы видов биогеохимических провинций могут не совпадать с ландшафно-геохимическими границами и поэтому в основу выделения видов не всегда могут быть положены ландшафно-геохимическое районирование и картографирование. Систематика же техногенных биогеохимических провинций является отдельной специальной проблемой.
Биогеохимические провинции типа S и, в частности, класса S1, формируются на участках присутствия сульфидов, с образованием серной кислоты, при рН до 2-3, а то и до 0, что резко увеличивает подвижность ряда металлов. Выделяются цинковые, медные и другие виды биогеохимических провинций. Возможно, что для эпох фанерозоя были типичны подобные условия. Они могли быть и центрами видообразования организмов.
Для других провинций характерны биогеохимические эндемии - болезни флоры, фауны, людей, связанные преимущественно с избытком элементов.
Класс S2 характерен для вулканических областей с кислыми HCl дождями, солянокислыми реками, при низких рН. В водах высоки содержа-
ния Al, Fe, повышены F, Cl, но содержания халькофильных минералов могут быть и не высоки.
Биогеохимические провинции типа W приурочены к гумидному климату. Характерно кислое выщелачивание. Содержание Ca может понижаться до 0,00n%. Здесь резкий дефицит многих биологически важных элементов. Имеет место минеральное голодание фауны, низкое содержание в организме кальция, развитие "биогеохимических эндемий дефицитности". Отмечены малые размеры животных, пониженная яйценосность птиц, тонкая скорлупа яиц. Из флоры не характерны "кальциефилы", распространены кислые злаки. К "алюминиевым" растениям относятся плауны, чай. Здесь могли возникать важные центры видообразования.
Класс W1 формируется при расчлененном рельефе, с преобладанием ландшафтов кислого (Н+) класса; для класса W2 характерны болотистые низменности, в частности Западно-Сибирская. В ультрапресных водах РОВ нередко представляет преобладающую часть сухого остатка. Это сочитается с дефицитом Са и других важных биоэлементов. Характерен избыток Fe, H+ и РОВ.
Биогеохимические провинции типа V отвечают лесостепям, степям и пустыням. Для класса V1 свойственны гидрокарбонатно-кальциевые воды, преобладание незасоленных почв. В аридном климате идет слабая миграция кальция. Возможен и избыток элементов с соответствующими эндемиями. Видообразование в этих условиях оптимально - дефицитных элементов мало.
Класс V2 развит в депрессиях рельефа бессточных областей. Организмы здесь существуют в условиях высокого содержания в водах Na, Mg, Cl, сульфат-иона. Это важные центры видообразования.
Биогеохимические провинции типа F отличаются развитием солонцов, с рН выше 8,5, иногда до 11. Известны содовые солонцы, солончаки, озера, болота, реки. Содержание Ca и Mg низко. Мало также Sr, Ba, Fe, Ni, Co, Pb. Отмечается дефицит многих элементов. Благоприятны условия для миграции и накопления Na, Li, B, Zn, Cu, Ag, Be, Si, Ge, Sn, Ti, W, Mo, Y, TR иттровой группы. В организмах повышены содержания TRY.
К близким выводам подошла и медицинская география. В частности было предложено комплексное эпидемиолого-географическое районирование мира. Выявлены основные закономерности эпидемиологии: пространственная неравномерность эпидемического процесса; рассеяние и концентрация в пространстве эпидемиологических явлений; цикличность в динамике эпидемиологического процесса; адекватность комплекса географических условий элементам эпидемического процесса; зональность и азональность предпосылок и проявлений эпидемического процесса.
Выделено 18 крупных эпидемиолого-географических регионов в мире, 20 районов в России (рис. 12.3) и 20 районов в России.
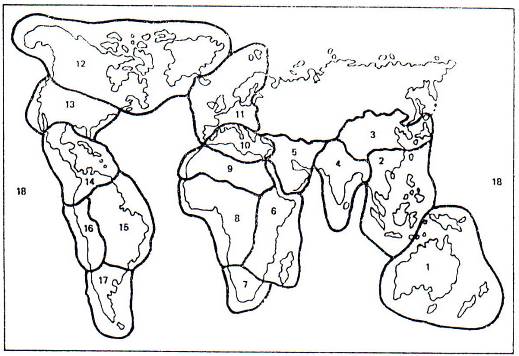
Рис. 12.3. Эпидемиолого-географическое районирование зарубежных территорий (по А.А. Келлеру, 1993).
Степень эпидемиологического напряжения: а - наиболее высокая, б - повышенная, в - умеренная, г - пониженная. Районы: 1 – Австралийский (б), 2 - Юго-Восточной Азии (а), 3 - Северо-Восточной Азии (б), 4 - Индийский (а), 5 - Юго-Западной Азии (б), 6 – Восточноафриканский (а), 7 – Южноафриканский (в), 8 – Западноафриканский (а), 9 – Центральноафриканский (а), 10 – Средиземноморский (в), 11 – Европейский (г), 12 - Канадско-Гренландский (г), 13 – Североамериканский (г0, 14 - Центральноамериканский (а), 15 – Восточно-Американский (а), 16 – Западноамериканский (б), 17 – Южноамериканский (г), 18 – Океанический (б)
Примером районирования конкретного вида заболеваний по территории России является карта эндемичного зоба в СССР (рис. 12.4).
Гл. 13. ХИМИЧЕСКАЯ ЭКОТОКСИКОЛОГИЯ
1. Биологическая активность химических элементов
Толчком к развитию науки экотоксикология явилось появление в 1962 г. книги Рэчел Карлсон "Молчаливая весна", ставшая алармистским актом. Три дисциплины - химия, экология и токсикология (учение о токсичности) - были объединены в единую научную дисциплину. Позднее сюда же привлекались знания биохимии, физиологии, популяционной генетики.
Экотоксикантами называются токсичные и устойчивые в условиях окружающей среды вещества, способные накапливаться в организмах до опасных уровней концентраций. Чужеродные вещества, не входящие в естественный биотический круговорот, называют ксенобиотиками. Экологи-
ческая магнификация - так называется процесс увеличения концентрации химиката в организмах при переходе от низших трофических уровней к высоким. Так, в планктоне содержание диметилртути составляет около 0,01 мкг/г, в мышечной ткани рыб 1,5, у птиц-рыболовов - 3-14 мкг/г.
Исследованием воздействия химических веществ на организм на различных уровнях (клетка, орган, организм, популяция и экосистема) занимается экотоксикология, так как при подобных исследованиях выявляются изменения состояния и возникают предположения о возможности прямого или косвенного вредного воздействия. Под вредным воздействием понимают явные изменения обычных колебаний численности популяции и долгосрочные или необратимые изменения состояния экосистемы.
К важнейшим задачам этой науки относятся выявление вредного воздействия (в качественном и количественном отношении), разработка лечебных мероприятий, выявление изменений видового состава, функциональные нарушения в экосистеме, проблемы сохранения и восстановления экосистем.
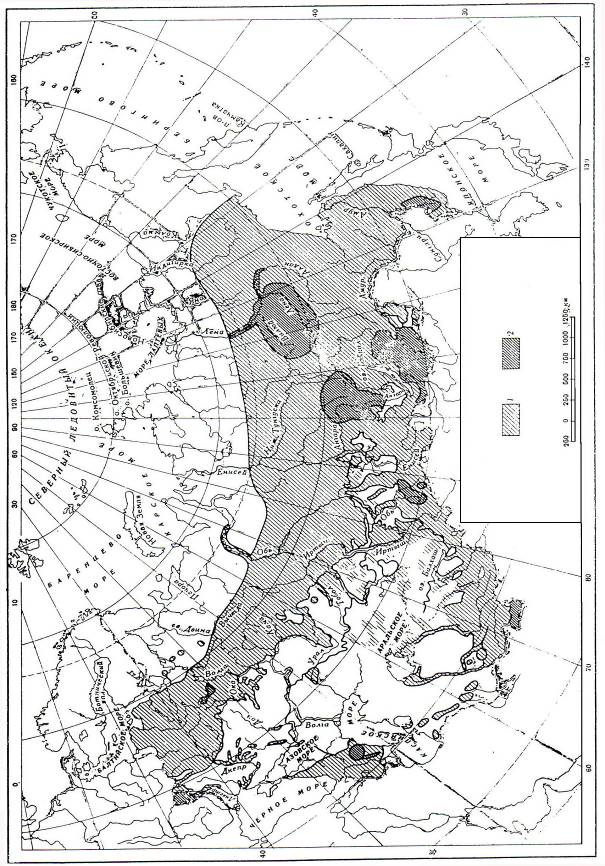
Рис.12.4. Карта эндемического зоба в СССР (по В.В. Ковальскому, 1982)
1 – эндемический зоб встречается; 2 – эндемичный зоб распростанен
В живом организме присутствуют многие химические элементы и каждый из них выполняет свою биологическую роль. Из организма человека 60% приходится на воду, 34% - это органические вещества, 6% - неорганические. Основные компоненты органики - C, H, O, а также N, P и S. Из неорганических веществ постоянно присутствует 22 химических элемента:
Ca, P, O, Na, Mg, S, B, Cl, R, V, Mn, Fe, Co, Ni, Cu, Zn, Mo, Cr, Si, J, F, Se. Условно принято считать, что если массовая доля элемента превышает в организме 10-2%, то он относится к макроэлементу, а если 10-3-10-5 % - это микроэлемент.
Большинство микроэлементов из перечисленных выше 22 - металлы, а из металлов больше половины - d-элементы. Многие биологические катализаторы-ферменты содержат ионы переходных металлов (d-элементов). Так, Mn входит в состав 12 различных ферментов, Fe - в 70, Cu - в 30, а Zn - более чем в 100.
Характерным признаком жизненно необходимых элементов является колоколообразный вид кривой ("удав, проглотивший слона") доза (n) - ответная реакция (R эффект) - рис. 13.1.
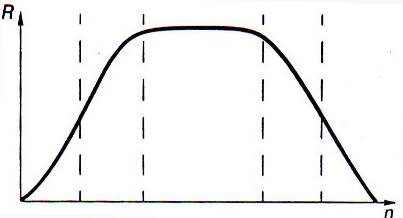
Рис. 13.1. Зависимость ответной реакции R от дозы (n) для жизненно необходимых элементов
Важнейшие биологические функции выполняют только Na, K, Mg, Fe и Ca, которые в целом дают почти 99% всех атомов - это макроэлементы.
При малом поступлении данного элемента организму наносится существенный ущерб и он находится на грани выживания. А избыток оказывает токсическое действие, вплоть до летального исхода.
Жизненно необходимы Na и K. Так, внутри клеток мышечных волокон, сердца, печени, почек содержатся повышенные количества ионов K, а вне клетки - Na. Этот градиент концентрации ионов К и Nа на границе клеток по мере старения организма падает. При наступлении смерти концентрации их выравниваются.
Гидротированные атомы Na, K, Mg и Ca участвуют в процессах осмоса и передачи нервных сигналов, а также обуславливают прочность костной ткани скелета.
Так, недостаток Fe приводит к анемии (малокровию), так как оно входит в состав гема - составной части гемоглобина крови (у взрослого примерно 2,6 г). Еще в XVII в. при малокровии принимали настой железных опилок в красном вине. Но и избыток Fe вреден: с ним связан сидероз глаз и легких. Главный регулятор Fe в крови - печень.
Недостаток Zn-содержащих компонентов (этот элемент входит в структуру активного центра важнейшего гормона инсулина, регулирующего уровень сахара в крови) составляет около 138 мкМ.
Недостаток Cu ведет к деструкции кровеносных сосудов, паталогическому росту костей, дефектам в соединительных тканях. Возможно, дефицит Cu служит одной из причин рака. Но и избыток Cu ведет к нарушению психики и параличу органов (болезнь Вильсона). В малых дозах Cu используют в медицине для задерживания роста и размножения бактерий (бактериостазное средство). Сульфат Cu(II) применяют для лечения конъюктивитов, прижигания при трахоме в виде глазных карандашей (сплав сульфата меди(II), нитрата K, квасцов и камфоры). При ожегах кожи фосфором проводят ее обильное смачивание 5%-ным раствором сульфата меди (II).
Cu-содержащие соединения в крови присутствуют при концентрациях около 15 мкМ, в сыворотке - 16-18 мкМ, в плазме - 18 мкМ. Cu входит в состав некоторых ферментов, например фенолазы и гемоцианина, способных, подобно гемоглобину, переносить кислород. Cu, как химический элемент, необходима при биосинтезе гемоглобина.
То же относится и к содержаниям микроэлементов, где и дефицит и излишек резко отражаются на состоянии здоровья. Многое здесь еще очень слабо изучено, но в качестве иллюстрации приведем характерные симптомы дефицита и избытка некоторых из макро- и микроэлементов в организме человека (табл. 13.1).
Таблица 13.1
Характерные симптомы дефицита и избытка некоторых химических элементов в живых и растительных организмах, г/т (по А.К. Бондареву, 1976, В.В. Ковалевскому, 1982, с добавлениями)
| Элемент | Отрицательная аномальная область нарушения регуляции | Фоновая область нормальной регуляции | Положительная аномальная область нарушенной регуляции | |||
| НПС+ | Болезнь из-за недостатка элемента | НПС-ПДК | ПДК | |||
| В | <6 | Отмирание почек роста, листьев, стеблей | 6-30 | >30 | Боровые энтериты у животных и растений | |
| Мn | <400 | Бесплодность, ухудшение роста скелета, заболевание костной системы, усиление зоба, рак кожи | 400-1500 | >1500 | Заболевание костной системы | |
| Со | <7 | Анемия, злокачественная анемия, эндемический зоб | 7-30 | >30 | Угнетение синтеза витамина В12 | |
| Сu | <15 | Анемия, вторичная анемия, заболевания костной системы, рак, слабость артерий, нарушение деятель-ности печени, невызревание злаков | 15-60 | >60 | Поражение почек, уродливость, желтуха | |
| Zn | <30 | Карликовый рост растений и животных, повреждения кожи, замедленное сексуальное созревание | 30-70 | >70 | Угнетение окислительных процессов, желтуха | |
| Sr | <3 | Рак, замедление клеточного роста | 3-600 | >600 | Рахит, уровская болезнь | |
| Mo | <1,5 | Заболевание растений, склонность к кариесу | >4 | Подагра, молибденовый токсикоз | ||
| J | <15 | Нарушение работы щитовидной железы, эндемичный зоб, замедление метаболизма, бесплодие; эндемия усиливается при несбалансированности с Со Мn, Сu, | 5-40 | >40 | Ослабление синтеза йодистых соединений | |
Cd - самый опасный элемент на все формы рака, костные заболевания.
Se - единственный токсичный элемент, избыток которого в растениниях до 0,05 г/т приводит к внезапной смерти человека и животных; наступает мускульная, в частности сердечная слабость
+ Норма пороговых содержаний
Целый ряд элементов, особенно тяжелые, являются ядами. Кроме 22 радионуклидов, имеются 13 металлов (Be, Al, Cr, As, Se, Ag, Cd, Sn, Sb, Ba, Hg, Tl, Pb) токсичных во всех своих водо-, щелоче- и кислотнорастворимых соединениях. И - многие тысячи органических веществ, преимущественно синтетического происхождения.
Ю.А. Ершов и Т.В. Плетнева (1989) приводят порядок расположения токсичных элементов в периодах и группах системы Д.И. Менделеева (табл.13.2).
Таблица 13.2
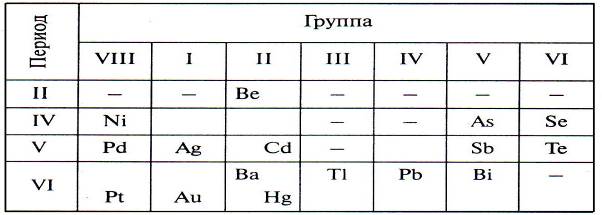
За исключением Be и Ba, все эти элементы образуют прочные сульфидные соединения. Эти элементы называются примесными. Их диаграмма доза - эффект имеет другую форму по сравнению с жизненно необходимыми (рис. 13.2).
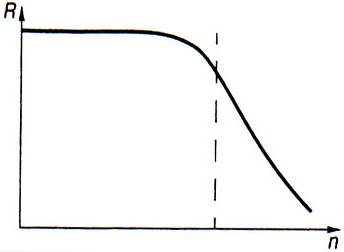
Рис. 13.2. Зависимость ответной реакции (R) от дозы (n) для приместных химических элементов
До определенного содержания этих элементов организм не испытывает вредного влияния, но при увеличении концентрации они становятся ядовитыми: нет ядовитых веществ, есть ядовитые концентрации.
As - сильный яд, нарушающий сердечно-сосудистую систему и поражающий почки и печень, но он же в малых дозах полезен и улучшает аппетит. Кислород при высокой концентрации ядовит. Ag в малых дозах бактерициден (колларгол применяют для промывки гнойных ран, мочевого пузыря, при хронических циститах и уретитах, в виде глазных капель при гнойном конъюктивите и беннорее; карандашами из нитрата серебра прижигают бородавки - возможно при взаимодействии с белками тканей образуются белковые соединения Ag - альбуминаты). Ag в повышенных количествах содержится в мозгу, железах внутренней секреции, печени.
Возглавляет неорганические токсины "страшная троица" - Pb, Cd, Hg.
Pb используется в широком спектре технических изделий: электрокабели, аккумуляторы, химическое машиностроение, атомная промышленность (защита), в производстве эмалей, лаков, хрусталя, пиротехники, пластмасс, пьезоэлектрике и т.п. Велико использование в транспорте. Потребляется свыше 2,5 млн т в год.
В воды попадает 500-600 тыс. т, оседает из атмосферы около 400 тыс. т, то есть около 1 млн т возвращается в виде загрязнений.
Окись свинца накапливается в костном скелете, изменяет ус-ловнорефлекторную деятельность, активность некоторых ферментов и гистологическую структуру головного и спинного мозга, увеличивается масса семенников и предстательной железы, нарушается сперматогенез.
При хронической токсификации свинцом происходит изменение нервной системы, возникают головные боли, головокружения, раздражительность, мышечная дистония, потливость.
ПДК в воздухе 3 мкг/м3, воды 0,03 мг/л, почв 20 мг/кг, у растений 2-3 мкг. Ежедневное поступление Pb в организм человека 70-400 мкг.
Основной источник поступления - пища, особенно растительная.
При неполноценном питании поступление Pb в кровь увеличивается.
Содержание в хлорированной воде больше, чем в исходной.
Cd. Используется в Ni-Cd аккумуляторах, бытовых батарейках, стержнях атомных реакторов, в сплавах, катализаторах, лазерных материалах, красителях, стабилизаторах, в виде антикоррозионного и декоративного покрытий.
Характерна избирательная аккумуляция в табаках.
К типичным Cd-заболеваниям горожан относятся гипертония, ишимическая болезнь сердца, почечная недостаточность, бронхиты, фарингиты.
Накапливается во всех тканях и органах, но более всего в почках и печени.
Поступление в организм составляет около 150 мкг/сут., а ДСД (допустимая суточная доза) - около 70 мкг.
Cd замещает цинк в Zn-содержащих ферментах, но с потерей их ферментативных свойств.
Hg. Применяется главным образом в электротехнической и электрохимической промышленности, в лабораторных приборах, лекарственных препаратах, фунгицидах.
Соединения токсичны, особенно сулема - HgCl2.
1/2 выбросов Hg природного происхождения.
Пары Hg поражают нервную систему.
Микромеркуализм приводит к быстрой утомляемости, повышенной возбудимости, ослаблению памяти, раздражительности, головным болям, дрожанию конечностей.
Существуют водные микроорганизмы, способствующие переводу Hg в диметилртуть - Hg(CH3)2.
Постоянно присутствует в организме (около 10 мг) в почках и печени, задерживается в легких.
ПДК 0,0003 мг/м3 в воздухе, 0,0005 мг/л в воде, t0,5 около 70 суток.
Недавно (70-е гг. XX столетия) выяснено, что к токсинам относится и Al. При нарушении деятельности почек, накапливание Al приводит к хрупкости костей, нарушению метаболизма Ca, Mg, P, F и развитию анемии. Наблюдается нарушение речи, провалы памяти, ориентации, помутнение рассудка, конвульсии. Все это симптомы мозгового заболевания - диализной энцифалопатии. Отклонения здоровья сходны с сиптомами болезни Альцгеймера ("старческий маразм").
Обогащение питьевой воды Al начинается на водоочистительной станции из-за обработки сульфатом аммония. Повышение содержания [Al 3+], а не [H+] приводит к гибели рыб, земноводных и моллюсков в водоемах, "обработанных" кислотными дождями.
Открытие токсичности Al сравнивается с "выстрелом в спину".
Из органических токсикантов наиболее опасны полиароматические углеводороды (ПАУ) иособенно диоксины (Д), образующиеся при сжигании топлива, мусора, в химическом, нефтехимическом и металлургическом производствах, в целлюлозно-бумажной промышленности (табл. 13.3).
Таблица 13.3
Характер воздействия органических загрязнителей на организмы
| Экотоксиканты | Химические стрессы | |
| Типы | Источники | |
| Альдрин, атразин, гептахлор, ДДТ, дильдрин, линдан, мирекс, токсафен, хлордан, хлордекон, эндосульфан, эндрин | Хлорорганические и другие пестицидные препараты | Биаккумуляция в жировых тканях организмов и трофических цепях, поражение центральной нервной и эндокринной систем, канцерогенез |
| Гексабромбифенил (ГББ) | Антивоспламе-нитель для термопластиков | Болезни кожи, выпадение волос, канцерогенез, эндокринные нарушения |
| Гекксахлорбензол (ГХБ) | Дымовые завесы, фейерверки | Болезни печени, канцерогенез |
| Нонил- и актилфеноны | Синтез детергентов, пластификаторов и стабилизаторов резины | Разрушение эндокринной системы у животных |
| Пентахлорфенолы (ПХВ) | Добавки в краски, текстиль, пестициды для защиты древесины | Токсичность по отношению к водной биоте и человеку |
| Полибромированные дифениловые эфиры (ПБДЭ) | Антивоспламенители для полиуретановых пен в коврах, матрицах и мебели | Канцерогенез, эндокринные нарушения и препятствия развитию мозга |
| Полихлорированные бифенилы (ПХБ) | Трансформаторные и смазочные масла, пластификаторы | Поражение эндокринных систем и проявление канцерогенеза |
| Полихлорированные дибензодиоксины (ПХДД) и дибензофураны (ПХДФ) | Микропримеси в ПХБ, хлорфенолах, пестицидах, продуктах сгорания ПХВ и отбеленной целлюлозе | Супертоксичность, проявление рератогенеза и канцерогенеза, поражение кожи (хлоракне), эндокринной, иммунной и репродуктивной систем |
| Полиядерные и араматические углеводороды (ПАУ) | Неполное сгорание древесины, угля и нефтепродуктов | Связывание метаболитами клеточной ДНК, возникновение раковых опухолей |
| Фталаты | Пластификаторы, репелленты, растворители | Связывание метаболитами клеточной ДНК, возникновение раковых опухолей |
| Метильные производные ртути | Метилирование катионов ртути (образуются в окружающей среде) | Разрушение центральной нервной системы, мозга и печени |
| Производные трибутил- и трифенилолова | Краски для судов и подводных конструкций, катализаторы, стабилизаторы ПВХ | Половые превращения молюсков и рыб (импосекс). Разрушение мозга человека и животных триметильными и триэтильными производными олова |
| Алкильные производные свинца | Антивзрывные добавки к топливу автомобилей | Онкологические заболевания дыхательного и пищеварительного трактов |
Все они основаны на химической структуре трех и более конденсированных бензольных веществ (рис. 13.3).
Среди наиболее опасных и стойких органических загрязнителей в настоящее время запрещены к использованию – альдрин, хлордан, дильдрин, эндрин, гептахлор, гексахлорбензол, мирекс, токсафен, полихлорированные бифенилы (ПХБ); ограничены в применении – ДДТ; запрещены к непреднамеренному производству – полихлорированные дибензо-n-диоксины (ПХДД) и полихлорированные дибензофураны (ПХДФ).
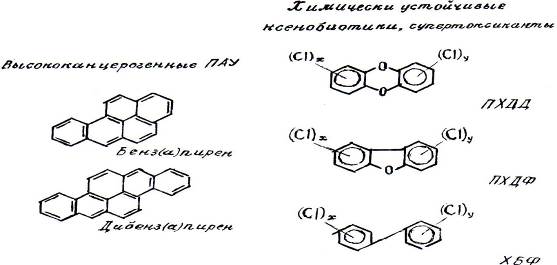
Рис. 13.3. Органические высококанцерогенные ПАУ и ксенобиотики
Главный адсорбент для ПАУ – пирена, бенз(а)пирена, бенз(а)нтрацена, дибенз(а)трацена и бензперилена - сажевые частицы.
Свойства диокинов политоксичны: онкологические заболевания, гибель плода в матке, рождение детей с уродствами (физическими и психическими), снижение и потеря иммунитета, потеря фертильности мужской спермы. 20% американских семей не могут иметь детей (а вскоре ожидается и 50%).
В организме концентрируются в жировой ткани.
Много Д (диоксина) образуется на мусоросжигающих заводах и сжигателях медицинских отходов (около 50%). Много поступает от предприятий химической промышленности и целлюлозно-бумажных комбинатов. Образуется и при лесных пожарах.
Для Д не существует таких норм, как ПДК.
Разработаны характеристики биологической активности химических элементов (табл. 13.4).
Таблица 13.4
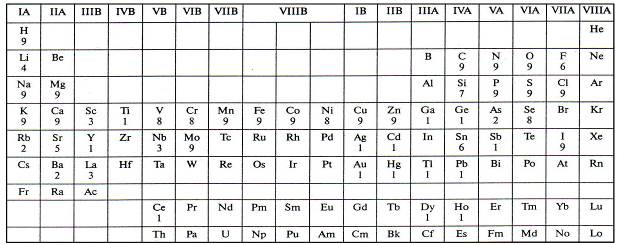
Учтены следующие симптомы (в порядке возрастания эффекта):
1 - снижение аппетита;2 - потребность в изменении диеты; 3 - значительные изменения состава тканей; 4 - повышенная повреждаемость одной или нескольких биохимических систем, проявляющаяся в специальных условиях; 5 - недееспособность этих систем в специальных условиях; 6 - субклинические признаки недееспособности; 7 - клинические симптомы недееспособности и повышенная повреждаемость; 8 - заторможенный рост; 9 - отсутствие репродуктивной функции.
Крайняя форма - смертельный исход.
Нет сомнения, что в живых организмах ионы металлов находятся в виде координационных соединений с "биологическими" молекулами, которые выполняют роль лигандов. Уже сформировалась новая отрасль химии - бионеорганическая химия.
2. Характеристики токсичности
Токсические эффекты живых организмов весьма разнообразны и могут быть специализированы по особенностям воздействия, по крайней мере на две основные группы токсикантов: тяжелые металлы (преимущественно ксенобиотики) и органические.
Механизмы токсического воздействия для первых можно подразделить на 4 категории:
1. Многие комплексы металлов с органическими лигандами близки по параметрам к обычным аминокислотам, гормонам, нейромедиаторам и поэтому могут связываться с соответствующими рецепторами, что приводит к эффекту мимикрии (подражательству), но без выполнения соответствующих органических функций.
2. Происходит замена биометаллов в металлсодержащих биокомплексах с утратой их биологической активности. Замена Zn на Hg или Pb приводит к дезактивации ферментов карбоангидразы, участвующей в синтезе гема.
3. Нарушается синтез цитохрома З-450, ответственного за биодеградацию ксенобиотиков, с накоплением в тканях и органах органических токсикантов и нарушением метаболизма.
4. Отмечена активация перекисного и свободнорадикального окисления, с повреждением белков, нуклеиновых кислот, липидов, биомембран в результате ингибирования ферментов, защищающих организм от накопления в нем H2O2.
Среди органических веществ, производимых человеком, много экотоксикантов (в том числе хлорорганических). Некоторые из них (хлорорганические пестициды...) обладают кумулятивным токсическим эффектом и накапливаются в жировых тканях. Способность атома Cl к нуклеофильному замещению объясняет их высокую биологическую активность. Реагируя с аминогруппами белков и нулеиновых кислот они вызывают их необратимое поражение.
Действие хлорорганических соединений (пестицидов) привело к увеличению размаха изменчивости и росту резистентных (устойчивых) видов насекомых-вредителей.
Особенно неблагоприятные последствия их использования проявляются в агроценозах, приводя к сокращению и без того бедного видового состава этих искусственных экосистем.
Токсические эффекты от особо опасных токсикантов могут быть следующими:
1.Эмбриотоксичные и терратогенные - повышение числа спонтанных абортов, рождение потомства с аномалиями развития.
2. Иммунотоксичные, аналогичные действию вируса СПИД.
3. Гистопатологические, вызывающие болезнь хлоракне (изменение клеток сальных желез кожи) и язвенную болезнь.
4. Метаболические, связанные с модуляцией активности.
5. Эндокринно-токсичные, связанные с влиянием на метаболизм гормонов типоксина, эстрогенов, андрогенов (подавление синтеза тестостерона приводит к устойчивой феминизации потомства).
6. Нейротоксичные (повышение нервозности, депрессии, снижение уровня умственного развития, что объясняют влиянием полихлорированных диоксинов и дибензофуранов на метаболизм некоторых нейротрансмиттеров в клетках головного мозга).
7. Канцерогенные (образование злокачественных опухолей).
8. Мутагенные (внезапное и резкое наследственное изменение того или иного признака или свойства организма).
Сейчас возможно определение риска рака с учетом двух ответственных за это биологических процессов: возрастания скорости деления клеток (литотической скорости) и увеличение скорости возникновения мутаций, не зависящих от литотической скорости. Различаются два типа канцерогенов: а) литотических (повышение вероятности спонтанных мутаций) и б) мутагенических канцерогенов, которые непосредственно влияют на ДНК (вызывая погрешности репликации).
Литотическая скорость строго контролируется физиологическими процессами, функционирующими через посредство сложной системы, которая включает разнообразные межклеточные молекулы-передатчики, что облегчает относительно устойчивую скорость деления клеток. Эти функции способны изменяться под влиянием внешних стрессов (потенциальных канцерогенов) лишь в определенных пределах, характеризующихся пороговой реакцией на малые воздействия стрессов. Пока эти стрессовые воздействия не выходят за пределы возможного физиологического контроля, литотическая скорость остается неизменной. Типично наличие определенного порога, зависящего от специфики индивидуальной физиологической реакции. Поэтому при малой концентрации литотические канцерогены должны рассматриваться как обычные токсиканты.
Классический мутагенез характеризуется пороговыми возмущениями, поскольку скорость мутаций контролируется физиологическими процессами. Введен термин "практический порог" (при воздействии ниже этого уровня их последствия не могут быть обнаружены). Почти каждая пища содержит малые количества канцерогенов. Таким образом, отрицание порогового уровня воздействия эквивалентно запрету на большую часть продуктов питания.
Ф. Корте приводит следующую общую схему химических воздействий на экосистемы по степени возрастания вредного последствия:
Направленное уничтожение отдельных видов растений и животных. Пример: альгицидные, фунгицидные, гербицидные... мероприятия.
Широко распространившееся уменьшение видового состава разнообразия организмов. Пример: использование пестицидов и удобрений.
Массированнае загрязнения. Пример: загрязнение нефтью при авариях.
Постоянное загрязнение биотопов. Пример: эвтрофикация после попадания в воды Р и N.
Глубокие изменения биотопа. Пример: засоление пресноводных биотопов.
Полное разрушение экосистемы в результате выпадения целостной интактной (нетронутой) структуры (биотопа) и ее функций (биоценоза). Пример: уничтожение мангровых лесов в результате применения гербицидов в качестве химического оружия во Вьетнамской войне.
Количественная характеристика токсичности веществ очень сложна.
В группах животных всегда существуют восприимчивые и резисторные представители. Поэтому нужна не частная, а общая характеристика. Такими являются две оценочные разновидности токсичности - ЛД50 и ЛД100 (летальные дозы, приводящие к поражению-гибели 50% животных или 100%). Доза обычно определяется в весе токсина на 1 кг живого веса объекта.
При воздействии дозами ниже летальных болезненное состояние организма может постепенно пройти. С мочей, фекалиями, потом, выдыхаемым воздухом происходит выведение токсина и продуктов его превращений из организма.
По аналогии с радиоактивным распадом, определено понятие времени полувыведения - t0,5. Оно колеблется от нескольких часов до нескольких десятков лет.
Кроме этих параметров, для определения характеристики токсичности необходимо знать и время гибели от ЛД50 и ЛД100.
У разных млекопитающих чувствительность к действию данных токсинов различна. Отсюда поиск "презентативных" лабораторных животных. Каждый яд действует по своему и поражает различные органы, ткани и т.п. Поэтому различные токсины по разному распределяются в организмах. Pb концентрируется в костях, Cd - в почках, большинство хлорорганических соединений - в жировых тканях, некоторые токсины - в клетках мозга.
Еще одно свойство токсинов - неаддитивность их действия. Токсический эффект от двух доз, введенных с временным интервалом, отличен от разового введения.
При непрерывном воздействии токсина вместо ЛД, то есть (Сорг - концентрация токсина в организме) используется характеристика ЛС50, ЛС100 (С - концентрация токсина в воде, воздухе или пище).
Поэтому на основе полученных зависимостей определяют предельно допустимые концентрации - ПДК для каждого вещества; это та концентрация, которая не вызывает негативного физиологического или поведенческого ответа организма. Близка к ПДК (время!) и ДСД (допустимая суточная доза).
Однако, и ПДК какого-либо токсина не отражает всей сложности воздействия токсикантов: многое зависит от форм нахождения элемента в растворах (табл. 13.5).
Таблица 13.5
Дата добавления: 2021-11-16; просмотров: 598;











