Структура белковой молекулы.
Органические вещества. Белки
Органические вещества.
Органические соединения составляют в среднем 20–30% массы клетки живого организма. К ним относятся биологические полимеры – белки, нуклеиновые кислоты и полисахариды, а также жиры и ряд низкомолекулярных органических веществ – аминокислоты, простые сахара, нуклеотиды и т.д. Полимеры – сложные разветвленные или линейные молекулы, при гидролизе распадающиеся до мономеров. Если полимер состоит из одного вида мономеров, то такой полимер называют гомополимером, если в состав полимерной молекулы входят различные мономеры – то это гетерополимер. Если группа различных мономеров в полимерной молекуле повторяется (А,Б,В,А,Б,В,А,Б,В) – это регулярный гетерополимер, если нет повторения определенной группы мономеров – гетерополимер нерегулярный.
|
Белки.
Из органических веществ клетки по количеству и значению на первом месте стоят белки. Белки, или протеины (от греч. протос – первый, главный) – высокомолекулярные гетерополимеры, органические вещества и распадающиеся при гидролизе до аминокислот. Значение белков настолько велико, что информация о белках включена в два наиболее популярных определения Жизни: «Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка» (Ф.Энгельс). «Живые тела, существующие на Земле, представляют собой открытые, саморегулирующиеся и самовоспроизводящиеся системы, построенными из биополимеров – белков и нуклеиновых кислот» (М.В.Волькенштейн).
В состав простых белков (состоящих только из аминокислот) входят углерод, водород, азот, кислород и сера. Часть белков (сложные белки) образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь – это сложные белки, содержащие помимо аминокислот еще и небелковую — простетическую группу. Она может быть представлена ионами металлов (металлопротеины — гемоглобин), углеводами (гликопротеины), липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеины).
Белки обладают огромной молекулярной массой: Один из белков – глобулин молока – имеет молекулярную массу 42000. Его формула С1864Н3012О576N468S21. Существуют белки, молекулярная масса которых в 10 и даже в 100 раз больше. Для сравнения: молекулярная масса спирта – 46, уксусной кислоты – 60, бензола – 78.
Белки представляют собой нерегулярные гетерополимеры, мономерами которых являются α-аминокислоты. В клетках и тканях обнаружено свыше 170 различных аминокислот, но в состав белков входит лишь 20 α-аминокислот. В зависимости от того, могут ли аминокислоты синтезироваться в организме, различают: заменимые аминокислоты – десять аминокислот, синтезируемых в организме и незаменимые аминокислоты – аминокислоты, которые в организме не синтезируются. Незаменимые аминокислоты должны поступать в организм вместе с пищей.
В зависимости от аминокислотного состава, белки бывают полноценными, если содержат весь набор незаменимых аминокислот и неполноценными, если какие-то незаменимые аминокислоты в их составе отсутствуют.
Общая формула аминокислот приведена на рисунке. Все α-аминокислоты при α-атоме углерода содержат атом водорода, карбоксильную группу (-СООН) и аминогруппу (-NH2). Остальная часть молекулы представлена радикалом.
|
|
Пептиды – органические вещества, состоящие из небольшого количества остатков аминокислот, соединенных пептидной связью. Образование пептидов происходит в результате реакции конденсации аминокислот (рис. ).
При взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой, между ними возникает ковалентная азот-углеродная связь, которую называют пептидной. В зависимости от количества аминокислотных остатков, входящих в состав пептида, различают дипептиды, трипептиды, тетрапептиды и т.д. Образование пептидной связи может повторяться многократно. Это приводит к образованию полипептидов. Если полипептид состоит из большого количества остатков аминокислот, то его уже называют белком. На одном конце молекулы находится свободная аминогруппа (его называют N-концом), а на другом – свободная карбоксильная группа (его называют С-концом).
Структура белковой молекулы.
Выполнение белками определенных специфических функций зависит от пространственной конфигурации их молекул, кроме того, клетке энергетически невыгодно держать белки в развернутой форме, в виде цепочки, поэтому полипептидные цепи подвергаются укладке, приобретая определенную трехмерную структуру, или конформацию. Выделяют 4 уровня пространственной организации белков.
Первичная структурабелка – последовательность расположения аминокислотных остатков в полипептидной цепи, составляющей молекулу белка. Связь между аминокислотами – пептидная.
|
В организме человека обнаружено порядка десяти тысяч различных белков, которые отличаются как друг от друга, так и от белков других организмов.
Именно первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке приводит к изменению свойств и функций белка. Например, замена в b-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к тому, что молекула гемоглобина в целом не может выполнять свою основную функцию – транспорт кислорода (в таких случаях у человека развивается заболевание – серповидноклеточная анемия).
Первым белком, у которого была выявлена аминокислотная последовательность, стал гормон инсулин. Исследования проводились в Кембриджском университете Ф.Сэнгером с 1944 по 1954 год. Было выявлено, что молекула инсулина состоит из двух полипептидных цепей (21 и 30 аминокислотных остатков), удерживаемых около друг друга дисульфидными мостиками. За свой кропотливый труд Ф.Сэнгер был удостоен Нобелевской премии.
|
Cкладчатый слой (синоним β-структра) формируется в том случае, если сегменты полипептидных цепей располагаются параллельно или антипараллельно друг другу в один слой. При этом образуется фигура, напоминающая лист, сложенный гармошкой.
|
У некоторых белков третичная структура стабилизируется дисульфидными ковалентными связями, возникающими между атомами серы двух остатков цистеина. На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны. По форме молекулы различают белки глобулярные и фибриллярные. Если фибриллярные белки выполняют в основном опорные функции, то глобулярные белки растворимы и выполняют множество функций в цитоплазме клеток или во внутренней среде организма.
|
Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин. Он образован двумя a-субъединицами (141 аминокислотный остаток) и двумя b-субъединицами (146 аминокислотных остатков).С каждой субъединицей связана молекула гема, содержащая железо.
|
Если по каким-либо причинам пространственная конформация белков отклоняется от нормальной, белок не может выполнять свои функции
Свойства белков.
Аминокислотный состав, структура белковой молекулы определяют его свойства. Белки сочетают в себе основные и кислотные свойства, определяемые радикалами аминокислот, чем больше кислых аминокислот в белке, тем ярче выражены его кислотные свойства. Способность отдавать и присоединять Н+ определяют буферные свойства белков, один из самых мощных буферов — гемоглобин в эритроцитах, поддерживающий рН крови на постоянном уровне.
Есть белки растворимые (фибриноген), есть нерастворимые, выполняющие механические функции (фиброин, кератин, коллаген).
Есть белки активные в химическом отношении (ферменты), есть химически неактивные, устойчивые к воздействию различных условий внешней среды и крайне неустойчивые.
|
Причиной денатурации является разрыв связей, стабилизирующих определенную структуру белка. Первоначально рвутся наиболее слабые связи, а при ужесточении условий и более сильные. Поэтому сначала утрачивается четвертичная, затем третичная и вторичная структуры. Изменение пространственной конфигурации приводит к изменению свойств белка и, как следствие, делает невозможным выполнение белком свойственных ему биологических функций.
Если денатурация не сопровождается разрушением первичной структуры, то она может быть обратимой, в этом случае происходит самовосстановление свойственной белку конформации. Такой денатурации подвергаются, например, рецепторные белки мембраны. Процесс восстановления структуры белка после денатурации называется ренатурацией. Если восстановление пространственной конфигурации белка невозможно, то денатурация называется необратимой. Разрушение первичной структуры белка называется деградацией.
Функции белков.
Благодаря сложности, разнообразию форм и состава, белки играют важную роль в жизнедеятельности клетки и организма в целом. Функции их разнообразны.
| Функция | Примеры и пояснения |
| 1. Строительная | Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. |
| 2. Транспортная | Белок крови гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят особые белки, которые обеспечивают активный и строго избирательный перенос некоторых веществ и ионов из клетки во внешнюю среду и обратно. |
| 3. Регуляторная | Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например, гормон инсулин регулирует уровень глюкозы в крови, способствует синтезу гликогена, увеличивает образование жиров из углеводов. |
| 4. Защитная | В ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов) образуются особые белки — антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений |
| 5. Двигательная | Сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных |
| 6. Сигнальная | В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды, таким образом осуществляя прием сигналов из внешней среды и передачу команд в клетку. |
| 7. Запасающая | В организме животных белки как правило не запасаются, исключение: альбумин яиц, казеин молока. Но благодаря белкам в организме могут откладываться про запас некоторые вещества, например, при распаде гемоглобина железо не выводится из организма, а сохраняется в организме, образуя комплекс с белком ферритином. |
| 8. Энергетическая | При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов — воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. |
| 9. Каталитическая | Одна из важнейших функций белков. Обеспечивается белками - ферментами, которые ускоряют биохимические реакции, происходящие в клетках. Например, рибулезобисфосфаткарбоксилаза катализирует фиксацию СО2 при фотосинтезе. |
Ферментыилиэнзимы – особый класс белков, являющихся биологическими катализаторами. Благодаря ферментам биохимические реакции протекают с огромной скоростью. Скорость ферментативных реакций в десятки тысяч раз (а иногда и в миллионы) выше скорости реакций, идущих с участием неорганических катализаторов. Вещество, на которое оказывает свое действие фермент, называют субстратом.
Ферменты – глобулярные белки, по особенностям строения ферменты можно разделить на две группы: простые и сложные. Простые ферментыявляются простыми белками, т.е. состоят только из аминокислот. Сложные ферменты являются сложными белками, т.е. в их состав помимо белковой части входит группа небелковой природы — кофактор. У некоторых ферментов в качестве кофакторов выступают витамины. В молекуле фермента выделяют особую часть, называемую активным центром. Активный центр – небольшой участок фермента (от трех до двенадцати аминокислотных остатков), именно в котором происходит связывание субстрата или субстратов с образованием фермент-субстратного комплекса. По завершении реакции фермент-субстратный комплекс распадается на фермент и продукт (продукты) реакции. Некоторые ферменты имеют (кроме активного) аллостерические центры–участки, к которым присоединяются регуляторы скорости работы фермента (аллостерические ферменты).
Для реакций ферментативного катализа
|
Субстратную и реакционную специфичность реакций ферментативного катализа объясняют гипотезы Э.Фишера (1890) и Д.Кошланда (1959). Э.Фишер (гипотеза «ключ-замок») предположил, что пространственные конфигурации активного центра фермента и субстрата должны точно соответствовать друг другу. Субстрат сравнивается с "ключом", фермент – с «замком».
Д.Кошланд (гипотеза «рука-перчатка») предположил, что пространственное соответствие структуры субстрата и активного центра фермента создается лишь в момент их взаимодействия друг с другом. Эту гипотезу еще называют гипотезой индуцированного соответствия.
Большинство неорганических катализаторов ускоряют химические реакции при очень высоких температурах, имеют максимальную эффективность в сильнокислой или сильнощелочной среде, при высоких давлениях, а большинство ферментов активны при температурах 35-45˚С, физиологических значениях кислотности раствора и при нормальном атмосферном давлении; скорость ферментативных реакций в десятки тысяч (а иногда и в миллионы раз) выше скорости реакций, идущих с участием неорганических катализаторов. Например, пероксид водорода без катализаторов разлагается медленно: 2Н2О2 → 2Н2О + О2. В присутствии солей железа (катализатора) эта реакция идет несколько быстрее. Фермент каталаза (М=252000) за 1 сек. расщепляет 100 тыс. молекул Н2О2 (М=34). Известно более 2000 различных ферментов, представленных белками с высокой молекулярной массой.
Скорость ферментативных реакций зависит от 1) температуры, 2) концентрации фермента, 3) коцентрации субстрата, 4) рН. Следует подчеркнуть, что поскольку ферменты являются белками, то их активность наиболее высока при физиологически нормальных условиях.
|
При увеличении количества молекул субстрата скорость ферментативной реакции растет до тех пор, пока не произойдет насыщение активных центров фермента – если активный центр каталазы расщепляет в секунду 100 000 молекул субстрата, то при количестве молекул субстрата более 100 000 на активный центр скорость реакции не возрастет.
Увеличение концентрации фермента приводит к усилению каталитической активности, так как в единицу времени преобразованиям подвергается большее количество молекул субстрата.
Для каждого фермента существует оптимальное значение рН, при котором он проявляет максимальную активность (пепсин – 2,0, амилаза слюны – 6,8, липаза поджелудочной железы – 9,0). При более высоких или низких значениях рН активность фермента снижается. При резких сдвигах рН фермент денатурирует.
|
Классификация ферментов. По типу катализируемых химических превращений ферменты разделены на 6 классов: 1) оксиредуктазы (перенос атомов водорода, кислорода или электронов от одного вещества к другому – дегидрогеназа), 2) трансферазы (перенос метильной, ацильной, фосфатной или аминогруппы от одного вещества к другому – трансаминаза), 3) гидролазы (реакции гидролиза, при которых из субстрата образуются два продукта – амилаза, липаза), 4) лиазы (негидролитическое присоединение к субстрату или отщепление от него группы атомов, при этом могут разрываться связи «С-С», «С-N», «С-О», «С-S» – декарбоксилаза), 5) изомеразы (внутримолекулярная перестройка – изомераза), 6) лигазы (соединение двух молекул в результате образования связей «С-С», «С-N», «С-О», «С-S» – синтетаза
| <== предыдущая лекция | | | следующая лекция ==> |
| | | Ключевые термины и понятия |
Дата добавления: 2017-11-21; просмотров: 2363;

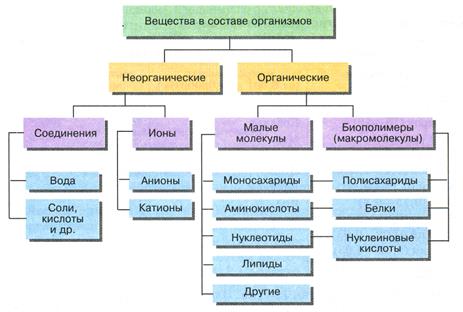
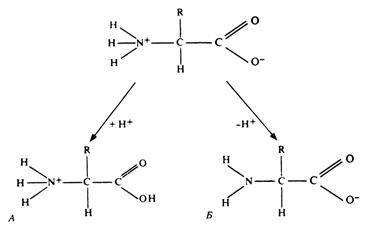 Рис. 255. Амфотерные свойства аминокислот при различных рН.
Рис. 255. Амфотерные свойства аминокислот при различных рН.
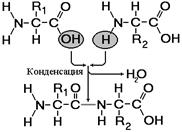 Рис. 256. Образование дипептида.
Рис. 256. Образование дипептида.
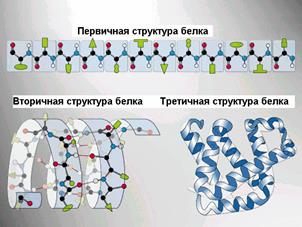
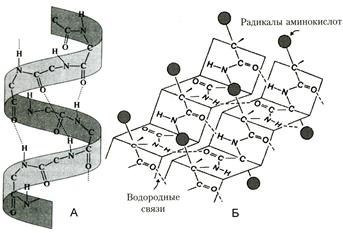 Рис. . Вторичные структуры белка
Рис. . Вторичные структуры белка
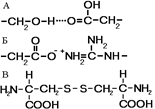 Рис. . Связи, стабилизирующие третичную структуру:
А — водородные, Б — ионные, В — дисульфидные.
Рис. . Связи, стабилизирующие третичную структуру:
А — водородные, Б — ионные, В — дисульфидные.
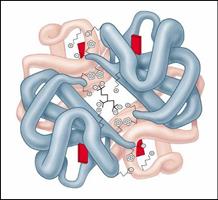 Рис. . Молекула гемоглобина
Рис. . Молекула гемоглобина
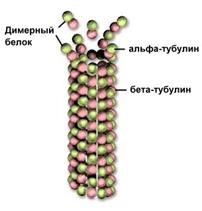 Рис. . Микротрубочка из тубулина
Рис. . Микротрубочка из тубулина
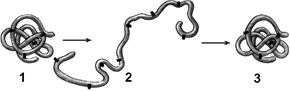 Рис. . Денатурация и ренатурация белка:
1 — молекула белка третичной структуры; 2 — денатурированный белок; 3 — восстановление третичной структуры в процессе ренатурации.
Рис. . Денатурация и ренатурация белка:
1 — молекула белка третичной структуры; 2 — денатурированный белок; 3 — восстановление третичной структуры в процессе ренатурации.
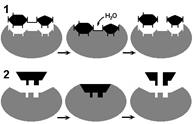 Соответствие фермента и субстрата:
1 — гипотеза «ключ – замок»; 2 — гипотеза «рука - перчатка».
Соответствие фермента и субстрата:
1 — гипотеза «ключ – замок»; 2 — гипотеза «рука - перчатка».
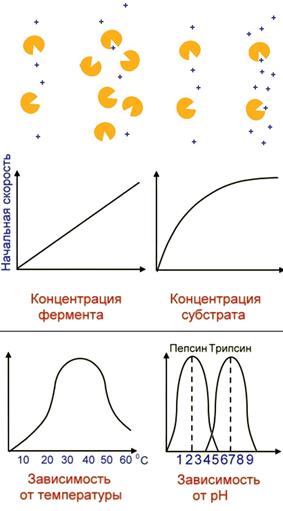 Рис. . Зависимость скорости реакции от концентрации фермента, субстрата, рН, температуры
Рис. . Зависимость скорости реакции от концентрации фермента, субстрата, рН, температуры
 Рис. . Алостерическое активирование и ингибирование ферментов
Рис. . Алостерическое активирование и ингибирование ферментов










