Биологическое действие радиации.
Действие ионизирующих излучений на живые организмы изучают с тех пор, как французскому ученому Андре Беккерелю в1896 г. удалось открыть явление радиоактивности. К ионизирующим относятся рентгеновские и гамма-излучения проявляющиеся в виде порций энергии, или так называемых квантов.
Пролетая над оболочкой атома, кванты и частицы способны вырывать из нее электрон. Лишившись отрицательно заряженного электрона, атомы и молекулы становятся положительно заряженными ионами. Так в общих чертах происходит процесс ионизации атомов и молекул. Наряду с этим при взаимодействии ионизирующих излучений с растворителями биологических молекул (водой или жирами) возникают и другие продукты ионизации — свободные радикалы (активные фрагменты молекул), обладающие одним или двумя не спаренными электронами.
Ионы и радикалы в силу своей высокой реактивности способны вступать в сложные химические реакции с другими молекулами, а сверх того выбитые радиацией электроны могут вызывать все новые и новые акты ионизации. Такая цепь событий приводит обычно к различным деструктивным изменениям макромолекул, из которых построены живые системы.
Удивительно различной оказалась чувствительность к радиации биологических макромолекул, находящихся в пробирке (вне организма) и в составе живых клеток. Повреждение 0,001—0,1% ДНК, практически не улавливаемое вне организма, приводит к катастрофе, если эти макромолекулы находятся в составе живой клетки. Такое различие возможно объяснить прежде всего двумя причинами. Во-первых, макромолекулы ДНК, из которых состоят гены, уникальны. Они содержатся в ядре клетки в количестве одной, двух или нескольких копий. Значит, повторяемость их ограничена. Во-вторых, в живой клетке и в целом организме существуют разного рода механизмы, многократно усиливающие первоначальный эффект. Это усиление проявляется, например, в том, что изменение (мутация) всего лишь одного гена в половой клетке в последующем — при оплодотворении ее и созревании плода — воспроизводит эту мутацию во всех клетках организма в форме отклонений в структуре и функциях.
Лимфоциты и другие клетки иммунной системы являются соматическими клетками. Наиболее полно изучен процесс гибели соматических клеток в результате облучения. Различают две основные разновидности гибели клеток при их контакте с радиацией: репродуктивную (в момент деления клеток) и интерфазную (в период покоя — между предшествующим и последующим делением).
В обоих случаях главная причина гибели клеток кроется в нарушении хромосом, а точнее, разрыва молекул ДНК. Каждая хромосома состоит из двух нитей ДНК. В зависимости от мощности радиации разрыв может произойти в одной или в обеих нитях ДНК.
Единичные разрывы одной нити легко залечиваются (восстанавливаются). Для этого в клетке "существует специальная репарационная система с набором восстановительных ферментов. А если происходит одновременный разрыв обеих нитей. В этом случае нити разъединяются, репарация становится клетка, как правило, погибает. При интенсивном облучении погибают любые делящиеся клетки (репродуктивная гибель), и прежде всего те, которые имеют двухнитевой разрыв ДНК. Интерфазная гибель связана с процессом созревания «покоящихся» клеток и является уделом лишь немногих типов клеток, в число которых входят лимфоциты. Интерфазные клетки погибают быстро — в течение первых суток после облучения. Механизмы ее реализации не до конца изучены. Существует представление, что интерфазная гибель – это ускорение естественной, генетически запрограммированной гибели клеток. Первоначально под влиянием фермента эндонуклеазы разрушается ДНК, а вслед за этим происходит невосстанавливаемое нарушение целостности клеточных мембран. Такая форма гибели наблюдаете не только при радиационном облучении, но и при действии на клетку УФ-лучей, кортикостероидных гормонов и некоторых лекарств. Следовательно, фактор радиации не имеет каких-либо особых отличий от физиологических факторов, запускающих биологические процессы. Вероятно, клетки способны переводить любые молекулярные события, возникшие под действием различных внешних факторов, на стандартный язык внутриклеточных сигналов.
Репродуктивная и интерфазная формы гибели облучаемых клеток являются причиной радиационного поражения высших организмов. При этом в связи с гибелью лимфоцитов опустошаются органы иммунной системы поочередно в две волны. Раннее опустошение возникает в результате интерфазной гибели. Более позднее наступает попричине репродуктивной гибели клеток. Репродуктивной гибели, как было сказано, подвержены все интенсивно., обновляющиеся ткани. В их число входят кроветворная, иммунная, генеративная ткани, слизистые ткани кишечника и т.д. Именно их поражение составляет наибольшую часть патологического процесса, который называют лучевой болезнью.
Более целостную картину общего лучевого поражения организма в зависимости от дозы мы рассмотрим с помощью табл.1.
Табл.1 Шкала биологических эффектов при общем облучении
| Доза(грей) | Эффект |
| ~2000 | Смерть под лучом |
| 10--100 | Церебральная форма лучевой болезни (коматозное состояние, летальный исход через 1-2 часа) |
| 6--10 | Кишечная форма лучевой болезни ( тяжелое поражение слизистой кишечника, летальный исход 3-12дней) |
| 4--6 | Костномозговая форма лучевой болезни( тяжелое поражение костного мозга, нарушение слизистой кишечника) |
| 2--4 | Средняя тяжесть лучевой болезни ( сокращение средней продолжительности жизни на 3-9лет) |
| 1--2 | Иммунодифицитное состояние( пострадиационный канцерогенез) |
| 0,5--1 | Нарушение кроветворения, первичные нарушения иммунитета, удвоение мутаций, учащение злокачественных новообразований |
| 0,1--0,5 | Временная мужская стерильность |
| 0,05--0,1 | Регистрация мутаций |
| 0,002--0,05 | Стимуляция жизнедеятельности |
| 0,001--0,002 | Оптимум жизнедеятельности |
| Менее 0,001 | Угнетение жизнедеятельности |
Однако и на данной схеме шкала биологических эффектов пострадиационного действия минимальна. Помимо этих эффектов, имеются и другие — различные нарушения функций иммуноцнтов, количественного соотношения различных форм иммуноцнтов при их кооперативных взаимодействиях, радиационное старение облученных органов, иммунной системы и т. д.
При этом следует сказать, что для всех ионизирующих излучений принято различать три дозы Поглощенную дозу определяют по количеству, энергии, поглощенной облучаемым объектом, и выражают в греях. Экспозиционную определяют по ионизационному эффекту в воздухе при нормальных условиях и обозначают «кулон на кг» Эквивалентную определяю по биологическим эффектам и выражают в зивертах.
В таблице № 2 приведены единицы измерения указанных доз в международной системе единиц-—СИ и соотношение их с внесистемными (производными) единицами.
Особо следует оговорить соотношение единиц поглощенной, экспозиционной и эквивалентной доз для гамма- и рентгеновского излучений, где 1 Гр=1 ЗБ, а 1 рад= 1 бэр. В связи с тем что степень поражаемости (радиочувствительность) биологических объектов определяется поглощенной дозой излучения и восприимчивостью данного объекта к действию радиации, дозы на рис. 1 в основном тексте выражены нами в греях.
Табл.2
| Наименование дозы | Единица измерения,СИ | Производные единицы |
| Экспозиционная | Кл/кг | Рентген(р) |
| Поглощенная | Грей(Гр) | Рад |
| Эквивалентная | Зиверт(Зв) | Бэр |
Радиационное поражение иммунной системы
Для того чтобы разобраться в особенностях действия радиации на различные звенья иммунной системы, нам необходимо ответить на вопрос - каким образом определяют радиочувствительность биологических объектов. Считают, что радиочувствительность зависит от поглощенной дозы и восприимчивости биологического объекта к радиации. Ее оценивают на разных биологических уровнях по-разному.
Радиочувствительность на уровне организма, к примеру, оценивают с помощью,ЛД50/30 - летальной дозы, вызывающей гибель 50% облученных организмов в течение 30 дней после облучения; на уровне клеток с помощью дозы, обозначаемой Д37. Дело в том, что радийочувствительность клеток удобнее : всего измерять в дозах, при которых на одну клетку в среднем приходится одно смертельное попадание частиц или квантов энергии. Но из-за того что попадания распределяются случайно, некоторые клетки поражаются дважды или трижды, а другие вообще остаются непораженными. По законам статистики таких непораженных клеток оказывается -37%. Поэтому Д37 взята за критерий оценки радночувствительности клеток. Для гибели клеток любых типов в момент деления Д37 примерно одинакова и составляет 1 Гр. Аналогичная доза и для лимфоцитов, вступающих в деление. Чувствительность интерфазных (покоящихся) клеток разнообразнее, поэтому Д37 для них варьирует от 0,5 до 3 Гр.
Если говорить о дозе, то радиационная гибель клеток заметно проявляется в пределах 1 Гр. По мере увеличения дозы число погибающих клеток нарастает вплоть до 6—7 Гр. После этого в организме остаются только радиоустойчнвые клетки лимфоидных тканей - макрофаги, элементы стромы ( эпителъные и соединительнотканные клетки), составляющие каркас органов, а также некоторая часть функционально зрёлых лимфоцитов, неуязвимых для радиации.
Если говорить о времени, то лимфоциты погибают в несколько этапов. Впервые сутки (спустя 6 - 12 часов) после облучения начинается интерфазная гибель клеток, которая приводит к весьма ощутимым последствиям. По мере гибели клеток уменьшаются размеры всех лимфоидных органов. Они как бы опустошаются, хотя их тканевый каркас сохраняется полностью. Вслед за этим начинается второй этап опустошения лимфоидных органов. Он идет в течение, последующих 3—4 суток, но значительно медленнее. На этом этане причиной опустошения становится репродуктивная гибель делящихся клеток. Деление клеток в этом случае провоцируется притоком различных (микробных) антигенов, нашествие которых усиливается в связи с нарушением естественных барьеров (кожи, слизистых тканей и т. д.).
Радиационное нарушений барьерных функций кожи и слизистых, строго говоря, не имеет прямого отношения к иммунной системе. Но это обстоятельство свидетельствует о том, насколько важны целостность и сохранение взаимосвязей различных систем для общей безопасности организма.
Радиационное нарушение естественных барьеров наводнение организма бактериальной флорой и переход большинства лимфоцитов к делению создают самый драматический период в отношениях между лимфоцитами м радиацией. Только через 3 - 4 дня меняется ситуация. При относительно переносимой дозе она меняется к лучшему. Клетки, не задетые или слабо задетые радиацией; перейдя в фазу покоя, могут развиваться дальше, переходить в фазу зрелости, а в дальнейшем и выполнять свои иммунологические функции. Потомки В-лимфоцитов (антителопродуценты) начинают выделять антитела, Т-киллеры—активно разрушать клетки - мишени,а Т-хелперы - синтезировать и выделять необходимые для межклеточного взаимодействия регуляторные белки (интерлейкины и т. д.).
На стадии функциональной зрелости лимфоциты, как правило, устойчивы к радиации даже в дозе нескольких десятков греев. В этом состоянии им не грозит интерфазная гибель, а опасность репродуктивной гибели они миновали.
Однако ситуация меняется при получении труднопереносимых доз облучения. Иммунной системе очень трудно возместить колоссальные потери. Поэтому всякий раз, когда облученные лимфоциты атакуются массой антигенов, на карту ставится не только жизнеспособность лимфоидных клеток, но и жизнь самого организма.
Говоря об интерфазной и репродуктивной гибели лимфоцитов мы, по существу, обсуждаем радиочувствительность двух фаз жизненного цикла этих клеток— фазы покоя и фазы деления, хотя фаза покоя—понятие весьма относительное. В этот период жизненного цикла клетки либо дифференцируются, т. е созревают переходя от одной стадии развития к другой, либо, достигнув стадии зрелости; выполняют свои прямые функциональные обязанности. Как видим, радиочувствительность разных стадий развития может отличаться весьма значительно. Проиллюстрируем это на примере :Т—клеток. Самые юные формы Т-клеток, ранние тимоциты и самые радиоустойчивые. Благодаря им организм, попадая в тяжелые ситуации, оказывается небезоружным при восстановлении облученной популяции Т-клеток. Клетки следующей стадии— кортикальные тимоциты, напротив, самые радиочувствительные клетки иммуннои системы, а может.быть, и всего организма. Они необыкновенно хрупкие и поэтому при любых стрессовых ситуациях поражаются первыми. Даже в норме большая их часть погибает, не выходя из тимуса. На следующей стадии развития, перед встречей с антигеном, клетки хотя и радиочувствительны еще, но намного меньше, чем корковые тимоциты.
При сравнительном изучении радиочувствительности иммуноцитов выявилось, что В-лимфоциты, ответственные за образование антител более радиочувствительны, чем Т-лимфоциты, а среди них Т-хелперы.: (особенно те, которые участвуют в реакциях клеточного, а не гуморального иммунного ответа). Именно Т-лнмфоциты обнаруживаются среди немногочисленных выживших лимфоцитов в лимфоидных органах после действия высоких доз радиации (десятки греев). Отметим, что популяций В-клеток более однородны по радиочувствительности, нежели Т-клетки.
Отсюда и разная степень поражения клеточных и гуморальных форм иммунного ответы, ведь он определяется радиочувствительностью клеток, ответственных за эти формы ответа-(рис. 1).
Рис1.Радиочувствительность различных типов иммунного ответа
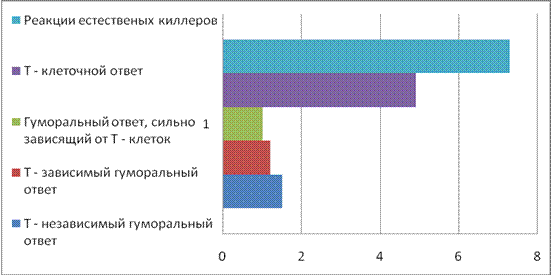
Иммунологические реакции, в основе которых лежит ответ В-лимфоцитов (образование антител), сильнее страдают от радиации, чем Т – клеточные реакции. Более уязвимой оказывается антибактериальная защита, связанная с продукцией антител, и менее — противовирусная защита, зависимая от Т-лимфоцитов. Однако нет правил без исключения, о чем свидетельствуют и супрессорные клетки. Их нестимулироваиные антигенами предшественники ничем не отличаются по радиочувствительности, от большей части других Т-клеток. После же контакта с антигенами и созревания в функционально активные формы Т-супрессоры оказываются в особом положений. Вместо того чтобы после стимуляции стать радиоустойчивыми, они сохраняют довольно высокую радиочувствительность. Поэтому большая их часть погибает при дозах 4 - 6 Гр.
Довольно устойчивы к радиации естественные киллеры (ЕК-клеткик) ответственные за противоопухолевый иммунитет. Д37 для них находится в пределах 7—8 Гр. Им не нужен предварительный контакт с антигенами, чтобы выполнить функцию клеток-убийц или приобрести радиоустойчивость.
Клетки памяти более радиоустойчивы, чем «девственные>, не контактировавшие с антигеном, лимфоциты. Этим объясняется большая радиоустойчивость вторичного иммунного ответа по сравнению с первичным иммунным ответом.
Однако разница между радиочувствительностью девственных лимфоцитов и. клетками памяти не столь велика, чтобы, ею можно было объяснить различия между радиочувствительностью первичного и вторичного ответов. Этот процесс, оказалось, зависит не только от особенностей клеток, но и от высокой оснащенности вторичного ответа. Дело в том, что в наличии всегда оказывается гораздо больше клеток, чем требуется для эффективного иммунного ответа. Поэтому гибель какого-то процента клеток до определенного момента почти не сказывается на уровне иммунного ответа.
При облучении очень уязвимыми оказываются все процессы, связанные с межклеточными контактами. Без кооперативного взаимодействия между Т-В-А- клетками практически, не обходится ни одна реакция иммунного ответа. Существует два вида межклеточного взаимодействия - гуморальный (дистанционный) и клеточный (контактный). При облучении сильнее, поражается второй, что связано со специфическим нарушением рецепторных систем клеточных мембран. Мы уже упоминали, что В-клетки не всегда способны в одиночку справиться с тем или иным очагом заболевания. И тогда к ним на помощь спешат Т-клетки, чтобы контактным способом завершить иммунный процесс. Однако очень часто процесс прерывается, так как чем сильнее задействованы межклеточные контакты в иммунных реакциях, тем сильнее на них действует облучение. Иммунный ответ в значительной степени зависит от того, когда произошла встреча иммуноцитов с антигенами – до и после облучения. В эксперименте эти процессы изучают на животных, проводя их иммунизацию, т.е вводят им антигены.
При облучении, нарушается процесс, избирательного проникновения лимфоцитов из кровяного русла в лимфоидные органы. В этом случае нарушается, как говорят иммунологи «домашний нстинкт» лимфоцитов, т. е. их способность находить свой дом (лимфоидные органы). Причина – в нарушении мембранных систем распознавания этих клеток. Нарушается путь миграции лимфоцитов в лимфоузлы кишечника, дыхательных путей и т. д., хотя в селезенку путь, остается свободным, что объясняется своеобразным строением ее капилляров. Поэтому и возникает такая ситуация, когда лимфоциты беспрепятственно проникают в селезенку, но не могут мигрировать в лимфоузлы. А это для них очень важно, ибо именно в лимфоузлах они рекрутируются, призываются на службу для защиты организма от внешней и внутренней агрессии. Поэтому подавление иммунного ответа в лимфоузлах выражено сильнее, чем в селезенке.
После облучения иммунитет подавляется в результате поражения иммуноцитов и проявляется в снижении максимальных показателей иммунных реакций (титра антител, активности киллеров) и замедлении темпов по установлению «нового максимального уровня» этих показателей. Все это оказывает вредное влияние на защитимые функции, особенно от внешней биологической агрессии. Облученная иммунная система не в состоянии дать надлежащий отпор микробам, наполняющим организм после облучения. Продукты жизнедеятельности микробов, оказывают на организм дополнительное иммунодепрессивное действие. Ситуация осложняется и тем, что наряду с патогенной флорой начинает активизировать и проявлять патогенные свойства облигатная (безвредная или частично полезная) микрофлора, до того мирно обитавшая в дыхательном и пищеварительном трактах и на коже. Таким образом формируются вторичные иммунодефицитные состояния, причина которых так называемые оппортунистические инфекции.
Проблема перехода облигатных микробов в условно-патогенное состояние становится все более острой в связи с ухудшением экологической обстановки в окружающей нас среде. И роль радиации здесь, как мы знаем, значительна.
В радиационной иммунологии при обсуждении радиочувствительности чаще всего речь идет о радиационной гибели клеток. В действительности же дело не исчерпывается только тем, выживет клетка или погибнет. Ведь выжившие после облучения клетки не всегда сохраняют свою функцию. Как правило, нарушается биоэнергетический потенциал клеток, работа ядерного аппарата, мембранных систем и т. д. Полное выздоровление у облученных клеточных популяций наступает редко, а восстановление их функциональных качеств обычно сопряжено с их количественным обновлением. Функциональные нарушения без гибели более характерны для макрофагов и других вспомогательных клеток иммунной системы.
Не вызывает никаких сомнений снижение устойчивости к возбудителям инфекций (инфекционного иммунитета). А вот действие радиации на противоопухолевый иммунитет сложнее. Хотя облучение и повышает частоту появления опухолей, однако развиваются они в более поздние сроки.
Кратко рассмотрим результаты радиационного воздействия на аутоиммунные процессы. С первого взгляда кажется неожиданным: почему на фоне общего уровня аутоиммунных процессов активизируются реакции, направленные против антигенов собственных клеток и тканей. В норме терпимость (толерантность) к собственным антигенам надежно обеспечивается механизмами центральных и периферических органов иммунной системы.
В момент созревания лимфоцитов на уровне центральных органов формируется первый щит - выбраковка клеточных клонов, направленных против собственных антигенов. Второй щит — запрет на реакции против своих антигенов осуществляется супрессорами, которые накладывают свое «вето» на конфликт между иммунной системой и клетками собственного тела. Но радиация, поражает оба щита, нарушает законы толерантности. В результате наблюдается деструкция тканей и органов тела, аутоантигены высвобождаются из-под влияния естественных взаимосвязей, ослабляется реакция на «чужое» и усиливается реакция на «свое». А это означает, что радиация не просто подавляет иммунитет она извращает согласованную работу иммунной системы, нарушает основы ее деятельности..
Все рассказанное позволяет нам сделать следующие обобщения. Поражение клеток, приводящее к их гибели или снижению функциональной активности, — вот причина ослабления иммунитета. Самые радиочувствительные — лимфоциты. Среди и субпопуляций и лимфоцитов существуют свои внутренние различия. В-лимфоциты более чувствительны к облучению, чем Т-лимфоциты. В пределах популяции Т-клеток обнаруживаются различия. Самые радиоустойчивые из них Т-хелпер, а самые радиочувствительные Т-суппрессоры. К радйоустойчивым принадлежат также естественные киллеры и магкрофаги. Большая часть лимфоцитов при облучении гибнет в интервале от 0,5 до 6 Гр. В первые сутки гибнут в основном интерфазные клетки, а в следующие 3—4 суток (как правило, в присутствии антигена) гибнут делящиеся клетки.
Всё лимфоциты (кроме супрессоров) после контакта с антигеном и достижения зрелой (эффекторной) стадии приобретают повышенную радиоустойчивость. В результате облучения наиболее поражаемым оказывается противоннфекционный иммунитет. Противоопухолевый иммунитет также поражается, но последствия обнаруживаются лишь спустя продолжительное время. Аутоиммунитет в отличие от двух первых, напротив, усиливается. Несмотря на относительно высокую радиочувствительность лимфоцитов, иммунная система самая уязвимая среди других систем организма в пределах доз не выше среднелетальных именно от иммунной системы, ответственной за индивидуальную целостность конкретного организма.
Факторы влияющие на радиационное поражение. На конечный биологический эффект влияют различные факторы, которые в основном делятся на физические, химические и биологические. Среди физических факторов на первом месте стоит вид излучения,характеризуемый относительной биологической эффективностью. Различия биологического действия обусловлены линейным переносом энергии данного вида ионизирующего излучения, связанным с плотностью ионизации и определяющим способность излучения проникать в слои поглощающего его вещества. ОБЭ представляет величину отношения дозы стандартного излучения (изотоп 60Со или рентгеновское излучение 220 кВ) к дозе исследуемого излучения, дающей равный биологический эффект. Так как для сравнения можно выбрать множество биологических эффектов, для испытуемого излучения существует несколько величин ОБЭ. Если показателем пострадиационного действия берется катарактогенный эффект, величина ОБЭ для нейтронов деления лежит вдиапазоне 5—10 в зависимости от вида облученных животных, тогда как по важному критерию — развитию острой лучевой болезни — ОБЭ нейтронов деления равняется примерно 1. Следующим существенным физическим фактором является доза ионизирующего излучения, которая в Международной системе единиц (СИ) выражается в грэях(Гр). 1 Гр=100 рад, 1 рад=0,975 Р. От величины поглощенной дозы зависят развитие синдромов радиационного поражения и продолжительность жизни после облучения. При анализе отношения между дозой, получаемой организмом млекопитающего, и определенным биологическим эффектом учитывается вероятность его возникновения. Если эффект появляется в ответ на облучение независимо от величины поглощенной дозы, он относится к разряду стохастических. За стохастические принимаются, например, наследственные эффекты излучения. В отличие от них нестохастические эффекты наблюдаются по достиженииопределенной пороговой дозы излучения. В качестве примера можно указать помутнение хрусталика, бесплодие и др. В Рекомендациях Международной комиссии по радиологической защите (№ 26,1977 г.) стохастические и нестохастические эффекты определены следующим образом: «Стохастическими называют те беспороговые эффекты, для которых вероятность их возникновения (а не столько их тяжесть) рассматривают как функцию дозы. Нестохастическими называют эффекты, при которых тяжесть поражения изменяется в зависимости от дозы и, следовательно, для появления которых может существовать порог». Химические радиозащитные вещества в зависимости от их эффективности снижают биологическое воздействие излучений в лучшем случае в 3 раза. Предотвратить возникновение стохастических эффектов они не могут. К существенным химическим факторам, модифицирующим действие ионизирующего излучения, относится концентрация кислорода в тканях организма у млекопитающих. Его наличие в тканях, особенно во время гамма- или рентгеновского облучения, усиливает биологическое воздействие радиации. Механизм кислородного эффекта объясняется усилением главным образом непрямого действия излучения. Присутствие же кислорода в облученной ткани по окончании экспозиции дает противоположный эффект. Для характеристики облучения, наряду с величиной общей дозы, важноезначение имеет продолжительность экспозиции. Доза ионизирующей радиации независимо от времени ее действия вызывает в облученном организме одно и то же число ионизаций. Различие, однако, состоит в объеме репарации радиационного поражения. Следовательно, при облучении меньшей мощности наблюдается меньшее биологическое поражение. Мощность поглощенной дозы выражается в грэях за единицу времени, например Гр/мин, мГр/ч и т. д. Изменение радиочувствительности тканей организма имеет большоепрактическое значение. Данная книга посвящена радиопротекторам, а также веществам, снижающим радиочувствительность организма, однако это не означает, что мы недооцениваем исследования радиосенсибилизаторов; их изучение ведется прежде всего в интересах радиотерапии. КЛАССИФИКАЦИЯ И ХАРАКТЕРИСТИКА РАДИОЗАЩИТНЫХ ВЕЩЕСТВ Радиозащитный эффект обнаружен у целого ряда веществ различной химической структуры. Поскольку эти разнородные соединения обладают самыми различными, подчас противоположными свойствами, их трудно разделить по фармакологическому действию. Для проявления радиозащитного эффекта в организме млекопитающего в большинстве случаев достаточно однократного введения радиопротекторов. Однако имеются и такие вещества, которые повышают радиорезистентность лишь после повторного введения. Различаются радиопротекторы и по эффективности создаваемой ими защиты. Существует, таким образом, множество критериев, по которым их можно классифицировать. С практической точки зрения радиопротекторы целесообразно разделить по длительности их действия, выделив вещества кратковременного и длительного действия. 1. Радиопротекторы или комбинация радиопротекторов, обладающих кратковременным действием (в пределах нескольких минут или часов), предназначены для однократной защиты от острого внешнего облучения. Такие вещества или их комбинации можно вводить тем же особям и повторно. В качестве средств индивидуальной защиты эти вещества могут найти применение перед предполагаемым взрывом ядерного оружия, вхождением в зону радиоактивного загрязнения или перед каждым радиотерапевтическим местным облучением. В космическом пространстве они могут быть использованы для защиты космонавтов от облучения, вызванного солнечными вспышками. 2. Радиозащитные вещества длительного воздействия предназначены для более продолжительного повышения радиорезистентности организма. Для получения защитного эффекта, как правило, необходимо увеличение интервала после введения таких веществ примерно до 24 ч. Иногда требуется повторное введение. Практическое применение этих протекторов возможно у профессионалов, работающих с ионизирующим излучением, у космонавтов при долговременных космических полетах, а также при длительной радиотерапии.Поскольку протекторы кратковременного защитного действия чаще всегоотносятся к веществам химической природы, говорят о химической радиозащите. С другой стороны, длительное защитное действие возникает после введения веществ в основном биологического происхождения; это обозначают как биологическую радиозащиту. Требования к радиопротекторам зависят от места применения препаратов; вусловиях больницы способ введения не имеет особого значения. В большинстве случаев требования должны отвечать задачам использования радиопротекторов в качестве индивидуальных средств защиты. Согласно Саксонову и соавт. (1976)эти требования должны быть как минимум следующими: — препарат должен быть достаточно эффективным и не вызывать выраженных побочных реакций; — действовать быстро (в пределах первых 30 мин) и сравнительно продолжительно (не менее 2 ч); — должен быть нетоксичным с терапевтическим коэффициентом не менее 3; — не должен оказывать даже кратковременного отрицательного влияния на трудоспособность человека или ослаблять приобретенные им навыки; — иметь удобную лекарственную форму: для перорального введения или инъекции шприц-тюбиком объемом не более 2 мл; — не должен оказывать вредного воздействия на организм при повторных приемах или обладать кумулятивными свойствами; — не должен снижать резистентность организма к другим неблагоприятным факторам внешней среды; — препарат должен быть устойчивым при хранении, сохранять свои защитные и фармакологические свойства не менее 3 лет. Менее строгие требования предъявляются к радиопротекторам,предназначенным для использования в радиотерапии. Они усложняются, однако, важным условием — необходимостью дифференцированного защитного действия. Следует обеспечить высокий уровень защиты здоровых тканей и минимальный -тканей опухоли. Такое разграничение позволяет усилить действие местно примененной терапевтической дозы облучения на опухолевый очаг без серьезного повреждения окружающих его здоровых тканей.
| <== предыдущая лекция | | | следующая лекция ==> |
| Структура пищевой цепи в морской экосистеме | | | Побочные эффекты дискретизации |
Дата добавления: 2017-01-16; просмотров: 8563;











