СПЕКАНИЕ С ФТОРСИЛИКАТНЫМИ РЕАГЕНТАМИ
В технологии редких металлов используют методы вскрытия руд спеканием их с кремнефтористым натрием или калием. Использование фтора, связанного в химическое соединение, уменьшает коррозию. При нагревании фторсиликаты натрия и калия разлагаются на SiF4 и соответствующий фторид металла. Термическая диссоциация становится заметной уже примерно с 450° С.
Вскрытие берилла спеканием с Na2SiF6
Метод был предложен Копо около 50 лет назад. В основе его лежит реакция
ВеO . Al2O3 . 6SiO2 + 6Na2SiF6 ® 3Na2ВеF4 + 2Na3AlF6 + 9SiO2 + 3SiF4
Спекание осуществляют при 750-850° С.
Полученный фторбериллат натрия растворим в воде. Алюминий и железо образуют труднорастворимые криолиты, а кремнезем не вступает в реакцию. Можно значительно сократить количество кремнефторида натрия, если ввести в реакцию соду. Схематически это можно отразить реакцией:
3ВеO . Al2O3 . 6SiO2 + 2Na2SiF6 + Na2СО3® 3Na2ВеF4 + Al2O3 + 8SiO2 + CO2
Это уравнение не точно. На самом деле часть Na2SiF6 (примерно 1/3) расходуется все же на связывание алюминия, а также кальция и магния, входящих в состав слюды, практически всегда сопровождающей берилл.
Фторбериллат натрия выщелачивают водой, и из раствора осаждают гидроокись бериллия. В зависимости от условий получения она образуется в трех модификациях: аморфной, метастабильной a-форме и кристаллической b-форме. Аморфная гидроокись получается при осаждении на холоду и представляет собой студенистый осадок состава Ве(ОН)2.хН2О, сорбирующий до 95% воды. При старении она переходит в метастабильную a-форму, гораздо хуже растворимую в щелочах, карбонатах щелочных металлов и кислотах, b-форма осаждается при кипячении раствора бериллатов.
Для осаждения хорошо фильтрующейся гидроокиси к части раствора (примерно 1/5 всей загрузки) добавляют все количество раствора NaOH. При этом образуется бериллат натрия. Раствор нагревают до кипения и вливают новые порции фторбериллата натрия, поддерживая раствор кипящим. При этом протекает реакция
Na2ВеF4 + NaOH® Be(OH)2 + 4NaF
Задача утилизации получающегося фторида натрия решается добавлением к фильтрату сульфата железа. При рН = 4, скорректированном добавлением серной кислоты, выпадает в осадок железный криолит:
12NaF + Fe2(SO4)3 ® 2Na3FeF6 + Зnа2SO4.
Феррофторид натрия используют для вскрытия в голове процесса:
3ВеO . Al2O3 . 6SiO2 + 6 Na3FeF6 ® 3Na2ВеF4 + + Al2O3 + Fe2O3 + 6SiO2
Гидроокись бериллия, получаемая по этому методу, в случае использования бериллия как материала в ядерной технике должна быть дополнительно очищена. Один из наиболее эффективных способов очистки состоит в получении основного ацетата бериллия Ве4O(СН3СОО)6 и его очистке перегонкой с последующим разложением.
Основной ацетат бериллия образуется при обработке технической гидроокиси бериллия уксусной кислотой. Полученный продукт перегоняется без разложения при 360-400° С и разлагается пиролизом при 600-700° С. Табл. 21 дает представление о достигаемой степени очистки.
Таблица 21
Содержание некоторых примесей в технической гидроокиси и окиси бериллия, полученной пиролизом основного ацетата, % к ВеО
| Примесь | Техническая гидроокись | Очищенная окись | Примесь | Техническая гидроокись | Очищенная окись |
| Fe | 0,3-0,1 | 1-3.10-3 | Сu | 0,01-0,015 | 5.10-4 |
| А1 | 0,5-1,5 | 3,7.10-3 | Ni | 0,003-0,005 | 2.10-3 |
| Si | 0,1-0,5 | 0,01-0,02 | В | 10-3 | 10-5 |
| Мп | 0,01-0,015 | 3.10-4 |
Получаемая ацетатным способом окись бериллия удовлетворяет требованиям по чистоте, предъявляемым к материалам для ядерных реакторов.
На рис. 37 приведена технологическая схема получения гидроокиси бериллия фтористым способом.
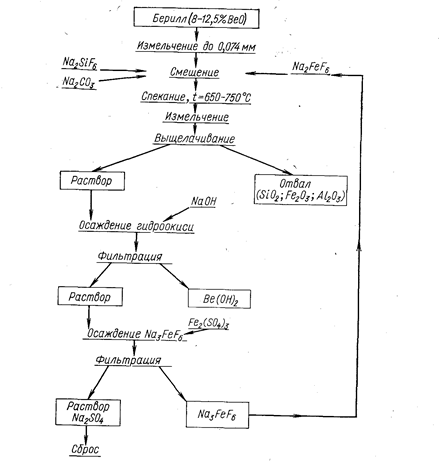
Рис. 37. Технологическая схема получения гидроокиси бериллия.
Измельченный бериллий смешивают в мельнице-смесителе с 60% железного криолита и 40% кремнефтористого натрия. В шихту добавляют также соду в количестве не более 25% теоретически необходимого для образования бериллата натрия. Смешанные продукты с небольшим количеством воды в виде пасты брикетируют. Средний размер брикета 200х63х75 мм. Брикеты сушат, а затем спекают в туннельной печи, через которую они продвигаются на специальных, футерованных огнеупором вагонетках. Время выдержки спека при 750° С составляет 2 ч. Вскрытие проходит на 90%.
Спеченные брикеты легко измельчаются и затем выщелачиваются водой. Пульпу отфильтровывают на барабанном вакуумном фильтре, и осадок промывают до содержания в нем водорастворимого бериллия <0,3%.
Фильтрат переводят в бериллат натрия, и при кипячении из него осаждают гидроокись бериллия. Осадок отфильтровывают и промывают горячей водой.
Вскрытие циркона спеканием с K2SiF6
Вскрытие циркона спеканием с фторсиликатом калия предложили Н. П. Сажин и Е. А. Пепеляева. Метод основан на получении фторцирконата и фторгафната калия с последующим их разделением фракционной кристаллизацией. Использовать при спекании более дешевый фторсиликат натрия не представляется возможным, так как фторцирконат натрия гораздо хуже растворяется в воде по сравнению с калиевой солью.
Фторсиликат калия может быть получен из Na2SiF6 конверсией с КС1: Na2SiF6 + 2KCl = K2SiF6+2NaCl. Реакцию осуществляют в растворе при 80-90о С (рис. 38).
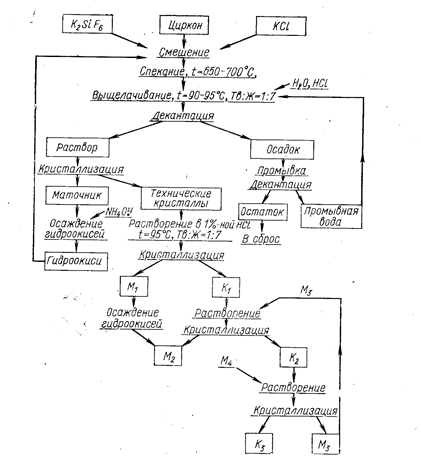
Рис. 38. Технологическая схема вскрытия циркона спеканием с K2SiF6.
Спекание проводят во вращающейся печи при температуре 650-700° С. Реакцию можно представить уравнением
ZrSiO4 + K2SiF6 ® K2ZrF6 + 2SiO2.
Добавка в шихту хлорида калия повышает скорость реакции и содействует полноте ее протекания. Не следует допускать перегрев реакционной массы, так как это приводит к потерям циркония в виде летучего фторида.
Спекшийся продукт выходит из печи в виде гранул размером в несколько миллиметров. Выщелачивание ведут в шаровой мельнице и затем в реакторах.
На 1 т опека расходуется примерно 7 т воды. Выщелачивание проводят водой, подкисленной соляной кислотой (около 1%-ной), при 90-95° С. Время выщелачивания 1,5-2 ч.
Горячий раствор декантируют, а осадок промывают водой, которую затем используют для выщелачивания.
Раствор охлаждают до обычной температуры. Кристаллы фторцирконата калия, обедненные гафнием, выпадают в осадок, так как их растворимость несколько ниже, чем у соответствующей гафниевой соли. Растворимость K2ZrF6 при 95° С составляет около 200 г/л, при 19° С - 16,3 г/л.
Кристаллы отделяют от раствора и передают на перекристаллизацию; 16-18 кристаллизации позволяют снизить содержание гафния во фторцирконате с 2,5 до 0,01 %.
Если использовать для каждой стадии кристаллизации свежую воду, выход продукта не превысит 10%. Поэтому каждую следующую кристаллизацию проводят в маточном растворе от предыдущей. Общее извлечение циркония при этом достигает 80%. Первый маточный раствор выводят из цикла. В нем происходит накапливание гафния.
Дата добавления: 2019-05-21; просмотров: 782;











