Круговорот веществ, биогеохимические циклы
Круговорот веществ, биогеохимические циклы - обмен веществом между различными компонентами экосистем и биосферы в целом, повторяющиеся цепочки химических, физических и биологических процессов.
Термин «биогеохимические циклы» был введен в нач. 20 в. академиком В. И. Вернадским, создателем учения о биосфере. До него считалось, что круговороты веществ в природе замкнуты, он же доказал, что они открыты: часть вещества выбывает из цикла (например, при захоронении в горных породах), с другой стороны, идет постоянное пополнение участвующих в круговороте веществ.
Различают круговороты, происходящие в отдельных экосистемах, и круговороты, охватывающие всю биосферу. Однако процессы эти, разумеется, взаимосвязаны. Так же как и биологические, и геологические процессы, хотя время обращения веществ в них очень различно.
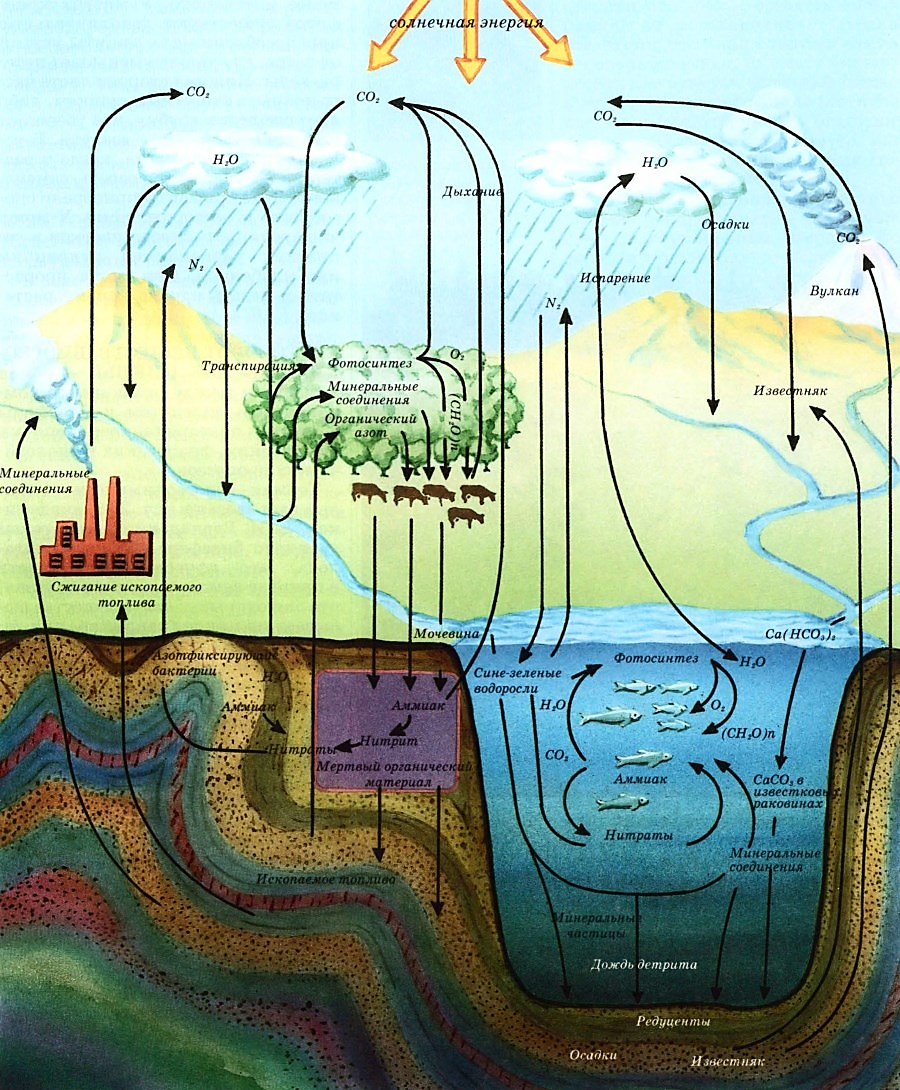
Рис. Круговорот углерода, азота и воды
Наиболее важны для понимания жизни на Земле и эволюции биосферы круговороты т. н. биогенных элементов — химических элементов, постоянно входящих в состав всех организмов и необходимых им для жизни. Хотя в клетках можно обнаружить в некоторых количествах практически все элементы, только ок. 20 из них встречаются практически всегда и в больших количествах.
В первую очередь это кислород (он составляет до 70 % массы организмов), углерод (18 %), водород (10 %), азот, кальций, калий, фосфор, сера, хлор, магний, натрий — они есть во всех клетках всех организмов, образуя важнейшие органические соединения (белки, жиры, углеводы, нуклеиновые кислоты). Некоторые биогенные элементы жизненно необходимы только некоторым группам организмов: например бор — растениям. Состав и концентрация биогенных элементов в разных организмах зависят как от физиологических, биохимических и экологических особенностей самих организмов, так и от содержания этих элементов в окружающей среде.
Различия в ходе геологической и биологической эволюции Земли привели к образованию на планете биогеохимических провинций, различающихся по содержанию химических элементов, прежде всего — биогенных. Биогенные элементы участвуют практически во всех процессах, протекающих в биосфере, — геологических (от извержения вулканов до выщелачивания горных пород) и биологических (включая фотосинтез, дыхание, перемещение по пищевым цепям). При этом складываются глобальные биогеохимические циклы этих элементов. Важнейшее значение среди них имеют циклы углерода и азота.
Количество углерода в веществах, образующих тела всех организмов на Земле, составляет 553 Гт (гигатонн, т. е. миллиардов тонн). Из них 550 Гт сосредоточены на суше, и только 3 Гт — в океане. Большая часть углерода входит в состав целлюлозы и лигнина — основного «строительного материала» наземных растений. После отмирания растительных тканей эти вещества медленно разлагаются, превращаясь в органическое вещество почвы — гумус.
Количество углерода, входящего в состав гумуса, в несколько раз превышает то, которое содержится в живых организмах. В океане в результате отмирания живущих в поверхностных слоях воды мелких организмов — планктона — образуются взвешенные в воде частицы органического вещества — так называемый детрит. Эти частицы обрастают бактериями и становятся ценным кормом для мелких рачков.
Помимо частиц детрита в океанических водах присутствует и большое количество растворенного органического вещества — 700 Гт углерода, что более чем в 230 раз превышает количество углерода, образующего тела морских организмов. Но еще больше углерода растворено в морской воде в форме ионов карбонатов и бикарбонатов — ок. 42 млн Гт.
Однако главные запасы углерода сосредоточены в осадочных породах. Присутствует он здесь в двух формах — так называемом керогене и карбонатах. Кероген — это органическое вещество, представляющее собой сильно измененные остатки мягких тканей организмов. Карбонаты (углекислые кальций и магний), из которых состоят известняки и доломиты, образованы остатками раковин и скелетов различных морских беспозвоночных. Количество углерода, связанное в керогене, оценивается как 15 млрд Гт, а в карбонатах — 60 млрд Гт. Углерод в составе молекул С02 присутствует и в атмосфере. Хотя общее количество его здесь не так велико — 750 Гт (чуть больше, чем в живых организмах), оно необходимо для поддержания жизни на Земле. Именно С02 — основной источник углерода для растений.
Рис. Всевозможные морские организмы используют, ионы кальция и бикарбоната для построения раковин
Углерод на Земле участвует в непрерывном круговороте. Геохимический цикл углерода, протекающий миллионы лет, начинается на суше, где происходит химическое разрушение (так называемое выветривание) горных пород, а именно карбонатов (СаСО3) и силикатов (CaSi03). Основное вещество, фигурирующее в этой реакции, — угольная кислота Н2СО3, которая постоянно образуется в почве в результате соединения С02, выделяющегося при разложении органических остатков, и воды.
Взаимодействие угольной кислоты с карбонатами и силикатами приводит к образованию ионов кальция Са+2 и бикарбоната НСО а также растворенного в воде кремнезема Si02. Все эти компоненты сначала попадают в реки, а затем выносятся в океан, где ионы кальция и бикарбоната используются всевозможными морскими организмами для построения раковин (состоящих из СаСО3). При этом С02 снова выделяется в окружающую среду.
Геохимический цикл углерода теснейшим образом переплетается с биологическим — гораздо более быстрым, протекающим за несколько лет. Ведь даже С02, на основе которого образуется угольная кислота, есть продукт разложения органического вещества. Образование в море карбонатов — также результат деятельности организмов. Основное же движение углерода в природе, происходящее при участии живых существ — это поглощение С02 растениями и цианобактериями и выделение его в процессе дыхания всех организмов, в первую очередь грибами и бактериями.
Азот — второй важнейший биогенный элемент — входит в нуклеиновые кислоты и белки. Хотя азота организмам нужно примерно в 7 раз меньше, чем углерода, именно его нехватка чаще всего ограничивает рост растений и на суше, и в океане. Молекулярный азот N2 — самый распространенный газ воздуха, но это в высшей степени инертное соединение: два атома его, образующие молекулу, соединены очень крепкой связью, а для того, чтобы ее разорвать, требуется очень большое количество энергии.
Эту энергию приходится затрачивать тем немногим организмам, которые способны использовать атмосферный азот для своих нужд. Азотфиксация, по-видимому, возникла очень давно, еще до того, как в атмосфере появился в больших количествах кислород. В океане основные азотфиксаторы — это свободноживущие планктонные цианобактерии, а на суше большую часть азотфиксации осуществляют бактерии, образующие тесный симбиоз с высшими растениями.
После отмирания организмов азот (главным образом в виде аминокислот) попадает в почву или в воду, где есть бактерии, осуществляющие аммонификацию — превращения его в ионы аммония NH4. После этого к работе приступают уже другие группы бактерий, которые окисляют ион аммония до нитритов (N02), а потом и нитратов (N03). Совокупность этих процессов, так называемая нитрификация, требует наличия в окружающей среде свободного кислорода. Большая часть азота почвы находится в виде нитратов.
Часть азотистых соединений накапливается в осадочных породах, а часть претерпевает так называемую денитрификацию — превращение в свободный молекулярный азот. Процесс этот весьма выгоден с энергетической точки зрения, но происходить может только в анаэробных условиях. В эволюции глобального круговорота азота денитрификация (по сути, замыкающая этот самый круговорот), возникла позже нитрификации.
Другие биогенные элементы, подобно углероду и азоту, также находятся в постоянном движении. Совокупность таких биогеохимических циклов обеспечивает целостность биосферы.
Дата добавления: 2024-10-24; просмотров: 597;











