Производство энтропии при смешении двух потоков, имеющих одинаковый состав, но разную температуру.
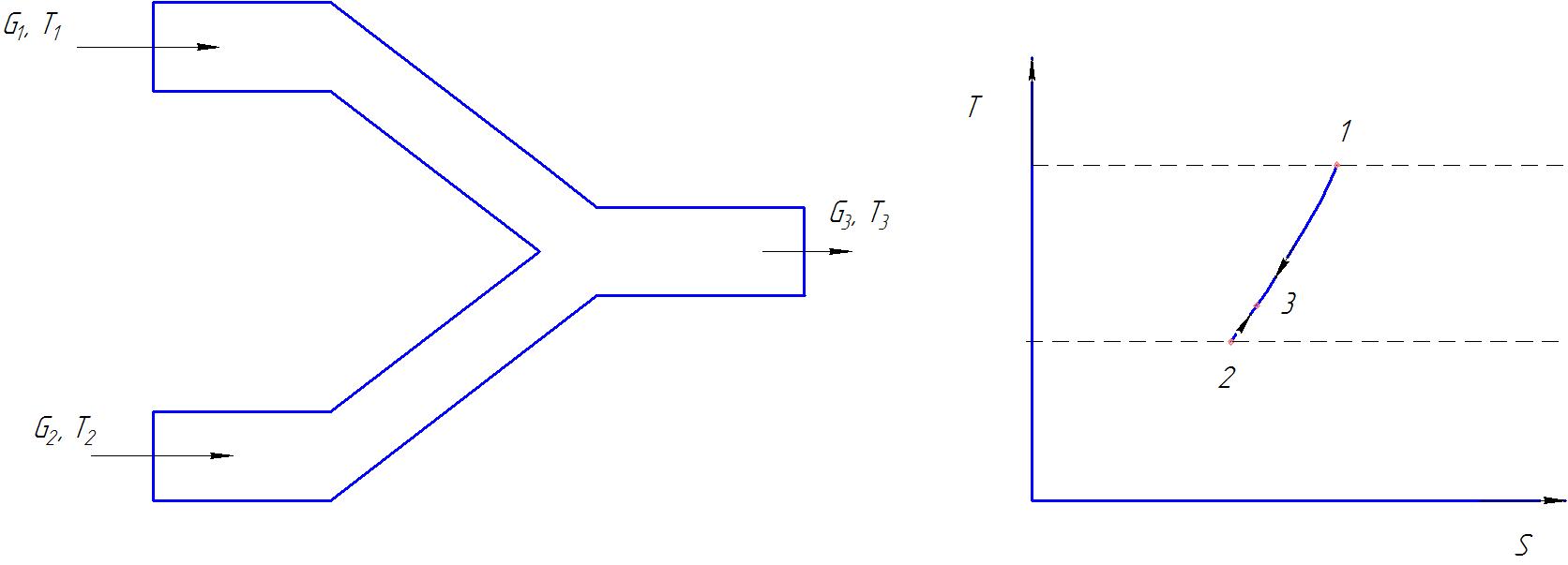
Рисунок 26. Смешение.
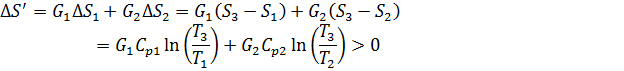
Пример.
| Дано: Газ – азот p=0.1 МПа T1=150 К T2=100 К G1 = 4 кг/c G2 = 6 кг/c Найти производство энтропии при смешении. | Решение:
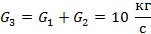
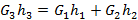 энтальпии для азота при давлении p=0.1 Мпа
энтальпии для азота при давлении p=0.1 Мпа
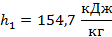
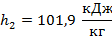
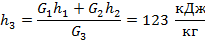 данной энтальпии при p=0.1 МПа соответствует температура
данной энтальпии при p=0.1 МПа соответствует температура
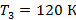
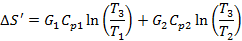
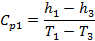
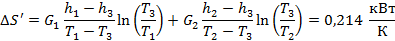
|
Лекция 9.
T-S диаграммы состояния вещества.
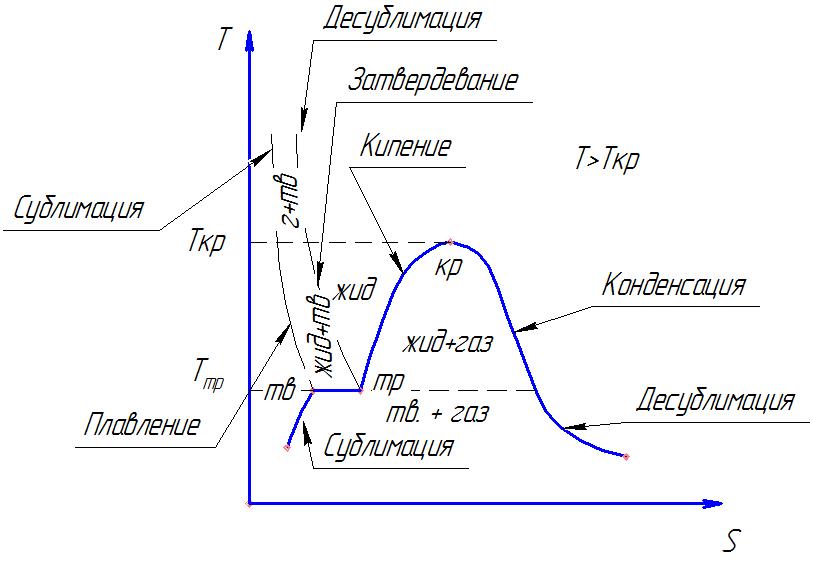
Рисунок 27. T-S диаграмма.
Твёрдое состояние рассматривать не будем.
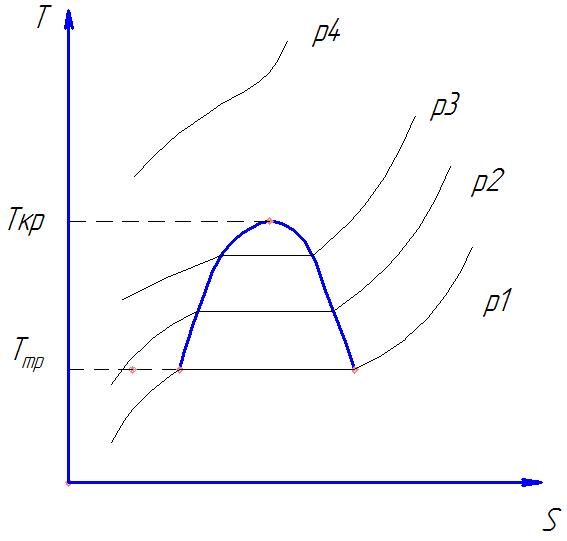
Рисунок 28. T-S диаграмма без твердого состояния с изобарами.
Обычно в T-S координатах не указываются изобары ниже 0,1 бара вследствие того, что разреженный газ при низких давлениях ведёт себя как идеальный и для определения его параметров достаточно уравнения состояния идеального газа.
При давлениях ниже критического изобары в двухфазной области (пар – жидкость) претерпевают излом и для чистых веществ в этой области изобары совпадают с изотермами, а для большинства смесей температура кипения не совпадает с температурой конденсации и изобара не совпадает с изотермой.
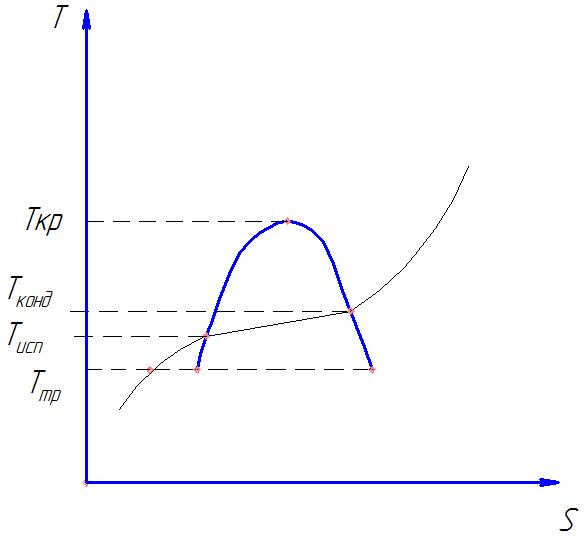
Рисунок 29. T-S диаграмма смеси.
Изохоры в T-S координатах не претерпевают излома в двуфазной области.
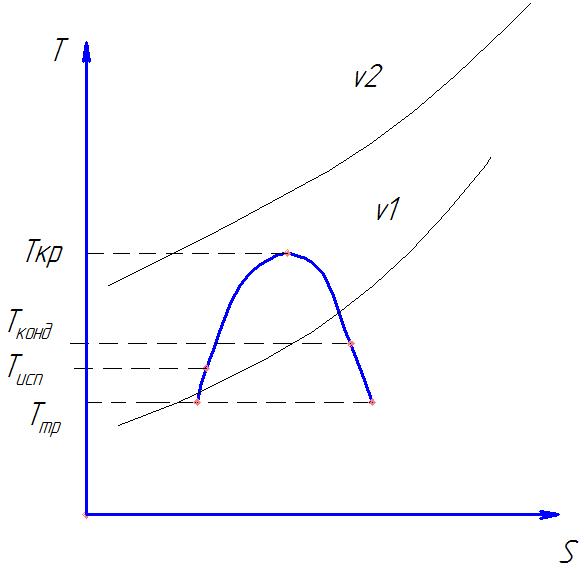
Рисунок 30. Изохоры в T-S диаграмме.
Изохора в T-S диаграммах проходит более круто, нежели изобара в газовой области.
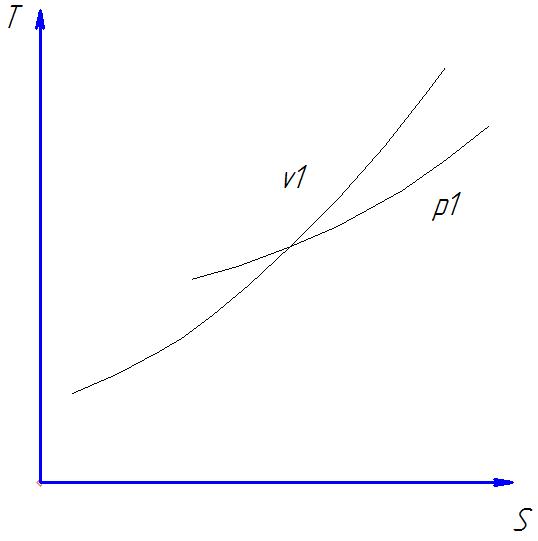
Рисунок 31. Изохора и изобара в газовой области.
Дата добавления: 2016-06-22; просмотров: 3247;











