Общая формула для теплоемкостей однородных систем.
Получим формулу справедливую для любого газа (идеального и реального) и любого процесса.
Для простоты вывода рассмотрим массовую (удельную) теплоемкость то есть 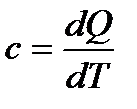 рассматривая термодеформационную сестему.
рассматривая термодеформационную сестему.
Из 1-ого начала термодинамики для термодеформационных системы имеем dQ = dU + p dv.
Как известно, внутренняя энергия является функцией состояния, а дифференциал функции состояния это всегда полный дифференциал.
Любую функцию состояния можно выразить через различные сочетания термодинамических параметров состояния
Пусть U=U(T,v), по правилам математики для полного дифференциала функции нескольких переменных можно записать:
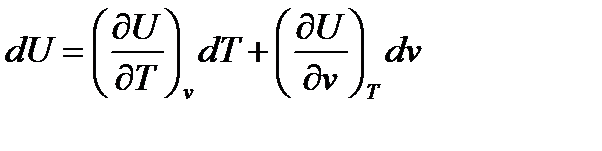 ,
,
таким образом, для определения теплоемкости получаем следующую систему уравнений:
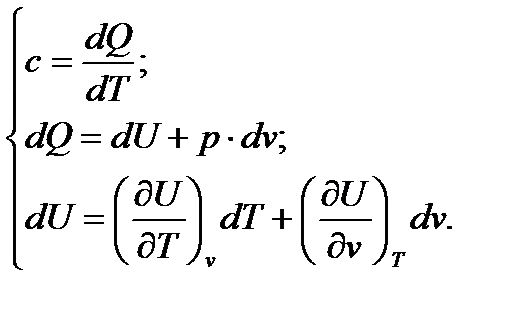
Решая эту сестему методом подстановки, получим:
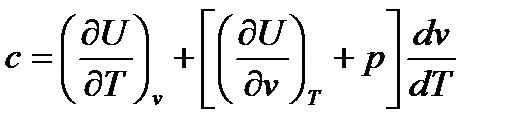 (60)
(60)
Для изохорного процесса (v=const) из формулы 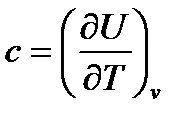 следует
следует
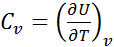 (61)
(61)
Формула (61) для массовой изохорной теплоемкости справедлива как для идеального газа, так и для реального.
Продолжим преобразовывать формулу (60), для чего найдем значение частной производной 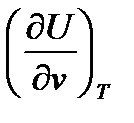 из 1 начала термодинамики для термодеформационной системы.
из 1 начала термодинамики для термодеформационной системы.
dU = TdS – p dv (28)
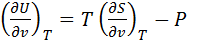 как известно,
как известно, 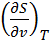 относится к третьему типу деформационных соотношений.
относится к третьему типу деформационных соотношений.
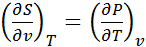 тогда после подстановки получим:
тогда после подстановки получим:
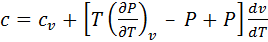
Окончательно:
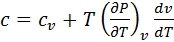 (62)
(62)
Формула (62) называется общей формулой для теплоёмкостей однородных систем (для идеального и реального газа).
Из полученной формулы можно найти значения для теплоёмкости, т.е. для изопроцессов и политропных процессов.
Например, массовая изобарная теплоёмкость любого газа запишется
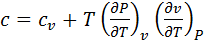 (63)
(63)
Для политропного процесса уравнение приобретает следующий вид:
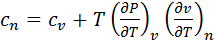
Дата добавления: 2022-05-27; просмотров: 90;










