Работа на деформацию (деформационная работа).
Примеры немеханической работы:
1) работа электрических сил;
2) работа химических реакций.
Единственными формами передачи энергии являются теплота и работа. Работа и теплота проявляются только в процессе передачи энергии.
Внутренняя энергия системы включает в себя кинетическую энергию поступательного и колебательного движения молекул, энергию межмолекулярного взаимодействия и химическую энергию.
Полная энергия E = Eкин + Ep + U.
Eкин – в поступательном и вращательном движении.
Условились рассматривать системы в состоянии, когда Eкин = 0 и Ep = 0, т. е. когда E = U.
В ходе развития науки было установлено, что
dQk = 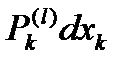
dAk = – dQk = – 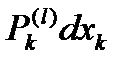
dAдеф = – dQk = 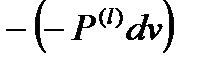 =
= 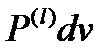
dQ = T dS – при тепловом взаимодействии.
У системы (E = U) все взаимодействия системы с окружающей средой сопровождаются изменением внутренней энергии системы.
dU = 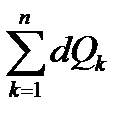 =
= 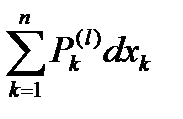 - первое начало термодинамики в обобщённом виде (n – число степеней свободы, т.е. количество взаимодействий разного рода, которые допускает система данного рода).
- первое начало термодинамики в обобщённом виде (n – число степеней свободы, т.е. количество взаимодействий разного рода, которые допускает система данного рода).
Например, у деформационной системы одна степень свободы – деформационная, и первое начало термодинамики для этой системы запишется как:
dU = dQдеф = - P(l)dxk.
У термодеформационной системы две степени свободы, поэтому
dU = dQдеф + dQтепл = dQдеф + dQ
Взаимодействия равновесное и неравновесное. Процессы статические и нестатические.
1) Слабое возмущение
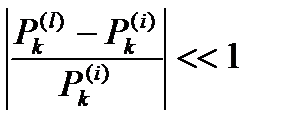
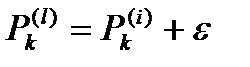 , где ε – возмущение.
, где ε – возмущение.
Первое начало термодинамики:
dU = 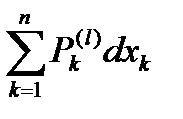 =
= 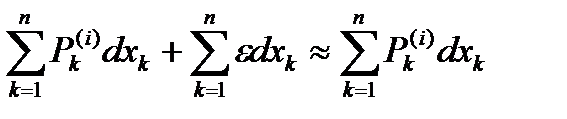 , (
, ( 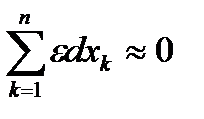 ).
).
О направлении протекания процесса можно судить по знаку ε.
dU = 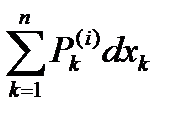 - не содержит информации о протекании процесса.
- не содержит информации о протекании процесса.
Процессы протекают как в прямом, так и в обратном направлении одинаковым образом, т.е. являются обратимыми.
Обратимыми называются процессы, в которых система и окружающая среда проходят через одни и те же состояния как при прямом, так и при обратном протекании процесса.
При слабом возмущении значения термодинамических параметров по всему объёму системы будут одинаковыми, как при равновесии, поэтому взаимодействия при различных возмущениях называются равновесными, а процессы, протекающие при этом, являются квазистатическими. В таких процессах системы как бы проходят через непрерывную цепь состояний равновесия. Время как параметр в силу квазистатичности в уравнениях не фигурирует.
Классическая термодинамика рассматривает равновесные взаимодействия и квазистатические процессы. В дальнейшем i опускается для простоты записи, тогда 1-е начало термодинамики примет вид:
dU = 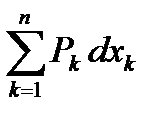 .
.
2) Сильные возмущения.
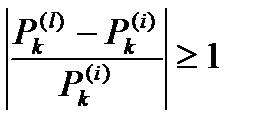 ,
,
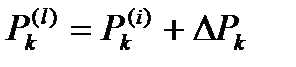 .
.
1-е начало термодинамики:
dU = 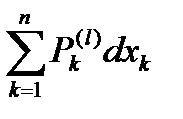 =
= 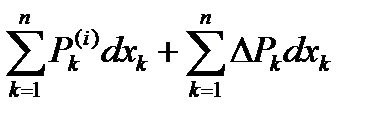 ,
, 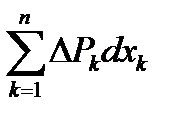 >0.
>0.
Изменение U системы при сильном возмущении всегда больше её значения, получаемого по значениям координаты и потенциала системы.
При сильном возмущении значения термодинамических параметров по объёму системы могут сильно отличаться, такие взаимодействия – неравновесные, процессы – нестатические (время как параметр).
При измерении давления ртутными приборами в мм.рт. столба следует иметь в виду, что показания этих приборов (ртутного манометра, барометра) зависят не только от величины измеряемого давления, но и от температуры ртути в приборе. При положительных температурах плотность ртути меньше, удельный объём выше, следовательно, показания приборов будут выше, чем при 0°C. При температурах ниже 0°C соотношение будет обратным. Показания ртутных приборов для измерения давления всегда приводятся к 0°C.
| Температуры столба ртути | |||||||
| Поправка на 1000 мм.рт.ст. | 0,87 | 1,73 | 2,59 | 3,45 | 4,31 | 3,17 |
Либо для ртутного барометра поправку ещё на ходят по формуле B0 = B(1-0.000172 t), где
B0 – барометрическое давление, приведенное к 0°C;
B – действительное давление при температуре ртути t°C.
Если t>0, то поправку вычитают, если t<0 – прибавляют.
Дата добавления: 2022-05-27; просмотров: 84;










