ГЛАВА 11. ИСПОЛЬЗОВАНИЕ МИКРООРГАНИЗМОВ В ТЕХНОЛОГИИ МЕТАЛЛОВ
Биогеотехнология металлов (биогидрометаллургия) – это наука об извлечении металлов из руд, концентратов, горных пород и растворов под воздействием микроорганизмов или их метаболитов при нормальном давлении и температуре от 5 до 80 – 90 °С.
Наиболее ранние сведения о выщелачивании меди встречаются в записях об античных горных производствах. Около 160 г. до н.э. К. Гален (натуралист и врач) сообщил о методе выщелачивания меди в древних медных рудниках острова Кипр. В 1497 г. в северном районе Венгрии получали медь из растворов, поступающих из руды, методом цементации на железном скрапе. В 1566 г. там же осуществили полный цикл выщелачивания с использованием системы орошения. На территории Германии выщелачивание меди из отвалов практиковалось также в XVI в.
Извлечение меди из растворов, поступающих из шахт медно-колчеданных месторождений, активно практиковали на Урале в середине 40 – 50-х годов XX в. В 1949 г. на Урале было добыто 5 730 т меди из сточных вод.
В 60-е годы в Канаде начали промышленное подземное выщелачивание урана. В настоящее время разработкой и освоением биогидрометаллургических технологий занимается более 100 фирм и организаций в 25 странах мира.
Открытие микроорганизмов, важных для биогеотехнологии металлов.Исследования русского ученого С. Н. Виноградского в конце XIX в. в области литотрофии стимулировали изучение роли микроорганизмов в круговороте серы и других элементов в природе. В 1902 г. крупнейший голландский микробиолог М. Бейеринк выделил новый автотрофный микроорганизм Thiobacillus thioparus, окисляющий серу и ряд ее восстановленных соединений при высоких значениях рН среды.
В 1921 – 1922 гг. В. Рудольф и А. Хельброннер впервые провели исследования на рудниках, которые показали, что некоторые неидентифицированные сероокисляющие микроорганизмы способны окислять пирит и сульфиды цинка.
В это же время С. А. Ваксман и Дж. С. Джоффи выделили автотрофный ацидофильный микроорганизм Thiobacillus thiooxidans (ныне Acidithiobacillus thiooxidans), окисляющий серу и ряд ее восстановленных соединений до серной кислоты. Предположения о возможной роли бактерий в образовании серной кислоты в шахтных водах в угольных месторождениях впервые были высказаны Л. Карпентором и Дж. Херндоном в 1933 г. В настоящее время известен ряд хемолитотрофных бактерий, важных для биогидрометаллургии. В практике добычи металлов особое внимание уделяется бактериям A. ferrooxidans, A. thiooxidans, A. caldus и Leptospirillum ferrooxidans, которые окисляют Fe2+, S2-, S° и сульфидные минералы.
Определенный интерес представляют ацидофильные гетеротрофные бактерии Acidiphilium cryptum, Ac. angustum, Ac. rubrum и Ac. facilis. Они способствуют выщелачиванию металлов хемолитотрофными бактериями.
Физико-химические основы выщелачивания металлов из руд. Бактериально-химическое выщелачивание – извлечение химических элементов из минералов, руд, концентратов и горных пород посредством их окисления и/или растворения микроорганизмами или продуктами их метаболизма. Основными физико-химическими факторами при кучном, подземном и чановом выщелачивании меди, цинка, никеля, урана являются рН, Eh, температура, наличие кислорода, ионов сернокислого оксидного железа (Fe3+) и т.д. От совокупности благоприятных факторов (рН 1,2 – 2,0; Eh 700 мВ, и др.) зависит активность сообщества бактерий, окисляющих сернокислое закисное железо (Fe2+), серу (S°, S2+) и сульфидные минералы.
Химические реакции, происходящие в процессе бактериального окисления:
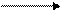 2FeSО + 0,5О2 + Н2SО4 бактерии Fe2(SО4)3 +Н2О
2FeSО + 0,5О2 + Н2SО4 бактерии Fe2(SО4)3 +Н2О
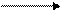 Fe2(SО4)3 + МеS бактерии МеSO4 + 2Fe SO4 + S°
Fe2(SО4)3 + МеS бактерии МеSO4 + 2Fe SO4 + S°
Образующиеся продукты этой реакции (Fe2+, S° и др.) окисляются бактериями до конечных продуктов:
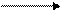 Fe2+ + О2 + 4Н+ бактерии 4 Fe3+ + 2Н2О
Fe2+ + О2 + 4Н+ бактерии 4 Fe3+ + 2Н2О
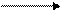 S°+ 4Н2О бактерии SO42- + 8Н+
S°+ 4Н2О бактерии SO42- + 8Н+
Продукты этой и подобных ей реакций окисляются бактериями до Fe3+ или H2SO4. Таким образом, эти бактериально-химические процессы едины и создают низкую величину рН, высокий окислительно-восстановительный потенциал среды, необходимую концентрацию Fe3+ и обеспечивают активные процессы выщелаивания металлов из руд. Следует отметить особые окислительные свойства Fe3+ в кислой среде в отношении вторичных сульфидных минералов меди, цинка и некоторых минералов никеля (окисное железо является сильным окислителем и растворителем сульфидов).
Механизм бактериального окисления Fe2+, S2- /S° и сульфидных минералов.Хемолитотрофные бактерии окисляют неорганические субстраты и получают энергию в соответствии с хемиосмотической теорией Митчела, а также по электрохимическим (коррозионным) механизмам (рис 11.1).
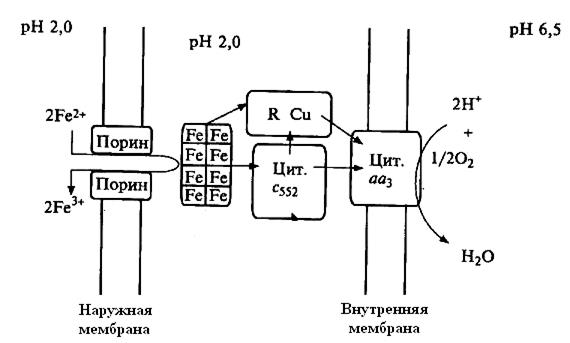
Рис.11.1. Модель функционирования железоокисляющей системы A. ferrooxidans и транспорта электронов
Бактериальное окисление субстратов включает следующие стадии:
· взаимодействие поверхностных структур бактерий с окисляемым субстратом (сорбция, адгезия);
· изменение физико-химических свойств окисляемых субстратов и их транспорт в клеточную стенку;
· окисление субстратов в поверхностных структурах клеток;
· транспорт электронов и протонов; образование мембранного потенциала;
· синтез АТФ и образование воды на внутренней поверхности ЦПМ.
Кучное и подземное выщелачивание меди.Бактериально-химическое выщелачивание цветных металлов проводят из отвалов бедной руды (кучное) и из рудного тела в месте залегания (подземное). Более распространено кучное выщелачивание меди. Технологические схемы приведены на рис.11.2.
Орошение дробленой руды в отвале или в рудном теле осуществляется водными растворами H2SO4, содержащими Fe3+, O2 и бактерии. При нормальной и пониженной температуре процессы окисления сульфидных минералов при рН 1,0 – 2,0 катализируют хемолитотрофные бактерии A. ferrooxidans, A. thiooxidans, L. ferrooxidans и F. acidiphilum.
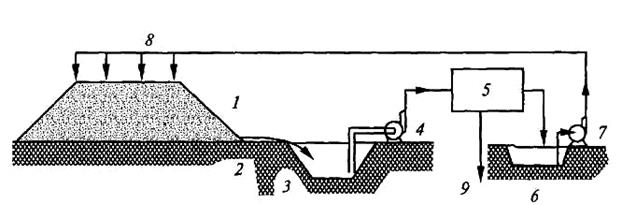
Рис.11.2 Процесс кучного выщелачивания:
1 – куча; 2 – поверхность почвы; 3 – прудок для сбора продуктивных растворов; 4– насос; 5 – желоба для цементации; 6 – прудок для отработанного раствора; 7– насос; 8 – система орошения отвала; 9 – металл
В зонах разогрева руды в результате экзотремических окислительных процессов при температуре 55 °С широко распространены умеренно-термофильные бактерии p. Sulfobacillus и A. caldus. При температуре выше 50 °С в окислительных процессах участвуют термофильные бактерии p. Acidianus и Metallosphaera.
Растворы подаются через скважины при подземном выщелачивании металлов или путем разбрызгивания, или создания прудков на поверхности отвалов при кучном выщелачивании металлов. В руде в присутствии окислителей (бактерии, О2, Fe3+) и при оптимальных условиях орошения руды сульфидные минералы окисляются, а цветные металлы в кислой среде переходят в растворимое состояние.
Металлы из растворов извлекают:
· цементацией. Цементацияв цветной металлургии, гидрометаллургический процесс, основанный на вытеснении более электроположительных металлов из растворов их соединений менее электроположительными металлами, находящимися в твёрдом состоянии. Разность потенциалов позволяет осуществлять реакцию, например:
Cu2+раствор + Znмeталл Zn2+раствор + Cuмeталл..
Чем больше разность потенциалов, тем меньше остаточное содержание в растворе осаждаемого металла
· концентрируют методом экстракции и затем извлекают электролизом.
После извлечения ценных элементов растворы опять поступают на орошение руды (схема замкнутая).
Переработка сложных руд и концентратов в реакторах (чановое выщелачивание).Процесс извлечения металлов из концентратов с использованием бактерий и осуществляемый в специальных аппаратах называется чановым. Он проводится в аппаратах, обеспечивающих перемешивание, аэрацию и регуляцию температурного режима в пульпе и предназначен для использования в комбинированных технологических схемах, включающих операции – гравитацию или флотацию, бактериальное окисление сульфидных минералов и переработку твердых остатков и растворов.
Бактериально-химическое окисление концентратов проводят в непрерывных условиях в серии последовательно соединенных реакторов с перемешиванием и аэрацией при 30 °С для мезофилов, от 45 – 40 °С для умеренных термофилов и 60 – 70 °С для облигатных термофилов.
Концентрат измельчают до размеров частиц 40 – 70 мкм, помещают в контактный чан и создают плотность пульпы от 20 до 40 % твердого вещества. После постепенного заполнения всех реакторов система работает в непрерывном проточном режиме. Схема переработки концентратов может быть замкнутой. Оборотные растворы после частичной или полной регенерации используют для выщелачивания или сбрасываются в хранилище.
Влияние технологических условий на процесс выщелачивания металлов. Размеры частиц и плотность пульпы. Размеры частиц руды или концентрата определяют площадь их поверхности, от которой зависит адгезия бактерий и скорость окислительных процессов. Наибольшая скорость окисления сульфидов в пульпе A. ferrooxidans при чановом выщелачивании наблюдается при размерах частиц от 2 – 3 до 40 мкм, однако в промышленных условиях обычно используются частицы флотационного концентрата размером 74 мкм. Частицы меньше 0,2 мкм повреждают структуру клетки, и FeS2 не окислялся.
При кучном и подземном выщелачивании металлов тонкое измельчение руды невозможно, так как с крупностью материала в тесной связи находится водопроницаемость и аэрация руды.
Плотность пульпы (соотношение твердого вещества к жидкому) при чановом выщелачивании зависит от типа концентрата или промпродукта. Переработку цинксодержащих продуктов мезофильными бактериями можно проводить при плотности пульпы 16 – 40 %, медных концентратов – до 30 %. Вскрытие золота в золото-мышьяковых концентратах эффективно проводится при плотности пульпы до 20 %.
Влияние химических элементов.Токсичность металлов для бактерий зависит от физиологического состояния бактерий, химического состояния металлов и степени их взаимодействия в среде. К наиболее токсичным катионам относят Cd, Ag, Hg и U. Анионы Se, Те, As и Mo более токсичны, чем большинство катионов металлов. Калий снижал токсичность серебра. Токсичность металлов снижается в присутствии комплексующих агентов. Например, добавление цистеина предотвращает ингибирование A. ferrooxidans Ag+. В целом A. ferrooxidans высокоустойчив к отдельным металлам: Сu – 50 г/л; Zn – 70 мг/л; Со – 30 г/л; As – 6–10 г/л; Мо – 200 мг/л; А1 – 20 г/л; Ni – 72 г/л; Ag – 1,0–10 мг/л; Cd – 120 мг/л; U3Og – 12 г/л. Резистентность других хемолитотрофов к металлам изучена недостаточно.
Источники питания.Важнейшими элементами для жизнедеятельности хемолитотрофных бактерий в биогидрометаллургии являются азот и фосфор. Как при чановом, так и при кучном и подземном выщелачивании металлов другие необходимые для бактерий элементы поступают из руды или концентратов. Азот и фосфор обычно либо отсутствуют, либо присутствуют в низких количествах, причем они постоянно выводятся из среды, вступая в реакции с другими элементами с образованием фосфатов железа и т.д., и поэтому требуется их постоянное добавление. С солями азота и фосфора поступает и калий. При замене в традиционных средах солей азота, фосфора и калия на аммофос снижается их стоимость в 10 раз без изменения.
Влияние микробиологических факторов.Штамм А. ferrooxidans является устойчивым в технологических условиях, который адаптирован к комплексу факторов (рН, ионы металлов, тип минерала и т. д.), а не к какому-либо одному из них. Этот тезис оказался справедливым и для других хемолитотрофов. В рудах и концентратах обычно присутствуют сообщества хемолитотрофных и некоторых ацидофильных гетеротрофных бактерий. В технологических условиях в окислении Fe2+, S2-/S° и сульфидных минералов принимает участие сообщество бактерий. Хотя, как уже отмечалось выше, в зависимости от условий существует лидер или несколько штаммов-лидеров.
Влияние температуры.При снижении температуры до 15 оС средняя удельная скорость роста различных штаммов A. ferrooxidans уменьшалась в 2,8 – 4 раза, а средняя скорость окисления Fe 2+ – в 2,3 – 3 раза. При снижении температуры до 8 °С эти величины уменьшались в 6,1 – 13,3 и 4,5 – 8,0 раз соответственно. Роль термофильных бактерий в биогидрометаллургии изучена еще слабо. В отвалах руд, богатых сульфидными минералами, при их окислении происходит разогрев вплоть до самовозгорания. Из этих руд выделяются умеренно- и экстремально-термофильные бактерии.
При спонтанном разогреве руд в отвалах можно ожидать положительного эффекта от деятельности термофильных бактерий.
Экологические аспекты выщелачивания металлов. При рассмотрении экологических проблем биогидрометаллургии следует прежде всего иметь в виду технологические особенности этого способа добычи металлов. Все технологические схемы замкнутые, поэтому в значительной мере исключают выброс растворов в биосферу. Исключаются выбросы вредных газов в атмосферу. Подземное выщелачивание исключает необходимость отвода больших участков земли под горные предприятия, при этом сохраняется ландшафт. В кучном выщелачивании утилизируют металлы старых отвалов и вновь отсыпаемых, тем не менее каждый тип выщелачивания имеет свои отходы, опасные для окружающей среды. Общим для всех гидрометаллургических предприятий отходом являются растворы, содержащие тяжелые металлы. Обычно растворы, которые выводятся из оборота, нейтрализуются и сбрасываются в специальные прудки, а затем, после естественной доочистки, в реки. При такой операции они в значительной мере очищаются от металлов. Однако и эти воды нуждаются в полной очистке от металлов. Микробиологические способы сорбции и осаждения металлов, по-видимому, являются наиболее перспективными для решения этой проблемы. Некоторые из них испытаны в промышленных условиях.
Не менее актуальна также проблема обезвреживания твердых отходов биогидрометаллургических производств, например соединений мышьяка (арсенат железа или кальция), цианидов, роданидов и т. д., однако она окончательно еще не решена.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ:
1. Что такое биогеотехнология металлов.
2. Характеристика микроорганизмов, важных для биогеотехнологии металлов.
3. Физико-химические основы выщелачивания металлов из руд. .
4. Химические реакции, происходящие в процессе бактериального окисления:
5. Механизм бактериального окисления Fe2+, S2- /S° и сульфидных минералов.
6. Стадии бактериального окисления субстратов?
7. Кучное и подземное выщелачивание меди.
8. Что такое цементация в цветной металлургии.
9. Влияние технологических условий на процесс выщелачивания металлов.
10. Экологические аспекты выщелачивания металлов.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Беккер, М.Е.Введение в биотехнологию/М.Е. Беккер. – М.: Пищевая промышленность, 1978. – 231 с.
2. Березин, И.В. Инженерная энзимология/ И.В. Березин, А.А.Клесов, В.К.Швядас. – М.: Высшая школа, 1987. – 144 с.
3. Березин, И.В. Иммобилизованные ферменты/И.В. Березин, Н.Л.Клячко, А.В.Левашев и др. – М.: Высшая школа, 1987. – 160 с.
4. Богданова, О.Ю. Основные питательные среды для культивирования микроорганизмов. Приготовление питательных сред/О.Ю. Богданова, Е.В. Макаревич// Методические указания к выполнению лабораторной работы. – Мурманск МГТУ, 2002. – 38 с.
5. Быков, В.А. Микробиологическое производство биологически активных веществ и препаратов/В.А. Быков, И.А. Крылов, М.Н. Манаков. – М.: Высшая школа, 1987. – 142 с.
6. Быков, В.А. Производство белковых веществ/В.А. Быков, М.Н. Манаков, В.И. Панфилов. – М.: Высшая школа, 1987. – 142 с.
7. Вербина, Н.М. Микробиология пищевых производств /Н.М. Вербина, Ю.В. Каптерова. – М.: Агропромиздат, 1988. – 288 с.
8. Голубовская, Э.К. Биологические основы очистки воды/Э.К. Голубовская. – М.: Высшая школа, 1978. – 270 с.
9. Гусев, М.В. Микробиология: Учебник для студ. биол.специальностей. /М.В. Гусев, Л.А. Минеева. – 4-е изд., стре. – М.: Изд. центр «Академия», 2003. – 464 с.
10. Жвирблянская, А.Ю. Микробиология в пищевой промышленности/А.Ю. Жвирблянская, О.А. Бакушинская. – М.: Пищевая промышленность, 1975. – 501 с.
11. Егоров, Н.С. Основы учения об антибиотиках/Н.С. Егоров. – М.: Высшая школа, 1986. – 448 с.
12. Егорова, Т. А. Основы биотехнологии/ Т. А. Егорова, С.М. Клунова, Е.А. Живухина// Учебное пособие. – М.: Академия, 2003. – 208 с.
13. Елдышев, Ю.Н. Современная биотехнология/Ю.Н. Елдышев. – М:Тайдекс Ко, 2004.
14. Литвинова, М.Ю. Ведение в биотехнологию/ М.Ю. Литвинова// Методические указания к лабораторным работам по дисциплине «Введение в биотехнологию». – Мурманск МГТУ, 2006.
15. Макаревич, Е.В. Микроорганизмы заквасок кисломолочных продуктов/Е.В. Макаревич, М.Ю. Литвинова// Методические указания. – Мурманск МГТУ, 2008.
16. Макаревич, Е.В.Гидромикробиологический анализ сточных вод/Е.В. Макаревич, М.Ю. Литвинова//Методические указания. – Мурманск МГТУ, 2008. – 32 с.
17. Макаревич, Е.В. Микробиологическая деструкция ксенобиотиков/Е.В. Макаревич// Методические указания. – Мурманск МГТУ, 2008.
18. Мюнх, Г.Д. Микробиология продуктов животного происхождения/Г.Д. Мюнх, Х.Заупе, М. Шрайтер. – М.: Агропромиздат, 1985. – 592 с.
19. Нетрусов, А.И. Экология микроорганизмов/А.И. Нетрусов. – М.: Академия, 2004. –267 с.
20. Определитель бактерий Берджи /Под ред. Дж. Хоулта, Н. Крига, П. Смита и др.//В 2 т.: Пер. с англ. – М.: Мир,1997.
21. Промышленная микробиология/Под ред. Егорова Н.С. – М.: Высшая школа, 1989.
22.Хиггинс, И. Биотехнология. Принципы и применение /И. Хиггинс, Д. Бест, Дж. Джонс. – М.: Мир, 1988. – 480 с.
Дата добавления: 2016-10-26; просмотров: 4600;











