Число соударений между молекулами и средняя длина свободного пробега молекул
Идеальный газ во внешнем поле
Если идеальный газ находится в силовом поле, то давление будет меняться от точки к точке, так как на молекулы газа действуют внешние силы. Рассмотрим наиболее простой случай, когда силы поля направлены в одну сторону, допустим вдоль оси Х.
Возьмем две площадки единичной площади, расположенных на расстоянии dx; на эти площадки будет оказываться давление, которое равно соответственно Р и Р + dР (рис.9.1).
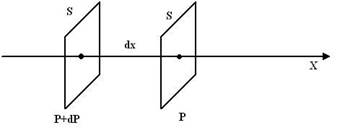
Рис.9.1
Разность давлений dP равняется суммарной силе, действующей на частицы в объеме Sdx (S =1 м³), т.е.
dP = nFdx (9.1)
где, n – объемная плотность молекул;
F – сила, действующая на одну молекулу с координатой х.
Сила F связана с потенциальной энергией Еп
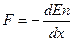 (9.2)
(9.2)
После подстановки (9.2) в (9.1) получим
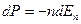 (9.3)
(9.3)
Для идеального газа Р = nkТ. Предполагая, что Τ = соnst
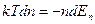 (9.4)
(9.4)
Проинтегрировав обе части равенства (9.4) получаем
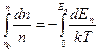 (9.5)
(9.5)
учитывая, что n0 – объемная плотность молекул в точке где Еn = 0, получим
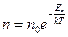 (9.6)
(9.6)
Полученная формула устанавливает связь изменения объемной плотности газа с потенциальной энергией его молекул и называется формулой Больцмана.
Если (9.6) умножить на kТ, получим уравнение для расчета давления
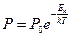 (9.7)
(9.7)
В поле тяжести Земли на высоте h молекула массой m0 обладает потенциальной энергией Еп= m0gh
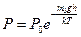 (9.8)
(9.8)
Уравнение (9.8) называется барометрической формулой.
Подставив вместо 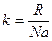 и m0Na = M, получим для барометрической формулы:
и m0Na = M, получим для барометрической формулы:
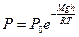 (9.9)
(9.9)
График зависимости давления газаот высоты Р( h) представлен на рис.9.2.
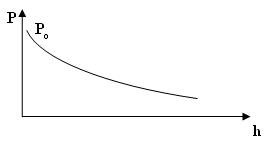
Рис.9.2
Чем больше молекулярная масса, тем быстрее давление убывает с высотой. Поэтому с увеличением высоты атмосфера обогащается легкими парами.
Число соударений между молекулами и средняя длина свободного пробега молекул
В результате хаотического движения молекулы газа непрерывно сталкиваются друг с другом. Вычислим число соударений между молекулами для идеального газа. Для этого будем рассматривать молекулы, как упругие шарики диаметром d, которые движутся со средней скоростью <u>. За единицу времени молекула на своем пути заденет другие молекулы, которые находятся в цилиндре диаметром 2d т.е. в объеме πd2<u> (рис.9.3).
Соответственно количество столкновений Z равно
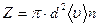 (9.10)
(9.10)
где, n – количество молекул в единице объема, концентрация молекул.
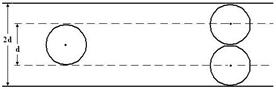
Рис.9.3
Если учесть, что все молекулы движутся, то число соударений увеличивается в 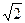
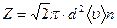 (9.11)
(9.11)
Надо отметить, что молекулы при каждом столкновении изменяет свое направление и движется не в таком прямом цилиндре, а в системе соединенных под разными углами цилиндров.
Среднее расстояние, проходимое молекулой между двумя последовательными соударениями называется средней длиной свободного пробега < λ >
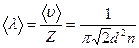 (9.12)
(9.12)
При T = const концентрация молекул n пропорциональна давлению Р. Следовательно
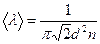 (9.13)
(9.13)
Минимальное расстояние, на которое сближаются при столкновении центры двух молекул, называется эффективным диаметром (рис.9.4).
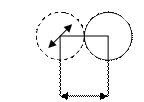
d
Рис.9.4
Эффективный диаметр зависит от скорости сталкивающихся молекул, т.е. от температуры газа.
Дата добавления: 2019-12-09; просмотров: 312;










