Пробоотбор и пробоподготовка
Для проведения анализа, как правило, берут так называемую среднюю пробу. Это небольшая часть анализируемого объекта, средний состав и свойства которой должны быть идентичны во всех отношениях среднему составу и свойствам исследуемого объекта. Различают генеральную, лабораторную и анализируемую пробы. Генеральная проба отбирается непосредственно из анализируемого объекта. Она достаточно большая – обычно 1-50 кг. Из генеральной пробы путем ее сокращения отбирают лабораторную пробу (обычно от 25 г до 1 кг). Одну часть лабораторной пробы используют для предварительных исследований, другую – непосредственно для анализа (анализируемая проба). Для анализируемой пробы проводят несколько определений компонента: из отдельных навесок 10-1000 мг (если анализируемый объект – твердое вещество) или аликвот (если анализируемый объект – жидкость или газ).
Содержание определяемого компонента в анализируемой пробе должно отражать среднее содержание этого компонента во всем исследуемом объекте, т.е. анализируемая проба должна быть представительной.
Способы отбора пробы и ее количество прежде всего определяются физическими и химическими свойствами анализируемого объекта. При отборе пробы нужно учитывать:
- агрегатное состояние анализируемого объекта (способы отбора пробы различны для газов, жидкостей и твердых веществ);
- неоднородность анализируемого материала (чем однороднее вещество, тем проще отобрать пробу);
- размер частиц, с которых начинается неоднородность;
- требуемую точность оценки содержания компонента во всей массе анализируемого объекта;
- возможность изменения состава объекта и содержания определяемого компонента во времени (переменный состав воды в реке, колебания состава дымовых газов промышленного предприятия).
Отбор пробы газов упрощен высокой степенью их однородности (неоднородность наблюдается на молекулярном уровне), поэтому генеральная проба может быть относительно небольшой. Пробу газа отбирают, измеряя его объем при помощи вакуумной мерной колбы или бюретки с соответствующей запорной жидкостью, иногда конденсируют газ в ловушках разного типа при низких температурах.
По-разному отбирают пробу газа из замкнутой емкости и из потока. В замкнутой емкости (цех, рабочая комната) пробы отбирают в разных точках и в зависимости от задачи либо смешивают, либо анализируют отдельно. При отборе пробы газа из потока обычно используют метод продольных струй (если состав газа вдоль потока не меняется) и метод поперечных сечений (если состав газа вдоль потока меняется).
Метод продольных струй заключается в делении потока на струи и проведении пробоотбора в струях через одну (рис.4.1, а). Метод поперечных сечений заключается в отборе пробы на определенных расстояниях, через специальные отверстия в трубах вдоль потока газа (рис. 4.1, б).
Отбор пробы жидкостей отличается для гомогенных и гетерогенных жидкостей. Отбор пробы гомогенных жидкостей, как и газов, относительно прост. Пробу гомогенной жидкости отбирают после предварительного перемешивания с помощью пипеток, бюреток и мерных колб. Если жидкость (например, из-за большого объема) нельзя перемешать, то отбор пробы проводят на разной глубине и в разных местах (рис.4.2, а). Для отбора проб на разной глубине используют батометры различных конструкций (цилиндрический сосуд, закрывающийся сверху и снизу крышками, после погружения его на заданную глубину). Отбор гомогенных жидкостей из потока проводят в определенные интервалы времени и в разных местах.
Например, при анализе сточных вод необходимо согласовывать время и место отбора пробы с технологическим процессом, учитывать время прохождения сточной воды через очистные сооружения, анализировать не только воду самих стоков, но и воду водоема ниже и выше впадения в него стока, что покажет, насколько водоем загрязняется сточными водами.
Пробы гетерогенных жидкостей отбирают не только по объему, но и по массе. Чтобы отобрать пробу, в одних случаях жидкость гомогенизируют, в других, наоборот, добиваются полного ее расслоения. Гомогенизацию проводят, изменяя температуру, перемешивая жидкость или подвергая ее вибрации. Если гомогенизировать жидкость невозможно, то ее расслаивают и отбирают пробу каждой фазы, используя при этом специальные пробоотборники с большим числом забирающих камер (рис. 4.2, б).
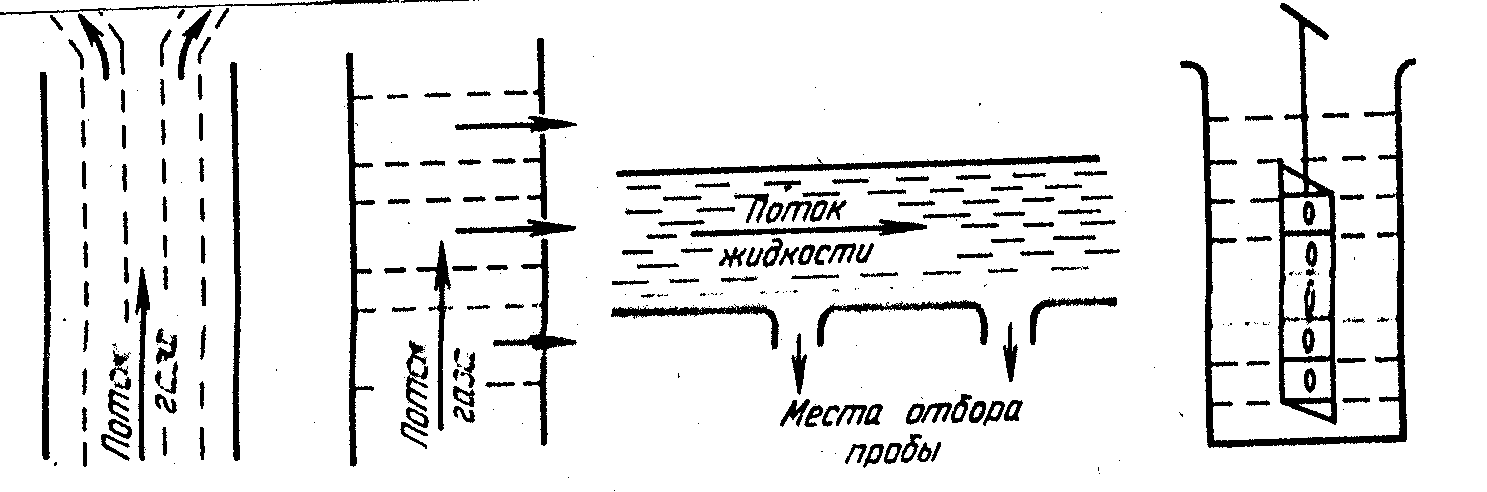
| Рис. 3.1. Отбор пробы газа в потоке: а - метод продольных струй; б - метод поперечных струй (стрелками показаны места отбора проб) | Рис. 3.2. Отбор пробы: а - жидкости в потоке; б - гетерогенной жидкости пробоотборником с изолированными ячейками |
Отбор пробы твердых веществ определяется степенью неоднородности анализируемого объекта, размером частиц, с которых начинается неоднородность, и требованиями к точности анализа. С учетом этих факторов определяется оптимальная масса представительной пробы. Для ее определения чаще всего используют приближенную формулу Ричердса – Чеччота:
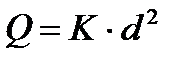 ,
,
где Q – масса пробы, обеспечивающая ее представительность, кг; d – наибольший диаметр неоднородных частиц, мм; К – эмпирический коэффициент пропорциональности, характеризующий степень неоднородности распределения определяемого компонента в материале, меняющийся в пределах 0,02¸1.
Отбор пробы твердых веществ тем труднее, чем неоднороднее анализируемый объект, поскольку в пробе должны быть представлены части разного размера, полно отражающие состав образца. При отборе пробы массу исследуемого объекта перемешивают и пробу отбирают в разных местах емкости и на разной глубине, используя при этом специальные щупы – пробоотборники.
После отбора генеральной пробы твердого вещества осуществляют процесс гомогенизации, включающий операции измельчения и просеивания (разделение крупных и мелких частиц, для того, чтобы избежать потерь в виде пыли, так как мелкие частицы измельчаются быстрее). После получения однородной пробы проводят операцию усреднения, включающую операции перемешивания и деления.
Подготовка пробы к анализу включает в себя три основные стадии:
- высушивание;
- разложение (чаще с переведением пробы в раствор);
- устранение влияния мешающих компонентов.
В зависимости от объекта анализа исследователь оценивает необходимость включения указанных стадий в схему анализа и устанавливает условия проведения каждой из них.
Высушивание образцов необходимо в том случае, если объект анализа содержит химически несвязанную (адсорбированную, окклюдированную) или химически связанную (стехиометрическую, кристаллизационную) воду. Для правильного установления состава образца и получения воспроизводимых результатов анализа необходимо удалить влагу из образца, высушить его до постоянной массы или определить содержание воды.
Образцы высушивают на воздухе, в сушильных шкафах, в эксикаторах над влагопоглощающими веществами (хлорид кальция, фосфорный ангидрид, перхлорат магния и др.). Если отсутствуют определенные указания в методике, то обычно образцы сушат в сушильных шкафах при 110 ºС в течение 1-2 часов.
Количество воды, содержащееся в пробе, определяют тогда, когда не удается полностью удалить воду из пробы или высушить ее до постоянной массы. Обычно количество воды в образце определяют с помощью поглотителя по увеличению массы предварительно взвешенного поглотителя.
Разложение образцов и переведение пробы в раствор требуется для измерения аналитического сигнала в большинстве используемых методах анализа (исключение составляют некоторые спектроскопические или ядерно-физические методы). Выбор способа разложения пробы и переведения в раствор определяется:
- природой матрицы (неорганической или органической);
- химическим составом определяемых компонентов;
- целями и методом последующего анализа;
- наличием и природой мешающих определению компонентов.
Способы разложения делят на сухие и мокрые. К сухим относят термическое разложение, сплавление и спекание с различными веществами. К мокрым – растворение пробы в различных растворителях, преимущественно в кислотах и их смесях.
Обычно сухой способ используют тогда, когда мокрый способ не дает удовлетворительных результатов. Сухие способы менее предпочтительны, чем мокрые, поскольку они связаны с высокими температурами, а это приводит к погрешностям анализа вследствие
- потери летучих веществ;
- разрушения материала посуды и последующего загрязнения образца;
- избытка плавня и разрушающихся агентов.
Термическим разложением называют разложение пробы при нагревании, сопровождающееся образованием одного или нескольких компонентов газообразной фазы. Образец нагревают в тигле или в лодочке в печи, наносят образец на металлическую проволоку или помещают в стеклянную трубку с инертным газом и нагревают до нужной температуры (обычно не менее 500-600 ºС). Иногда используют термическое разложение при облучении лазером, потоком электронов и др. Чаще всего термическое разложение используют при анализе органических веществ.
Сплавление чаще используют при анализе неорганических веществ. При сплавлении тонко измельченный образец перемешивают с 8-10 кратным избытком реагента (плавня) и нагревают (300-1000 ºС) до получения прозрачного плавня. Время плавления определяется природой разлагаемой пробы и варьируется от нескольких минут до нескольких часов. После охлаждения застывшую массу растворяют в воде или кислотах.
При сплавлении используют плавни: щелочные (карбонаты, гидрооксиды щелочных металлов), кислые (гидросульфат калия, оксид бора), окислительные (щелочные плавни с окислителем пероксидом, хлоратом, нитратом щелочных металлов).
Спекание – это взаимодействие веществ при повышенных температурах в твердой фазе. В отдельных случаях оно позволяет провести разложение пробы быстрее, при более низких температурах и меньшем избытке (по сравнению со сплавлением) реагентов. Спекание проводят обычно со смесью щелочных металлов и оксидов магния, кальция, цинка. Наиболее эффективно его можно использовать при разложении проб силикатов, сульфидов, оксидов металлов.
Мокрые способы позволяют действовать на образец в более мягких условиях и с большой скоростью проводить его разрушение. Лучший растворитель – вода. Многие неорганические соли и некоторые органические соединения (спирты, аминокислоты, соли органических кислот и др.) легко растворяются в воде.
Для растворения часто применяют различные кислоты и их смеси при нагревании. В отдельных случаях используют смесь воды и органического растворителя. Для растворения органических соединений применяют органические растворители (спирты, хлорпроизводные углеводородов, кетоны, диметилформамид, циклогексанон и др.).
После отбора и разложения пробы устраняют влияние мешающих компонентов. Одним из способов устранения мешающих компонентов является маскирование – перевод мешающих компонентов в такую форму, которая уже не оказывает мешающего влияния. Маскирование – это торможение или полное подавление химических реакций мешающих компонентов, не связанное с образованием новой фазы.
Обычно маскирование мешающих компонентов связано с образованием ими более устойчивых соединений (комплексных, малорастворимых) со специальными веществами – маскирователями. Например, замаскировать ион железа (III) и устранить его мешающее влияние при определении иона кобальта в присутствии тиоцианата аммония, с которым оба иона образуют устойчивые комплексы, можно добавлением фторид иона, который связывает железо в бесцветный комплекс FeF63- , более устойчивый, чем комплекс железа с тиоцианатом.
Часто используют такие маскирователи, как комплексоны, полифосфаты, глицерин, тиомочевина, галогенид-, цианид-, тиосульфат- ионы. Маскирование не всегда удается осуществить, особенно при анализе многокомпонентных смесей. В этом случае используют разделение веществ или концентрирование.
Дата добавления: 2022-05-27; просмотров: 299;










