Насыщенный и ненасыщенный пар, их свойства.
Динамическое равновесие пара и жидкости – состояние, при котором число молекул, вылетающих из жидкости в единицу времени, равно числу молекул, возвращающихся в нее за то же время.
Пар, находящийся в динамическом равновесии со своей жидкостью, называют насыщенным.
Свойства насыщенного пара:
- насыщенный пар имеет при данной температуре наибольшее число молекул в единице объема (наибольшую плотность) и оказывает наибольшее давление.
- давление насыщенного пара при неизменной температуре – величина постоянная (закон Гей-Люссака неприменим, т.к. объем не зависит от температуры);
- давление насыщенного пара не зависит от его объема;
- концентрация молекул насыщенного пара в закрытом объеме с жидкостью неизменна при данной температуре, независимо от занимаемого объема;
- давление насыщенного пара возрастает с повышением температуры;
- законы Бойля-Мариотта и Шарля к насыщенному пару неприменимы вследствие изменения массы газа при изобарическом и изотермическом процессах.
Пар, не находящийся в динамическом равновесии со своей жидкостью, называют ненасыщенным.
Ненасыщенным будет пар над поверхностью жидкости, если испарение преобладает над конденсацией. Плотность ненасыщенного пара меньше, чем плотность насыщенного пара.
 Состояние насыщенного пара приближенно описывается уравнением состояния идеального газа, его давление определяется формулой
Состояние насыщенного пара приближенно описывается уравнением состояния идеального газа, его давление определяется формулой 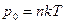 .
.
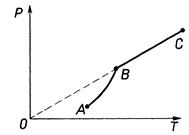
К участку АВ данный закон неприменим, т.к. в закрытом сосуде возрастает концентрация молекул пара, меняется масса пара.
Когда вся жидкость испарится, пар при дальнейшем нагревании перестает быть насыщенным и его давление при постоянном объеме будет возрастать прямо пропоционально абсолютной температуре – участок ВС.
Критическая температура – это температура, при которой исчезают различия в физических свойствах между жидкостью и ее насыщенным  паром.
паром.
При температуре выше критической ни при каких давлениях газ нельзя обратить в жидкость.
Дата добавления: 2020-02-05; просмотров: 322;










