Потенциал взаимодействия молекул.
Для изучения связи между макроскопическими параметрами системы (температуры, давления и т.д.) и ее микроскопическими параметрами (размер, масса и скорость молекул или атомов, силы взаимодействия между ними) необходимо привлекать модельные представления. В зависимости от сложности модели мы можем описывать свойства макроскопических тел в том или ином приближении.
В курсе общей физики для описания свойств идеального газа молекулы его представляли упругими шарами бесконечно малых размеров; столкновение шаров-молекул происходит за бесконечно малый промежуток времени. Поэтому большую часть времени молекулы проводят в свободном полете, не испытывая взаимодействия между собой.
В модели реального газа Ван-дер-Ваальса, молекулы имеют ненулевые размеры и испытывают упругие столкновения. Молекулы взаимно притягиваются, но сила притяжения быстро убывает с расстоянием. По существу сказанное означает, что между двумя молекулами, удаленными на расстояние R имеет место потенциал U(R) взаимодействия. Наиболее употребительным является современное представление
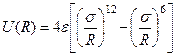 , (4.1)
, (4.1)
где e и s – константы.
Потенциал (4.1) называется потенциалом Леннарда – Джонса, его графическое представление U(R) приведено на рис. 4.1.
Так как сила F взаимодействия равна F = – dU/dR, то в точке R = Rmin сила F = 0. Нетрудно проверить, что Rmin = 21/6s. На расстояниях R > Rmin, где dU/dR > 0 и F < 0, молекулы притягиваются (рис. 4.2). Наоборот, если R < Rmin , то dU/dR < 0 и F > 0 и между молекулами происходит отталкивание.
Можно считать, что потенциал U(R) Леннарда – Джонса состоит из притягивающей U+ ~ R–6 и отталкивающей U– ~ R–12 частей.
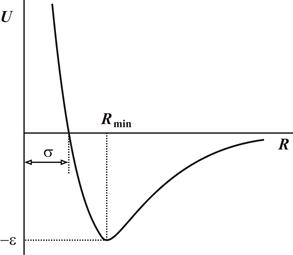
Рис. 4.1. График функции потенциала Леннарда – Джонса.
На рис. 4.2 молекулы изображены кружочками (с конкретными размерами) только для наглядности. На самом деле, согласно (4.1), они не обладают какими-либо конкретными размерами.
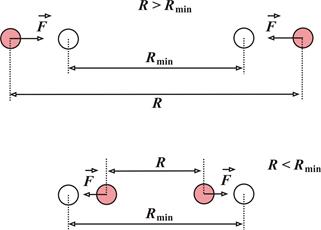
Рис. 4.2Притягивание при R > Rmin и отталкивание при R < Rmin молекул, согласно потенциалу Леннарда – Джонса.
Но по мере приближения (R ® 0) молекул сила отталкивания настолько быстро возрастает (~ 1/R12), что в скором времени полная кинетическая энергия налетающих друг на друга частиц полностью перейдет в потенциальную энергию, и в последующем частицы начнут разлетаться. При этом половину расстояния максимального сближения можно условно принять за размер молекул, т.к. это расстояние, вообще говоря, зависит от начальной кинетической энергии сталкивающихся молекул.
Вандерваальсово взаимодействие всегда существует между близко расположенными атомами, но играет важную роль лишь в отсутствие более сильных механизмов связи. Сила Ван-дер-Ваальса имеет частично электростатическую и частично квантово-механическую природу.
Согласно квантовой теории микрочастицы имеют нулевые колебания – движения, не прекращающиеся даже при абсолютном нуле температуры в силу принципа неопределенности. Нулевые колебания создают у каждого электрически нейтрального атома флуктуирующий дипольный момент с быстро меняющейся ориентацией и амплитудой. Поле, индуцируемое диполем, убывает пропорционально кубу расстояния. Таким образом, если ядра двух атомов находятся на расстоянии r друг от друга, диполь одного из атомов в каждый момент времени создает в точке, где находится другой диполь, мгновенное поле, пропорциональное 1/r3. При этом потенциальная энергия взаимодействия между диполями, приводящая к притяжению (второй член в формуле (4.1)), определяется как
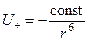 .
.
С уменьшением расстояния между атомами электронные облака атомов начинают перекрываться, возникает механизм, приводящий к ослаблению притяжения. Это можно понять с помощью принципа Паули, согласно которому в одном и том же квантовом состоянии не может находиться не более одного электрона. Таким образом, перекрытие электронных облаков двух атомов с почти заполненными электронными оболочками возможно лишь при переходе некоторых электронов в более высокие квантовые состояния или на более высокие орбиты, для чего требуется дополнительная энергия. Это обстоятельство проявляется как наличие силы отталкивания между атомами с потенциалом
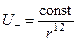 .
.
Потенциал Леннарда-Джонса применяется при моделировании многих систем, и на его основе проверена справедливость многих научных гипотез, нашли теоретическое объяснение множество экспериментальных фактов, рассчитаны важные кинетические параметры газов и жидкостей. Тем не менее, этот потенциал является лишь приближенным представлением формы и характера взаимодействия атомов и молекул. Наиболее точные результаты получаются для атомов аргона.
Дата добавления: 2018-11-26; просмотров: 863;










